Связывание пигментов в пигмент-белковых комплексах. Понятие и принцип строения фотосистемы.
Две пигментные фотосистемы – это две машины, движущие фотосинтез на световой стадии. Каждая состоит из реакционного центра и ансамбля молекул – светособирающих пигментов (пигмент-белковый комплекс – ПБК. Каждой фотосистеме соответствует свой отдельный набор пигментов, а также связанных с ними переносчиков электронов и в каждой фотосистеме происходят свои, только ей присущие фотосинтетические реакции.
В состав ФС I входят первая пигментная система с Р700, мономерная форма Хл а695, белки, содержащие железо и серу, 1–2 молекулы ферродоксина, по 1 молекуле цитохрома и пластицианина и 2 молекулы цитохрома b6;В состав ФС II – вторая пигментная система с Р680, 4 молекулы пластацианина, 2 молекулы цитохрома b559 и 6 атомов марганца. В ЭТЦ входит и пул пластахинонов – липидрастворимых переносчиков е– и Н+.
В состав светособирающих пигментов (светособирающие антены) входят: каротин, Хл а662, а670, а677, а684, а692 (ФС I) и ФС II: а622, а670, а677. Кроме того, имеется еще светособирающий белковый комплекс (ССК).
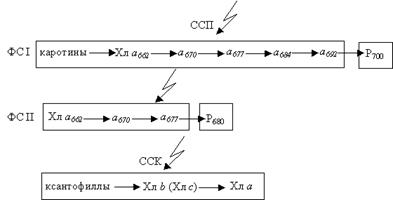
| Рис. 2.9. Схема организации ФС I и ФС II |
Считают, что при низкой интенсивности света собственные антенны ФС I и ФС II поглощают мало квантов света и поэтому не могут поддерживать необходимой скорости фотосинтезирующих реакций, и нужен дополнительный приток энергии, который обеспечит ССК. Наоборот, при высоких интенсивностях света пигментным системам не нужно столько энергии и поэтому они содержат значительно меньше ССК. В состав ССК входят ксантофиллы, хлорофилл b, некоторое количество хлорофилла а. ССК передает поглощенную энергию на ПБК и затем на реакционный центр. Получив эту энергию, специальная форма хлорофилла в реакционном центре переходит в возбужденное состояние (Хл*). Хл* обладает очень высокой реакционной способностью и является сильным восстановителем.
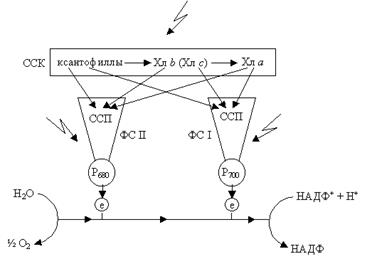
| Рис. 2.10. Схема взаимодействия пигментов ФС I, ФС II и светособирающего комплекса |
В окислительно-восстановительной системе А/А– происходит восстановление А до А–. От А– электрон переходит дальше и через другие компоненты электрон-транспортной цепи в конечном счете переносятся на НАДФ+. Хлорофилл, который отдал электрон, переходит в состояние свободного катиона – радикала Х+. Он возвращается в основное первичное состояние, получив электрон восстановленной формы Д– – второй окислительно-восстановительной системы Д/Д–. Окисленный Д восстанавливается до Д–, получая электрон от воды. 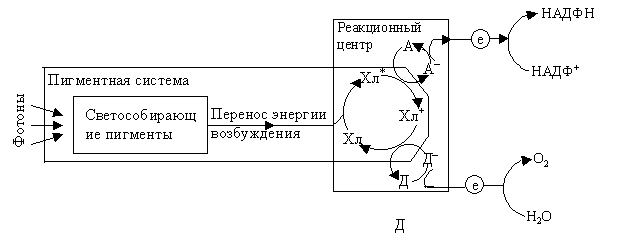 Рис. 2.11. Упрощенная схема работы пигментной системы
Рис. 2.11. Упрощенная схема работы пигментной системы
ФС (II) и ФС (I) размещаются последовательно в цепи транспорта электронов от Н2О до НАДФ+. Для восстановления одной молекулы НАДФ+ в процессе фотосинтеза необходимо два электрона и два протона, при этом донором электронов является вода. Фотоиндуцированное окисление воды происходит в ФС II, восстановление НАДФ+ – ФС I. Таким образом, фотосистемы должны функционировать во взаимодействии.
Исходя из данных квантового выхода фотосинтеза (количество выделенного О2 или связанного СО2 на 1 квант поглощенной энергии), необходимо восемь квантов света для выделения одной молекулы О2; из состава компонентов ФС I и ФС II и величины окислительно-восстановительного потенциала была разработана схема последовательности реакций в световой стадии фотосинтеза. Из-за подобия с буквой Z эта схема получила название Z-схемы. ФС I – единственная, имеющаяся у бактерий, работает без участия кислорода; эта ФС, вероятно, имела преимущества на ранних этапах биологической эволюции, когда кислорода в земной атмосфере было мало. С развитием ФС II растения получили возможность выделять молекулярный кислород из воды. Вероятно, это обстоятельство и определило изменения свойств земной атмосферы: из анаэробной она стала аэробной. Таким образом, фотохимическую работу у высших растений, выполняемую при фотосинтезе, в конечном счете, можно свести до разложения воды.
Реакционный центр ФС II включает кислород выделяющий комплекс, хлорофилл Р680, первичный акцептор электронов феофитин (Фео) – производное Хл, в котором Mg замещен протонами, и вторичные акцепторы – молекулы монохинона (Qн и Qв), а также пластохинон (Q). Ядро реакционного центра ФС II составляют два мембранных белка (D1 и D2) с молекулярной массой (ММ) 32 и 34 кД. Оба белка имеют по пять трансмембранных петель и служат основой для связывания большинства простетических групп, выполняющих функции переносчиков электронов. Другие белки (43 и 47 кД) ФС II входят в состав комплекса светособирающих пигментов или участвуют в выделении кислорода при фотоокислении воды (33, 23, 16 кД). Функции остальных белков с небольшой ММ, например цитохрома b559 и других, пока неизвестны.
В кислородвыделяющий комплекс входит Mn-содержащий пул и как кофакторы кальций и хлор. Посредником между кислородвыделяющим центром и хлорофиллом Р680 является остаток аминокислоты тирозина (Yz) белка D1.
Реакционный центр ФС I включает первичный донор электронов Хл Р700, первичный акцептор – Хл а (А0), промежуточный акцептор – филлохинон (А1), вторичные акцепторы – железосерные белки (FX, FA, FB), водорастворимы железосерный белок ферредоксин (ФД), растворимый флавопротеин – ферредоксин-НАДФ-редуктазу (ФП). ФС I представляет собой интегральный пигментбелковый комплекс с ММ около 340 кД.
Комплекс цитохром b6/f состоит из цитохрома b6, цитохрома f, железосерного белка Риске и субъединицы IV. Цитохром b6 и субъединица IV являются наиболее гидрофобными элементами комплекса. Простетическая группа цитохрома f представлена гемом с-типа, а аналогичная группа цитохрома b6 состоит из двух гемов b-типа, ковалентно связанных с остатками гистидина. Один гем называют высокопотенциальным (Н), второй низкопотенциальный (L).В передаче электронов от ФС II, а именно от комплекса b6/f к ФС I участвует пластоцианин (водорастворимый белок, содержащий два атома меди.
