Природа мембранного потенциала покоя.
Природа мембранного потенциала покоя.
Потенциал покоя – это разность между электрическими потенциалами внутри и вне клетки в состоянии покоя.
Величина ПП варьируется в пределах 30-90 мВ.
ПП составляет основу возбуждения и переработки информации нервной клеткой, обеспечивает регуляцию деятельности внутренних органов и опорно-двигательного аппарата посредством запуска процессов возбуждения и сокращения в мышце.
Главным ионом, обеспечивающим формирование ПП, является ион К+. В покоящейся клетке устанавливается динамическое равновесие между числом выходящих из клетки и входящих в клетку ионов К+. Электрический и концентрационный градиенты противодействуют друг другу: согласно концентрационному градиенту К+ стремиться выйти из клетки, а отрицательный заряд внутри клетки и положительный заряд наружной поверхности клеточной мембраны препятствуют этому. Когда концентрационный и электрический градиенты уравновесятся, число выходящих из клетки ионов К+ становится равным числу входящих ионов К+ в клетку. В этом случае на клеточной мембране устанавливается равновесный калиевый потенциал.
В создании ПП принимают участие и другие ионы: Na+, Cl¯, Ca²+.
Проницаемость клеточной мембраны в покое для Na+ очень низка. Ионы Na+ согласно концентрационному и электрическому градиентам стремятся и в небольшом количестве проходят внутрь клетки. Это ведет к уменьшению ПП, т.к. на внешней поверхности клеточной мембраны суммарное число положительно заряженных ионов уменьшается, а часть отрицательных ионов внутри клетки нейтрализуется входящими в клетку положительно заряженными ионами Na+.
Влияние Cl¯ на величину ПП противоположно влиянию Na+. Cl¯ согласно концентрационному градиенту стремиться и проходит в клетку. Концентрации ионов К+ и Cl¯ близки между собой. Но Cl¯ находится в основном вне клетки, а К+ - внутри клетки. Препятствует входу Cl¯ в клетку электрический градиент, поскольку заряд внутри клетки отрицательный, как и заряд Cl¯. Наступает равновесие сил концентрационного градиента, способствующего входу Cl¯ в клетку, и электрического градиента, препятствующего входу Cl¯ в клетку. При поступлении Cl¯ внутрь клетки число отрицательных зарядов вне клетки несколько уменьшается, а внутри клетки увеличивается: Cl¯ добавляется к крупным анионам белковой природы, находящимся внутри клетки. Таким образом, Cl¯, проникая внутрь клетки, увеличивает ПП.
Наружная и внутренняя поверхности клеточной мембраны несут собственные электрические заряды. Фиксированные наружные отрицательные заряды, нейтрализуя положительные заряды внешней поверхности мембраны, уменьшают ПП. Фиксированные внутренние отрицательные заряды клеточной мембраны, напротив, суммируясь с анионами внутри клетки, увеличивают ПП. Ионы Ca²+ взаимодействуют с наружными отрицательными фиксированными зарядами мембраны клетки, что ведет к увеличению и стабилизации ПП.
В целом ПП – это алгебраическая сумма не только всех зарядов ионов вне и внутри клетки, но и отрицательных внешних и внутренних поверхностных зарядов самой клеточной мембраны.
Билет 2.
Роль натрий-калиевого канала.
Основное назначение — поддерживать клеточный потенциал и регулировать клеточный объём.
Натрий-калиевый обменный насос
Большинство возбудимых клеток имеют потенциал покоя от —90 до - 60 мВ. Равновесный потенциал для ионов натрия (2JNa) — обычно порядка +50 мВ. Таким образом, существует большой электрохимический потенциал, стремящийся перенести ионы натрия внутрь клетки. Такой перенос осуществляется при помощи многочисленных механизмов. Кроме того, равновесный потенциал для калия более отрицателен, чем потенциал покоя, вследствие чего ионы калия постоянно выводятся из клетки. Для поддержания жизнеспособности клетки необходимо, чтобы ионы натрия непрерывно переносились наружу, а ионы калия внутрь клетки, т. е. против их электрохимических градиентов. Для этой цели в мембране клетки существует натрий-калиевый обменный насос, который при каждом своем цикле переносит три иона натрия наружу и два иона калия внутрь клетки.
Билет 3
Потенциал действия.
ПД – это электрофизиологический процесс, выражающийся в быстром колебании мембранного потенциала покоя вследствие перемещения ионов в клетку и из клетки и способный распространятся без затухания.
ПД обеспечивает передачу сигнала между нервными клетками, между нервными центрами и рабочими органами, в мышцах ПД обеспечивает процесс электромеханического сопряжения.
Величина ПД колеблется в пределах 80-130 мВ. Амплитуда ПД не зависит от силы раздражения, она всегда максимальна для данной клетки в конкретных условиях: ПД подчиняется закону «все или ничего», но не подчиняется закону силы.
При малом раздражении клетки ПД либо совсем не возникает, либо достигает максимальной величины, если раздражение является пороговым или сверхпороговым.
Выделяют три фазы ПД:
1. деполяризация – исчезновение заряда клетки (уменьшение мембранного потенциала до нуля)
2. инверсия – изменение заряда клетки на обратный, когда внутренняя сторона мембраны клетки заряжается положительно, а внешняя – отрицательно
3. реполяризация – восстановление исходного заряда клетки, когда внутри клетки заряд снова становится отрицательным, а снаружи – положительным.
Фаза деполяризации: При действии деполяризующего раздражителя на клетку (например, электрического тока) начальная деполяризация клеточной мембраны происходит без изменения ее проницаемости для ионов. Когда деполяризация достигает примерно 50% порогового потенциала, возрастает проницаемость мембраны клетки для Na+. Условием, обеспечивающим вход Na+ в клетку, является увеличение проницаемости клеточной мембраны, которая определяется состоянием воротного механизма Na–каналов (расположен на внешней и внутренней сторонах клеточной мембраны). Когда деполяризация клетки достигает критической величины – 50 мВ, проницаемость мембраны для Na+ резко возрастает: открывается большое число Na-каналов и Na+ лавиной устремляется в клетку. В результате интенсивного тока Na+ внутрь клетки процесс деполяризации проходит очень быстро. В итоге ПП (потенциал покоя) исчезает, становится равным нулю. Фаза деполяризации на этом заканчивается.
Фаза инверсии: После исчезновения ПП вход Na+ в клетку продолжается, поэтому число положительных ионов в клетке больше числа отрицательных ионов, заряд внутри клетки становится положительным, снаружи – отрицательным. Теперь электрический градиент препятствует входу Na+ внутрь клетки (положительные заряды отталкиваются друг от друга), Na-проводимость снижается. Тем не менее некоторое время Na+ продолжает входить в клетку, о чем свидетельствует продолжающее нарастание ПД. Это означает, что концентрационный градиент, обеспечивающий движение Na+ в клетку, сильнее электрического, препятствующего входу Na+ в клетку. Примерно через 0,5-2 мс после начала деполяризации рост ПД прекращается в результате закрытия Na и открытия K-каналов, т.е. вследствие увеличения проницаемости для K+ резкого возрастания выхода его из клетки. K+ выталкивается положительным зарядом из клетки и притягивается отрицательным зарядом снаружи клетки. Так продолжается до полного исчезновения положительного заряда внутри клетки – до конца фазы инверсии.
Фаза реполяризации связана с тем, что проницаемость клеточной мембраны для K+ все еще высока, K+ продолжает быстро выходить из клетки. Поскольку клетка теперь снова внутри имеет отрицательный заряд, а снаружи – положительный, электрический градиент препятствует выходу K+ из клетки, что снижает его проводимость, хотя он продолжает выходить. Часто в конце ПД наблюдается замедление реполяризации, что объясняется уменьшением проницаемости клеточной мембраны для K+.
Главную роль в возникновении ПД играет Na+, обеспечивающий всю восходящую часть пика ПД.
Билет 5.
Вопрос 6.
Билет 7.
O Классификация по Ллойду
Классифицирует только афферентные нейроны.
| Тип волокна | Функция | Диаметр, мкм | Скорость проведения, м/с | Миелинизация |
| Ia | Мышечные веретёна | 18-22 | 90-120 | + |
| Ib | Сухожильные рецепторы | 15-18 | 60-90 | + |
| II | Механорецепторы кожи, вторичные мышечные веретёна | 7-15 | 40-90 | + |
| III | Рецепторы связок | 1-5 | 3-25 | прерывистая |
| IV | Болевые рецепторы, рецепторы соединительной ткани | 0,1-1 | 0,5-2 | - |
9. Значение миелиновой оболочки и перехватов Ранвье в проведении возбуждения по нервному волокну
Дубинин –
"Если ПД (потенциал действия) возник в некоторой точке 1 мембраны (рис. 3.17, а), он начинает выполнять функцию запускающего стимула по отношению к соседним областям. При этом ток натрия, формирующий первую фазу ПД, оказывает действие, аналогичное влиянию деполяризующего электрического стимула. В результате потенциал-зависимые ионные каналы на еще не активированной мембране начинают открываться, и ПД делает первый шаг. Развившись в точке 2, ПД запускает возбуждение в точке 3 и т. д. Этот процесс можно уподобить волне, расходящейся по воде от места падения камня.
В ходе этого распространения фронт ПД движется от точки возникновения в разные стороны без «возвратов» назад, так как только что сработавшая мембрана приходит в состояние абсолютной рефрактерности. В каждый момент времени она может проводить сигнал только в одном направлении, и повторное проведение возможно лишь после возврата потенциал-зависимых каналов в состояние готовности.
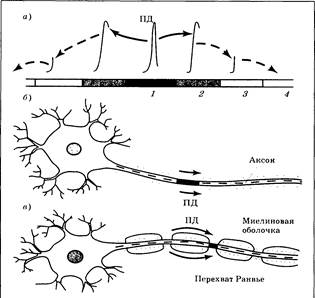
Рис. 3.17. Схемы распространения ПД по нервным клеткам: а — общая схема; б — распространение ПД по немиелинизированному (безмякотному) волокну (1, 2, 3, 4 — участки мембраны нейрона); в — распространение ПД по миелинизированному волокну
Необходимость открывания ионных каналов на последовательных участках мембраны делает проведение ПД весьма медленным — около 0,5—1 м/с (рис. 3.17, б), при этом ширина одномоментно активированной зоны (фронт ПД) составляет примерно 1 мм.
Скорость распространения можно увеличить, делая нервные волокна более толстыми: в гигантском аксоне кальмара при толщине 1 мм она достигает 10 м/с. Другой путь — формирование миелиновых оболочек. В этом случае очередным возбужденным участком при проведении ПД будет не соседняя точка мембраны, а ближайший перехват Ранвье. В результате импульс будет распространяться прыжками (сальтаторно; рис. 3.17, в), развиваясь только на участках аксона, не закрытых Шванновскими клетками. Ширина таких участков — 0,5 мкм (против 1 мм для миелинового сегмента). Скорость «прыжка» определяется толщиной миелиновой оболочки. При общем диаметре волокна 1 мкм она составляет 3 м/с, при максимальном диаметре 22 мкм — 120 м/с. Кроме резкого увеличения скорости проведения, сальтаторный вариант является очень экономичным, поскольку изменения ионного баланса в результате ПД происходят только в зоне перехватов.
Скорость, близкая к 100 м/с, характерна для передачи кожной и мышечной чувствительности, двигательных команд. Именно задержки, возникающие при такой передаче, определяют латентный (скрытый) период простых сенсомоторных реакций. Он составляет около 20 мс, что соответствует «длине пути» нервного импульса — около 2 м (по руке к спинному мозгу и обратно).
Конечной целью бегущего по нерву ПД являются пресинаптические окончания, где электрический сигнал превращается в химический, и скачок потенциала на мембране запускает выделение медиатора, т. е. пока сигнал остается в «границах» одного нейрона, он передается в электрической форме (ПД). Для передачи между нейронами информация преобразуется в химическую форму (медиатор). Подействовав на постсинаптическую мембрану, медиатор вновь переводит сигнал в электрическую форму (ВПСП, ТПСП, запуск ПД)."
Смирнов –
"Сальтаторный типпроведениянервного импульса осуществляется в миелиновых волокнах (типа А и В), для которых характерна концентрация потенциалзависимых ионных каналов только в небольших участках мембраны "Перехваты Ранвье", где их плотность достигает 12000 на 1 мкм2, что примерно в 100 раз выше, чем в мембранных безмиелиновых волокон. В области миелиновых муфт (межузловые сегменты длиной 1-2 мм), обладающих хорошими изолирующими свойствами, потенциал-зависимых каналов почти нет, и мембрана осевого цилиндра там практически невозбудима. В этих условиях ПД, возникший в одном перехвате Ранвье, электротонически (без участия ионных каналов) распространяется до соседнего перехвата, деполяризуя там мембрану до критического уровня, что приводит к возникновению нового ПД, т.е. возбуждение проводится скачкообразно.
Постоянная длины мембраны миелинового волокна достигает 5 мм. Это значит, что ПД, распространяется электротонически на этом расстоянии, сохраняет 37% своей амплитуды (около 30 мВ) и может деполяриховать мембрану до критического уровня (пороговый потенциал в перехватах Ранвье равен около 15 мВ), поэтому в случае повреждения ближайших на пути следования перехватов Ранвье потенциал действия может электротонически возбудить 2-4-й и даже 5-й перехваты (фактор надежности).
Сальтаторное поведение ПД по миелиновым волокнам является эволюционно более поздним механизмом, возникшим впервые у позвоночных. Оно имеет два важных преимущества оп сравнению с непрерывным проведением возбуждения. Во первых, оно более экономично в энергетическом плане, т.к. возбуждаются только перехваты Ранвье, площадь которых менее 1% мембраны, и, следовательно, надо меньше энергии для восстановления трансмембранных градиентов Na+ и Ka+, уменьшающихся в процессе формирования ПД. Во вторых, возбуждение проводится с большей скоростью, чем в безмиелиновых волокнах, так как возникший ПД на протяжении миелиновых муфт распространяется электротонически, что в 107 раз быстрее, чем скорость физиологического проведения ПД."
Проведение нервного импульса от тела нейрона к окончанию аксона различается в немиелинизированных и имелинизированных волокнах.
Безмиелиновые нервные волокна. В покое мембрана аксона (осевого цилиндра) поляризована — положительно заряжена снаружи и отрицательно внутри. При ПД полярность изменяется, и наружная поверхность мембраны приобретает отрицательный заряд. Из-за разности потенциалов между возбуждённым и невозбуждёнными сегментами возникают локальные токи, деполяризующие соседний участок мембраны. Теперь этот участок становится возбуждённым и деполяризует следующий участок мембраны. Такое проведение известно как электротоническое, а проведение ПД — своего рода «эстафета», в которой каждый участок мембраны является сначала раздражаемым, а затем раздражающим. ПД возникает за счёт увеличения проводимости через потенциалозависимые Na+ каналы, встроенные в аксолемму с плотностью около 110–120 каналов на 1 мкм2. Появление так называемых рефрактерных каналов (рефрактерное состояние мембраны после прохождения ПД) предупреждает распространение возбуждения в обратном направлении. Скорость проведения возбуждения по безмиелиновому нервному волокну в основном составляет 0,5–2 м/с и зависит от диаметра волокна: чем больше диаметр, тем выше скорость проведения ПД.
Миелиновое нервное волокно. состоит из осевого цилиндра (аксона), вокруг которого шванновские клетки образуют миелин за счёт концентрического наслаивания собственной плазматической мембраны. Миелин прерывается через регулярные промежутки (от 0,2 до 2 мм) концентрической щелью шириной около 1 мкм, это узлы, или перехваты Ранвье. Таким образом, межузловые сегменты аксона, расположенные между соседними перехватами Ранвье, содержат миелин — электрический изолятор, не позволяющий проходить через него локальным токам, поэтому ПД возникают только в перехватах Ранвье. Другими словами, ПД перемещается вдоль нервного волокна скачками, от одного перехвата Ранвье к другому перехвату (скачкообразное проведение).
? Плотность потенциалозависимых Na+ каналов аксолеммы в перехватах Ранвье — до 2000 на 1 мкм2 (в перикарионе — 50–70, в начальном сегменте аксона — 2000, в межузловых сегментах Na+ каналы практически отсутствуют). В силу высокой плотности Na+ каналов перехваты Ранвье характеризуются высокой возбудимостью, а локальные токи достаточно велики для возбуждения соседнего перехвата.
? Локальные токи текут от перехвата к перехвату (через внеклеточную жидкость кнаружи от миелина и через аксоплазму внутри аксона) с минимальными потерями.
? Скорость проведения ПД в миелиновых волокнах в десятки раз выше, чем в наиболее «быстрых» безмиелиновых аксонах.
? Энергозатраты нервного волокна на проведение ПД относительно невелики, поскольку возбуждаются только перехваты Ранвье, площадь которых составляет менее 1% общей поверхности мембраны аксона. Поэтому даже после длительных ритмических пачек ПД трансмембранный градиент концентраций ионов практически не изменяется.
? В физиологических условиях ПД движутся в одном направлении от места раздражения (ортодромное проведение). ПД, проходящий по нервному волокну, возбуждает следующий, но не предыдущий участок мембраны. Это связано с рефрактерностью предыдущего участка после возбуждения. Проведение в противоположном направлении (антидромное проведение) возможно при травматическом поражении нервных волокон и в редких случаях (аксон–рефлекс).
? Нарушение миелинизации нервных волокон приводит к нарушениям проводимости (демиелинизирующие заболевания). При разрушении миелиновой оболочки происходит резкое снижение скорости и надёжности проведения возбуждения по нервам. Наиболее распространённым среди демиелинизирующих заболеваний является множественный склероз, проявляющийся различными параличами и потерей чувствительности.
См. предыдущий билет
Волна ожидания.
Е–волна (англ. expectation – ожидание) — ритм мозга, описанный Г. Уолтером, который представляет собой отрицательное изменение электрического потенциала в передних отделах коры мозга между действием настраивающего сигнала и пускового, требующего какую–либо реакцию испытуемого. Свидетельствует о состоянии готовности действовать при восприятии сигнала. Возникает через 0,5 с. после действия настраивающего сигнала. Ее амплитуда прямо связана со скоростью требуемой двигательной реакции, а также с напряжением внимания или воли, что позволяет рассматривать ее как проявление действия механизмов произвольного поведения человека.
Далее сотрудники Уолтера стали применять два следующих друг за другом стимула: щелчок, а затем вспышка. Сначала лоб отвечал на тот и другой раздражитель. Потом реакция исчезла.
Но вот методику усложнили.
Испытуемых, когда они видят вспышки, Уолтер просил нажимать на кнопку. Таким образом, щелчок превращался в предупредительный сигнал, словно желтый свет светофора, а вспышки - в императивный, приказывающий сигнал.
Почти сразу же после щелчка с помощью электродов, расположенных вблизи фронтальной коры, была зарегистрирована негативная (направленная вверх от нулевой линии) волна амплитудой примерно 30 микровольт. Она длилась до появления вспышек, что обычно совпадало с нажатием на кнопку. Эту волну Уолтер назвал волной ожидания (expectancy wave, или Е-волна). Ничего подобного не сообщали электроды, установленные на темени, виске и затылке.
Исследователь считает, что Е-волна может действовать как "корковый запал", как "заряд взрывчатки", вызывающий синхронную детонацию или разряд корковых нейронов, отвечающих за движение. Действительно, движения руки, которой нажимали кнопку, происходили тем быстрее и точнее, чем более крупной была Е-волна.
Регистрировали ее и тогда, когда надо было выполнить умственную работу, и у велосипедиста, который по радио получил приказ "стой", и у баскетболиста, когда он видел летящий на него мяч. Но как только мяч был пойман, Е-волна исчезла. У ребенка до 3-4 лет Е-волну получить невозможно. У детей старшего возраста она возникает только тогда, когда приказывает взрослый человек, пользующийся их доверием. Но если тот же приказ они слышат от молодой лаборантки, никакой Е-волны не появится.
Электрические синапсы.
Электрические синапсы представляют собой довольно плотные контакты между клетками (ширина синаптической щели всего около 2 нм), благодаря чему нервный импульс «перескакивает» с пресинаптической на постсинаптическую мембрану. Дополнительно в электрическом синапсе между пресинаптической и постсинаптической мембраной существуют т.н.мостики, представляющие собой белки-каналы, через которые могут проходить мелкие молекулы и ионы. Благодаря таким каналам не происходит потерь сигнала в результате утечки электрического тока через внеклеточную среду. Вследствие этого изменения потенциала в пресинаптическом окончании могут передаваться на постсинаптическую мембрану практически без потерь.
Электрические синапсы и их морфологический субстрат - щелевые контакты- были обнаружены в самых разных отделах нервной системы беспозвоночных и низших позвоночных животных. В мозге млекопитающих также встречаются электрические синапсы. Они обнаружены в стволе головного мозга: в ядре тройничного нерва, в вестибулярном ядре Дейтерса, в нижней оливе продолговатого мозга.
Проведение возбуждения в таких синапсах осуществляется быстро, с небольшой задержкой или даже без задержки. Электрические синапсы обладают как односторонним, так и двусторонним проведением возбуждения. Это легко доказать при регистрировании электрического потенциала на синапсе: при раздражении афферентных путей мембрана синапса деполяризуется, а при раздражении эфферентных волокон - гиперполяризуется. Оказалось, что синапсы нейронов с одинаковой функцией обладают двусторонним проведением возбуждения (например, синапсы между двумя чувствительными клетками). В таких синапсах ток возможен в обоих направлениях, но иногда сопротивление в одном из направлений выше, чем в другом (выпрямляющий эффект). Синапсы между разнофункциональными нейронами (сенсорные и моторные) обладают односторонним проведением. Электрические синапсы позволяют синхронизировать активность групп нейронов, они дают возможность получать постоянные, стереотипные реакции при многократных воздействиях, т.к. они в меньшей степени, чем химические синапсы, подвержены метаболическим и прочим влияниям.
Химические синапсы.
Ацетилхолин.
По химическому строению ацетилхолин представляет собой соединение двух молекул — азотсодержащего холина и остатка уксусной кислоты:
Ацетилхолин в качестве медиатора работает в трех функциональных блоках нервной системы: в нервно-мышечных синапсах, периферической части вегетативной нервной системы и некоторых областях ЦНС.
Ацетилхолин является медиатором мотонейронов нервной системы, которые расположены в передних рогах серого вещества спинного мозга и двигательных ядрах черепных нервов. Их аксоны направляются к скелетным мышцам и, разветвляясь, образуют нервно-мышечные синапсы.
В ЦНС ацетилхолин вырабатывается частью нейронов ретикулярных ядер моста и интернейронами полосатого тела базальных ганглиев и некоторых других локальных зон. Рассматривается роль этого медиатора в регуляции уровня бодрствования, а также в системах памяти, двигательных системах. Доказана эффективность применения антагонистов ацетилхолина при ряде двигательных нарушений.
Выделяясь из пресинаптического окончания, ацетилхолин действует на постсинаптические рецепторы. Эти рецепторы неоднородны и различаются локализацией и рядом свойств. Выделено два типа рецепторов: первый, помимо ацетилхолина, возбуждается под действием алкалоида табака никотина (никотиновые рецепторы), второй тип активируется ацетилхолином и токсином мухомора мускарином (мускариновые рецепторы).
В периферической НС ацетилхолин является основным медиатором нервно-мышечного синапса, действуя на никотиновые холинорецепторы.
В вегетативной нервной системе ацетилхолин осуществляет передачу в симпатических и парасимпатических ганглиях (выделяется из окончаний преганлионарных волокон), а также влияет на работу внутренних органов, выделяясь из периферических окончаний парасимпатических нервов (мускариновые рецепторы).
Аминокислоты.
Медиаторы-аминокислоты являются самыми распространёнными медиаторами в НС. До 80% нейронов выделяют из своих окончаний аминокислоты в качестве медиаторов.
1. Возбуждающие аминокислоты.
Глутаминовая кислота – основной возбуждающий медиатор в ГМ. Образуется в мозге из глюкозы. Больше всего глутамата в конечном мозге и мозжечке. Принимает участие в процессах памяти, является медиатором сенсорных путей.
Аспаргиновая кислота – возбуждающий медиатор среднего мозга, нижней оливы продолговатого мозга и серого вещества спинного мозга. АК регулирует спинномозговые рефлексы.
Обе возбуждающие аминокислоты участвуют в регуляции состоянии беспокойства.
2. Тормозные аминокислоты.
Гамма-аминомасляная кислота (ГАМК) – образуется в мозге из глутаминовой кислоты. Много ГАМК в коре больших полушарий, в коре мозжечка, в чёрной субстанции среднего мозга, в сетчатке глаза.
Успокаивающий, усыпляющий эффект. Нельзя использовать, т.к. не проходит ГЭБ.
ГАМКа – ионотропные, ГАМКб – метаботропные.
Нарушение ГАМК-эргической системы – эпилепсия, расстройство сна, дисфункции в сердечно-сосудистой системе.
Глицин – тормозной медиатор спинного и в меньшей степени ГМ. Тела синтезирующий глицин нейронов в основном в спинном и продолговатом мозге, в ядрах черепномозговых нервов, в промежуточном мозге. Только один тип рецепторов – ионотропный. Глицин обеспечивает возвратное торможение мотонейронов спинного мозга, уменьшает психомоторную расторможенность.
Пуриновые медиаторы.
Пурины – группа природных азотистых гетероциклических соединений и их производных. В качестве модулятором и в меньшей степени медиаторов встречаются в основном аденозин, а также АТФ(аденозинтрифосфорная кислота). Пурины действуют через особый тип рецепторов – пуриновые, основной из которых – метаботропный А1-рецептор. Рецепторы действуют в периферической НС, в афферентных окончаниях болевых волокон.
Аденозин – нейромодулятор, оказывает в основном тормозное влияние на возбуждающие синапсы.
Физиологическая роль пуринэргической системы в том, что при длительной нагрузке на мозг в нём образуется большое количество АМФ (аденозинмонофосфорной кислоты), которая тормозит работу синапсов через А1-рецепторы, защищая ЦНС в экстремальных условиях. А вещества, блокирующие работу этих рецепторов, способны активизировать НС: кофеин, теофилин, теобромин.
Пептидные медиаторы.
Это вещества, состоящие из цепочек аминокислот. Первым из них было открыто вещество Р(от powder — порошок), выделенное из сухого порошка спинного мозга. Его введение в кровь в очень малых дозах вызывает расширение кровеносных сосудов и спазм кишечника.
Наиболее изученной группой пептидных медиаторов считаются опиоидные пептиды.Их название происходит от опиума — субстанции, выделенной из мака и обладающего анальгетическим и эйфорическим действием. Под влиянием опиума по мере увеличения дозы наблюдается обезболивание, успокоение и засыпание. В 1803 г. было выделено основное действующее начало опиума, названное морфином. Показано, что обезболивающие эффекты морфина осуществляются через задние рога спинного мозга, через гипоталамус, где расположен центр положительных эмоций. Засыпание связано с общим торможением стволовых структур. Сверхбольшие дозы морфина могут вызвать остановку дыхания.
Синтез медиаторов-пептидов (в том числе опиоидных) протекает значительно сложнее по сравнению с синтезом медиаторов других групп. В ходе этого процесса рибосомы вначале строят белок-предшественник, а затем особые ферменты вырезают из него необходимые фрагменты, причем один белок может содержать внутри себя несколько медиаторов-пептидов.
Основной механизм действия опиоидов в ЦНС — пресинаптическое торможение выделения медиаторов.
Существуют нейропептиды, избирательно управляющие половым поведением, пищевой мотивацией, терморегуляцией. В целом соединения этой группы образуют сложную иерархическую систему, в которой одни нейропептиды активируют или подавляют высвобождение других нейропептидов. Последние способны воздействовать как на метаболизм нейронов, так и на функционирование «классических» медиаторных систем; при этом сфера влияний конкретного нейропептида часто ограничивается узким кругом эффектов, связанных, например, только с какой-либо одной биологически значимой потребностью или с определенным типом памяти.
Стволовые клетки
Найдены не только в основных регенерирующих тканях, таких, как эпителий и кровь, но также в статических тканях, таких, как нервная система и печень, где они играют центральную роль в тканевом росте и сохранении. Механизм, с помощью которого стволовые клетки поддерживают популяции высоко дифференцированных короткоживущих клеток, как кажется, включает критический баланс между альтернативными путями (судьбами): дочерние клетки либо сохраняют идентичность стволовых клеток, либо инициируют дифференциацию. Недавние исследования на низших организмах выявили регуляторный механизм ассимитричных клеточных делений стволовых клеток. В этих моделях окружение, вероятно, обеспечивает ключевые инструктивные сигналы для выбора судьбы клеток. Наше понимание сейчас распространяется на внутренние механизмы клеточной полярности, которая влияет на ассиметричные деления стволовых клеток/12
Вот, что нашла. Из 1-ой лекции по анатомии.
Хотя сами по себе нервные клетки могут размножаться и восстанавливаться. Например, стволовые клетки. Какое-то количество дендритов не специализируется и в случае необходимости стволовые клетки получают сигнал о необходимости «прийти на помощь», они прибывают на место повреждение и начинают специализироваться. Например, при инсульте значительная часть клеток гибнет, а некоторая восстанавливается из стволовых клеток.
Дубинин
Альфа — 8—13 Гц,
Бета — 14—40 Гц,
Тета — 4—6 Гц,
Дельта — 0,5—3 Гц,
Гамма — выше 40 Гц и др.).
У здорового взрослого человека при закрытых глазах регистрируется основной альфа-ритм. Это так называемая синхронизированная ЭЭГ.
При открытых глазах или при поступлении сигналов от других органов чувств происходит блокада альфа-ритма и появляются бета-волны. Это называется десинхронизацией ЭЭГ.
Тета-волны и дельта-волны в норме у бодрствующих взрослых не выявляются, они появляются только во время сна.
Для ЭЭГ подростков и детей напротив характерны более медленные и нерегулярные дельта-волны даже в бодрствующем состоянии.
В зависимости от частотного диапазона, но также и от амплитуды, формы волны, топографии и типа реакции различают ритмы ЭЭГ, которые также обозначают греческими буквами. Например, альфа-ритм, бета-ритм, гамма-ритм, дельта-ритм, тета-ритм, каппа-ритм, мю-ритм, сигма-ритм и др. Считается, что каждый такой «ритм» соответствует некоторому определённому состоянию мозга и связан с определёнными церебральными механизмами.
Пространственная суммация.
(рис. 4.7, б) Раздельная стимуляция каждого из двух аксонов вызывает подпороговый ВПСП, тогда как при одновременной стимуляции обоих аксонов возникает ПД – процесс, который не может быть обеспечен одиночным ВПСП. Пространственная суммация связана с такой особенностью распространения возбуждения, как конвергенция.
Последействие – это продолжение возбуждения нервного центра после прекращения поступления к нему импульсов по афферентным нервным путям. Последействие вызывает ряд причин: а) длительное существование ВПСП (полисинаптического или высокоамплитудного), когда при одном ВПСП возникает несколько ПД; б) многократные появления следовой деполяризации, что свойственно нейронам ЦНС (при Екр возникает ПД); в) циркуляция возбуждения по замкнутым нейронным цепям. Существование ВПСП и многократные появления следовой деполяризации действуют десятки-сотни миллисекунд, циркуляция возбуждения может продолжаться минуты и даже часы. Последействие играет важнейшую роль в процесса обучения (кратковременная память).
Медиаторы и рецепторы.
1. преганглионар. нейроны и рецепторы ганглионар. нейронов. Эфферентный вход в вегетативном ганглии (экстра- и интрогенный) представлен возбуждающим холинергическим преганглионаным волокном, образующим синапс с ганглионар. нейроном при помощи Н-холинорецепотра (медиатор – ацетилцелин). Рецептор получил своё название (Д. Ленги) из-за чувствительности к никотину: малые его дозы возуждают нейрон, малые – блокируют. В вегетативных ганглиях кроме него имеются различные нейропептиды (М-холинорецепторы, вставочные адренергические клетки, регулирующие возбудимость нейронов).
2. От ганглионарных нейронов отходят постганглионар. симпат. волокна, в окончаниях которых главным медиатором явл. норадреналин – около 90%. Он синтезируется из аминокислоты тирозина в аксоне ганглионар. нейрона, в основном в терминал. симпат. окончаниях, около 1% - в теле нейрона. В ответ на раздражение симпат. нейрона вместе с норадреналином выдел. также белок хромагрин дофамин-β-гидроксилаза, мет-энкефалин. Эту смесь дополняют медиаторы соседних нервных окончаний, гормоны, метаболиты и ионы эффекторных клеток.
3. Инактивация медиатора. 75-80% выделившегося в синаптическую щель норадреналина захватывается обратно пресинаптической мембраной и поступает в пузырьки. Не попавший туда норадреналин разрушается моноаминоксидазой (МАК), локализованной на пресинаптич. мембране. Часть выделившегося в синаптич. щель и не связавшегося с пост- и пресинаптич. рецепторами норадреналина разрушается в области рецепторов постсинаптич. Мембраны ферментом катехол-О-метилтран… феразой (КОМТ) клеточных эффекторов, другая – диффундирует в интерстиций… кровь. Вклад МАО и КОМТ в процессы инактивации выделившихся в синаптич. щель катехоламинов невелик, а доля участия этих ферментов в разных органах и тканях различна: в ЦНС действует в основном МАО, в периферич. симпат. НС – КОМТ.
4. Эффекторные рецепторы. Выделившийся норадреналин действует на α- и β-постсинаптич. адренорецепторы, являющиеся …гликопротедами. Это деление рецепторов основано на чувствительности их к различным фармакологическим препаратам: α-адренорецепторы блокируются фентоламином, а β- - пропранолом. Оба типа рецепторов дел. на 2 подтипа: α1 и α2, β1 и β2-адренорецепторы. В больш-ве органов, реагирующих на катехоламины, содержатся оба рецептора.
Связь постгаглионар. симпат. окончаний с адренорецепторами. Считается, что симпат. иннервацию имеют только α1 и β1-адренорецепторы, которые активизируются в основном медиатором норадреналином. α2- β2- преимущественно не имеют иннервации, расположены вне синапсов на клетках-эффекторах и активизируются циркулирующим в крови адреналином и диффундиру
