ИСПАРЕНИЕ ЖИДКОСТИ. Насыщеный и ненасыщеный пар
Изотерма реального газа. Кипение жидкости. Влажность воздуха.
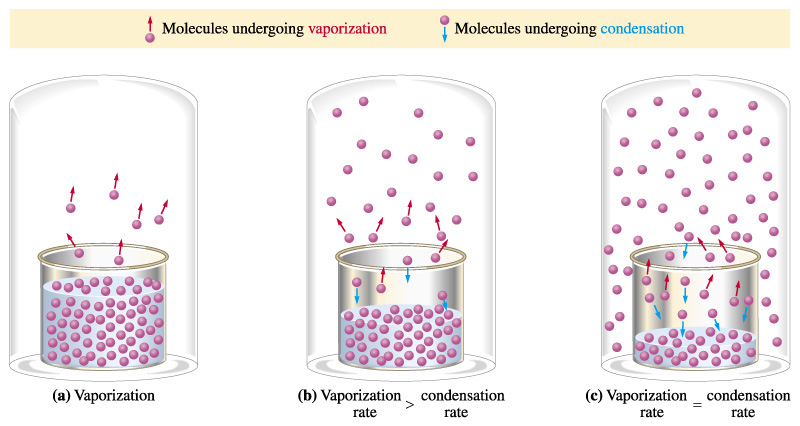 Как известно из опыта, жидкости способны испаряться, т.е. переходить в газообразное состояние. Чтобы молекула, находящаяся вблизи поверхности, оторвалась от жидкости, она должна совершить некоторую работу, связанную с наличием сил молекулярного притяжения. Эту работу обычно называют работой выхода. Работа выхода совершается за счёт кинетической энергии молекул и условием испарения будет mυ2/2>Авых. Из опыта Штерна известно, что при любой температуре имеются молекулы с достаточно большими скоростями, значит, процесс испарения должен наблюдаться при любой температуре. Испарение наблюдается не только у жидкости, но и у твёрдых тел. Испарение твёрдых тел, минуя жидкое состояние, называется сублимацией или возгонкой. Хорошо испаряются такие вещества, как лёд, нафталин, сера, йод и т. д. Интенсивность испарения зависит от рода вещества, площади свободной поверхности, от температуры, конвекции в жидкости, давления над поверхностью жидкости. При испарении уменьшается масса вещества и происходит охлаждение жидкости, так как жидкость покидают молекулы с наибольшим значением энергии.
Как известно из опыта, жидкости способны испаряться, т.е. переходить в газообразное состояние. Чтобы молекула, находящаяся вблизи поверхности, оторвалась от жидкости, она должна совершить некоторую работу, связанную с наличием сил молекулярного притяжения. Эту работу обычно называют работой выхода. Работа выхода совершается за счёт кинетической энергии молекул и условием испарения будет mυ2/2>Авых. Из опыта Штерна известно, что при любой температуре имеются молекулы с достаточно большими скоростями, значит, процесс испарения должен наблюдаться при любой температуре. Испарение наблюдается не только у жидкости, но и у твёрдых тел. Испарение твёрдых тел, минуя жидкое состояние, называется сублимацией или возгонкой. Хорошо испаряются такие вещества, как лёд, нафталин, сера, йод и т. д. Интенсивность испарения зависит от рода вещества, площади свободной поверхности, от температуры, конвекции в жидкости, давления над поверхностью жидкости. При испарении уменьшается масса вещества и происходит охлаждение жидкости, так как жидкость покидают молекулы с наибольшим значением энергии.
Пар, находящийся в равновесии с жидкостью, когда процессы испарения и конденсации идут в одинаковой мере, называется насыщенным. Если такого равновесия не наблюдается, то пар называется ненасыщенным или пересыщенным. Давление ненасыщенного пара меньше давления насыщенного при той же температуре. Для пересыщенного пара это соотношение противоположное. Насыщенный пар имеет место в закрытых сосудах, с достаточно большим количеством жидкости. В таком сосуде наряду с испарением наблюдается и конденсация, причем эти процессы уравновешивают друг друга. В открытых сосудах, как правило, процесс испарения преобладает над конденсацией, равновесие пара и жидкости отсутствует.
Ненасыщенный пар подчиняется всем газовым законам. Насыщенный пар газовым законам не подчиняется. Проведем сравнение свойств ненасыщенного и насыщенного паров.
Рассмотрим поведение ненасыщенного и насыщенного паров в изотермическом процессе, когда температура газа остается постоянной. Для этого тот и другой газ поместим в цилиндр с поршнем. При сжатии ненасыщенного пара его давление будет возрастать, а масса оставаться постоянной. Пар будет подчиняться закону Бойля-Мариотта. Изотерма ненасыщенного пара представляет собой гиперболу. Если сжимать насыщенный пар, то он начнет превращаться в жидкость, его масса будет уменьшаться, а давление оставаться постоянным. Познакомимся с поведением ненасыщенного и насыщенного паров при их нагреве, если объем при этом будет оставаться постоянным. При нагреве ненасыщенного пара его масса будет оставаться постоянной, а давление возрастать прямо пропорционально температуре. Ненасыщенный пар подчиняется закону Шарля. Теперь обратимся к насыщенному пару. Чтобы пар оставался насыщенным, в сосуде должна присутствовать жидкость. При нагреве насыщенного пара часть жидкости будет превращаться в пар. Масса пара при этом возрастает, а линейная зависимость между давлением и температурой нарушается. Надо отметить, что с ростом температуры возрастает как кинетическая энергия молекул насыщенного пара, так и их концентрация. На этих примерах было показано, что насыщенные пары не подчиняются газовым законам.
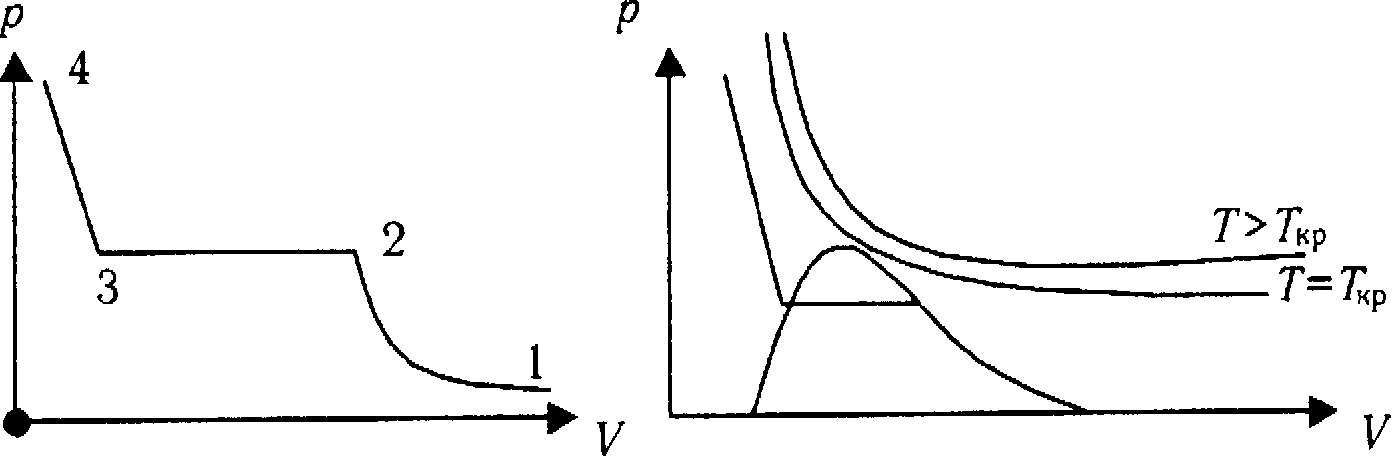 Теперь рассмотрим переход ненасыщенного пара в насыщенный пар, а потом в жидкость. Если ненасыщенный пар сжимать при постоянной температуре, то давление и плотность газа будут возрастать и при некотором давлении пар становится насыщенным. Дальнейшее сжатие газа будет происходить при неизменном давлении до тех пор, пока пар полностью не превратится в жидкость. Эти процессы можно изобразить диаграммой, указанной на рисунке. Участок 1-2 соответствует изотерме ненасыщенного пара, 2-3 — изотерме насыщенного пара, 3-4 — жидкости. При увеличении температуры получим ряд таких изотерм, которые изображены на втором рисунке. Они показывают, что с ростом температуры область существования насыщенного пара уменьшается и при некоторой температуре насыщенный пар не образуется. Такое состояние газа называется критическим. При температурах Т > Ткр газ в жидкость не переводится.
Теперь рассмотрим переход ненасыщенного пара в насыщенный пар, а потом в жидкость. Если ненасыщенный пар сжимать при постоянной температуре, то давление и плотность газа будут возрастать и при некотором давлении пар становится насыщенным. Дальнейшее сжатие газа будет происходить при неизменном давлении до тех пор, пока пар полностью не превратится в жидкость. Эти процессы можно изобразить диаграммой, указанной на рисунке. Участок 1-2 соответствует изотерме ненасыщенного пара, 2-3 — изотерме насыщенного пара, 3-4 — жидкости. При увеличении температуры получим ряд таких изотерм, которые изображены на втором рисунке. Они показывают, что с ростом температуры область существования насыщенного пара уменьшается и при некоторой температуре насыщенный пар не образуется. Такое состояние газа называется критическим. При температурах Т > Ткр газ в жидкость не переводится.
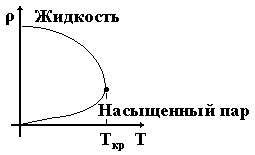 К понятию о критическом состоянии вещества можно подойти из других соображений. Если в закрытом сосуде нагревать жидкость, то плотность насыщенного пара растет, а плотность жидкости, из-за ее расширения, уменьшается. При некоторой температуре плотности пара и жидкости станут одинаковыми. Температура, при которой плотность насыщенного пара и жидкости совпадают, называется критической. В этом случае исчезает различие между жидкостью и паром. Эти процессы можно наблюдать на опыте. В специальной ампуле находится некоторое количество эфира. Между паром и жидкостью существует резкая граница. С нагревом объём жидкости увеличивается, а плотность её уменьшается. При некоторой температуре и давлении исчезает граница между жидкостью и паром. В этот момент жидкость полностью превращается в пар. При сжижении газов требуется знание критических условий.
К понятию о критическом состоянии вещества можно подойти из других соображений. Если в закрытом сосуде нагревать жидкость, то плотность насыщенного пара растет, а плотность жидкости, из-за ее расширения, уменьшается. При некоторой температуре плотности пара и жидкости станут одинаковыми. Температура, при которой плотность насыщенного пара и жидкости совпадают, называется критической. В этом случае исчезает различие между жидкостью и паром. Эти процессы можно наблюдать на опыте. В специальной ампуле находится некоторое количество эфира. Между паром и жидкостью существует резкая граница. С нагревом объём жидкости увеличивается, а плотность её уменьшается. При некоторой температуре и давлении исчезает граница между жидкостью и паром. В этот момент жидкость полностью превращается в пар. При сжижении газов требуется знание критических условий.
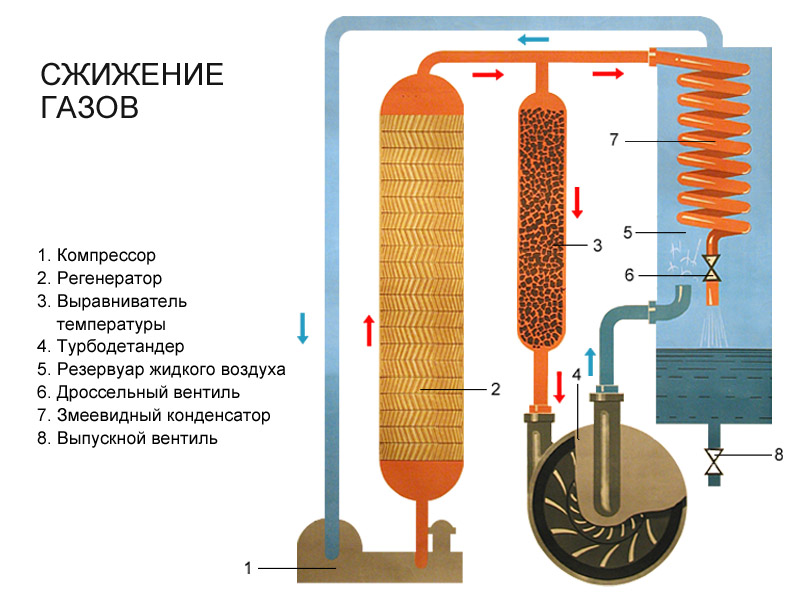
Чтобы газ превратить в жидкость путём сжатия, его предварительно необходимо охладить до критической или более низкой температуры. В настоящее время техника позволяет превращать в жидкость любые газы. Испарение может происходить не только с поверхности жидкости, но и в пузырьки воздуха, который обычно растворён в жидкости. Объём этих пузырьков невелик, но с ростом температуры испарение внутрь пузырьков увеличивается, давление насыщенного пара в них увеличивается, их объём резко возрастает. Эти пузырьки всплывают на поверхность жидкости и лопаются, выбрасывая пар в атмосферу. Процесс испарения, идущий по всему объёму жидкости, называется кипением. Вблизи поверхности жидкости давление в пузырьке чуть больше атмосферного. Температура кипения жидкости равна температуре, при которой давление насыщенного пара равно внешнему давлению.
Увеличивая внешнее давление, мы можем увеличить давление насыщенного пара, т.е. температуру кипения. Уменьшая внешнее давление можно уменьшить температуру кипения. Испарение воды с поверхности различных водоёмов приводит к тому, что в воздухе всегда присутствует пар. Количество водяных паров, содержащихся в воздухе, имеет большое значение для всего живого и растительного мира, для процессов, протекающих в атмосфере.
Для характеристики содержания водяных паров в атмосфере, т.е. влажности, вводят следующие величины:
1. Абсолютная влажность воздуха. Под абсолютной влажностью воздуха понимают количество водяного пара в 1 м3 воздуха или плотность водяного пара. Абсолютная влажность или плотность водяного пара находится р = m/V.
2. Относительная влажность воздуха. Относительная влажность воздуха определяется отношением плотности водяного пара, находящегося в воздухе, к плотности насыщенного пара при той же температуре. Она вычисляется 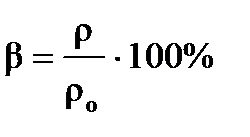 , где β — относительная влажность воздуха, ρ – плотность водяного пара при данной температуре, а ρо — плотность насыщенного пара. Относительная влажность воздуха измеряется в процентах. Плотность и давление насыщенного пара зависит от температуры воздуха. Так же используется формула
, где β — относительная влажность воздуха, ρ – плотность водяного пара при данной температуре, а ρо — плотность насыщенного пара. Относительная влажность воздуха измеряется в процентах. Плотность и давление насыщенного пара зависит от температуры воздуха. Так же используется формула 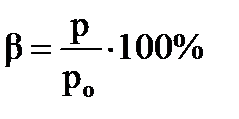 , где Р – парциальное давление водяных паров при данной температуре – упругость водяного пара, Р0 – давление насыщенного пара при данной температуре.
, где Р – парциальное давление водяных паров при данной температуре – упругость водяного пара, Р0 – давление насыщенного пара при данной температуре.
Для определения влажности воздуха используются гигрометры и психрометры. Одним из простейших приборов является гигрометр, определяющий точку росы. Если воздух охлаждать, то водяной пар при некоторой температуре становится насыщенным и происходит конденсация водяных паров (выпадает роса). Температура, при которой водяной пар достигает состояния насыщения, называется точкой росы. Если в металлическую коробочку налить быстро испаряющуюся жидкость, то при быстром испарении жидкость и коробочка будут охлаждаться. На этом основано действие гигрометра. Как только на стенках прибора появляется роса, определяется температура по термометру, помещенному в прибор, затем по таблице — абсолютная влажность.
Устройство другого, так называемого волосяного гигрометра, основано на свойстве обезжиренного волоса. Он изменяет свою длину в зависимости от влажности. Изменение длины волоса фиксируется поворотным механизмом. Шкала прибора градуируется в процентах, т.е. прибор измеряет относительную влажность.
Одним из наиболее распространенных приборов является психрометр. Прибор состоит из двух термометров, один из которых обернут кусочком ткани. Ткань опускается в сосуд с водой, поэтому термометр называют влажным. Вследствие испарения жидкости влажный термометр показывает более низкую температуру, чем сухой. Чем интенсивнее идет испарение, тем больше разность показаний термометров, а испарение зависит от влажности воздуха. Таким образом, используя разность показаний термометров и показания одного из термометров, можно определить влажность воздуха. Кроме указанных существуют другие приборы, в которых используются свойства тонких пленок и полупроводников. Влажность воздуха является важным фактором жизни человека. Влажность воздуха учитывают при хранении различных продуктов. В музеях поддерживают определённую постоянную влажность воздуха.
Вопросы:
1. Какой пар называется насыщенным?
2. Подчиняется ли ненасыщенный газ газовым законам?
3. Начертите изотерму реального газа.
4. Какая температура называется критической?
5. Как осуществляется сжижение газов?
6. Какая физическая величина называется абсолютной влажностью?
7. Какая физическая величина называется относительной влажностью?
8. Какие приборы используют для определения относительной влажности?
9. Где учитывается влажность воздуха?
ЗАДАЧИ
1. Относительная влажность воздуха в комнате равна температура воздуха 15°С. Какова упругость водяного пара (парциальное давление водяного пара)?
Мм рт. ст.
2. Над поверхностью моря при температуре 25°С относительная влажность воздуха оказалась равной 95%. При какой температуре можно ожидать появление тумана?
24°С
3. При какой температуре воздуха его относительная влажность равна 50%, если известно, что в состояние насыщения водяные пары, содержащиеся в воздухе, переходят при 7°С?
18°С
4. Относительная влажность воздуха в комнате 43%, а температура 19°С. Какую температуру показывает влажный термометр психрометра?
12°С
ДОМАШНЕЕ ЗАДАНИЕ 12
1. Температура воздуха в комнате 22°С, относительная влажность воздуха 60%. При какой температуре воздуха за окном начнут запотевать оконные стекла?
2. В комнате объемом 220 м3 при температуре 25°С относительная влажность составляет 60%. Определить массу водяных паров в воздухе комнаты. Упругость насыщенного водяного пара 1,7 кПа.
3. По гигрометру обнаружено появление росы при температуре 8°С. Какова абсолютная и относительная влажность воздуха, если его температура равна 20°С?
4. Сухой термометр психрометра показывает 50°С. По разности показаний термометров нашли, что относительная влажность равна 50%. Найти давление водяного пара в воздухе. Какова температура влажного термометра? Чему равна точка росы?
5. В комнате объемом 60 м3 температура воздуха 25°С, его относительная влажность 30%. Сколько надо испарить воды, чтобы относительная влажность достигла 60%.
1. В цилиндре под поршнем находится смесь ν молей жидкости и ν молей ее насыщенного пара при температуре Tо. К содержимому цилиндра подвели количество теплоты Q, медленно и изобарически нагревая его, и температура внутри цилиндра увеличилась на ΔТ. Найти изменение внутренней энергии содержимого цилиндра. Начальным объемом жидкости пренебречь.
∆U=Q-VRTo-2νR∆T (МФТИ)
2. Жидкость и ее насыщенный пар находятся в цилиндре под поршнем при некоторой температуре. При медленном изобарическом нагреве температура системы повысилась до 100°С, а объем увеличился на 54%. На сколько градусов нагрели содержимое цилиндра, если масса пара вначале составляла 2 /3 от полной массы смеси? Начальным объемом жидкости по сравнению с объемом системы пренебречь.
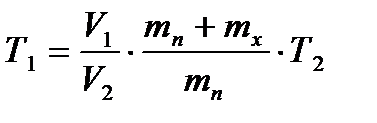 =363К
=363К
