Первое начало термодинамики
План
1. Основные термодинамические понятия: внутренняя энергия, работа, теплота. Уравнение первого начала термодинамики.
2. Применение первого начала термодинамики к изопроцессам идеального газа. Зависимость теплоёмкости идеального газа от вида процесса. Формула Майера.
3. Работа, совершаемая газом при изопроцессах.
4. Адиабатический процесс. Политропические процессы.
1. Основные термодинамические понятия
Термодинамика в отличие от молекулярно-кинетической теории не вдаётся в рассмотрение микроскопической картины явлений (оперирует с макропараметрами). Термодинамика рассматривает явления, опираясь на основные законы (начала), которые являются обобщением огромного количества опытных данных.
Внутренняя энергия – энергия физической системы, зависящая от её внутреннего состояния. Внутренняя энергия включает энергию хаотического (теплового) движения всех микрочастиц системы (молекул, атомов, ионов и т.д.) и энергию взаимодействия этих частиц. Кинетическая энергия движения системы как целого и её потенциальная энергия во внешних силовых полях во внутреннюю энергию не входит. В термодинамике и её приложениях представляет интерес не само значение внутренней энергии, а её изменение при изменении состояния системы. Внутренняя энергия – функция состояния системы.
Работа термодинамической системы над внешними телами заключается в изменении состояния этих тел и определяется количеством энергии, передаваемой системой внешним телам при изменении объема.
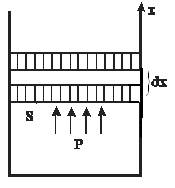 | Работа в термодинамике не является полным дифференциалом (не является функцией состояния, а зависит от пути) и обозначается 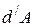 . Для того чтобы изменить объём, занимаемый газом, надо совершить работу. Представим себе газ, заключённый в цилиндрический объём с поршнем, движением которого изменяется объём газа (рис. 14.1). . Для того чтобы изменить объём, занимаемый газом, надо совершить работу. Представим себе газ, заключённый в цилиндрический объём с поршнем, движением которого изменяется объём газа (рис. 14.1). |
| Рис. 14.1 |
Сила, создаваемая давлением газа 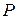 на поршень площади
на поршень площади 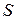 равна
равна 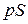 . Работа, совершаемая при перемещении поршня
. Работа, совершаемая при перемещении поршня 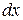 , равна
, равна 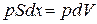 , где
, где 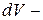 изменение объёма газа (рис. 14.1), то есть
изменение объёма газа (рис. 14.1), то есть
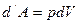 |
Теплота (количество теплоты) – количество энергии, получаемой или отдаваемой системой при теплообмене. Элементарное количество теплоты 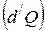 не является в общем случае дифференциалом какой-либо функции параметров состояния. Передаваемое системе количество теплоты, как и работа, зависит от того, каким способом система переходит из начального состояния в конечное. (В отличие от внутренней энергии, для которой
не является в общем случае дифференциалом какой-либо функции параметров состояния. Передаваемое системе количество теплоты, как и работа, зависит от того, каким способом система переходит из начального состояния в конечное. (В отличие от внутренней энергии, для которой 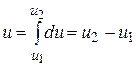 , но
, но 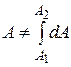 , нельзя сказать, сколько работы содержит тело, “это функция” процесса – динамическая характеристика).
, нельзя сказать, сколько работы содержит тело, “это функция” процесса – динамическая характеристика).
1-ый закон (начало) термодинамики: количество теплоты, сообщённое системе, идёт на приращение внутренней энергии системы и на совершение системой работы над внешними телами.
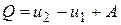 |
где 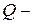 количество сообщённой телу теплоты;
количество сообщённой телу теплоты;
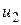 и
и 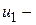 начальное и конечное значения внутренней энергии;
начальное и конечное значения внутренней энергии;
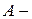 работа, совершённая системой над внешними телами.
работа, совершённая системой над внешними телами.
В дифференциальной форме 1-ое начало:
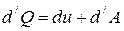 |
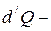 сообщённое телу элементарное количество теплоты;
сообщённое телу элементарное количество теплоты;
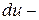 изменение внутренней энергии;
изменение внутренней энергии;
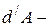 совершённая телом работа (например, работа, совершённая при расширении газа).
совершённая телом работа (например, работа, совершённая при расширении газа).
