Из двух или нескольких компонентов раствора растворителем является тот, который взят в большем количестве и имеет то же агрегатное состояние, что и раствор в целом
Вода
Вода – самое распространенное вещество на Земле. Поверхность земного шара на 3/4 покрыта водой, в довольно больших количествах вода находится в атмосфере, а также в земной коре. Основное количество воды содержится в океанах (около 97,6%), запасы же пресной воды достаточно ограничены. Около 85% всех запасов пресной воды сосредоточено в ледниках.
Вода – единственное вещество, которое встречается на Земле в трех агрегатных состояниях: твердом (лед), жидком и газообразном (водяной пар).
Необычным, или даже аномальным, свойством воды является ее способность расширяться при замерзании. Т.е. лед имеет меньшую плотность, чем жидкая вода. Поэтому он всплывает на поверхность, что очень важно для обитателей водоемов зимой.
Вода – универсальный растворитель.
При какой температуре вода должна кипеть? Вода, исходя из химического состава, – оксид водорода, но ее можно еще назвать гидридом кислорода. Если проанализировать все температуры кипения гидридов, то окажется, что вода должна кипеть при температуре ниже нуля. Вот и опять исключение из правил – вода кипит приблизительно на сто восемьдесят градусов выше, чем должна кипеть.
При какой температуре вода замерзает? Не правда ли, вопрос не менее странен, чем предыдущий? Ведь все знают, что вода замерзает при нуле градусов? А при какой температуре вода должна замерзать в соответствии со своей химической природой? Оказывается, гидрид кислорода на основании его положения в таблице Менделеева должен был бы затвердевать при ста градусах ниже нуля.
Повышение температур кипения и замерзание обусловлено взаимодействием молекул воды друг с другом, то есть водородными связями.
Если в сосуд с водой поместить кристаллы поваренной соли, сахара или перманганата калия (марганцовки), то мы можем наблюдать, как количество твердого вещества постепенно уменьшается. При этом вода, в которую были добавлены кристаллы, приобретает новые свойства: у нее появляется соленый или сладкий вкус (в случае марганцовки появляется малиновая окраска), изменяется плотность, температура замерзания и т.д. Полученные жидкости уже нельзя назвать водой, даже если они неотличимы от воды по внешнему виду (как в случае с солью и сахаром). Это – растворы.
Растворы не отстаиваются и сохраняются все время однородными. Если раствор профильтровать через самый плотный фильтр, то ни соль, ни сахар, ни марганцовокислый калий не удается отделить от воды. Следовательно, эти вещества в воде раздроблены до наиболее мелких частиц – молекул или ионов.
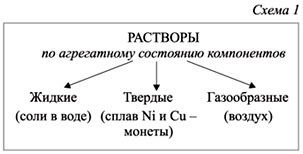 Растворами называются гомогенные (т.е. однородные) смеси переменного состава из двух или более веществ. Наиболее распространенное агрегатное состояние растворов – жидкое.
Растворами называются гомогенные (т.е. однородные) смеси переменного состава из двух или более веществ. Наиболее распространенное агрегатное состояние растворов – жидкое.
Существуют растворы не только жидкие, но и твердые. В твердых растворах частицы одного вещества хаотично распределены среди частиц какого-нибудь другого, но обязательно твердого вещества. Например, водород охотно растворяется в некоторых металлах (платине, палладии), и это пример твердого раствора. Смеси газов (например, воздух) не называют растворами. Дело в том, что важным свойством растворов является заметное взаимодействие между частицами растворителя и растворенных веществ, а в газах такое взаимодействие практически отсутствует.
Любой раствор состоит из растворителя и растворенного вещества:
Из двух или нескольких компонентов раствора растворителем является тот, который взят в большем количестве и имеет то же агрегатное состояние, что и раствор в целом.
Не всегда обязательно вода является растворителем – существуют и неводные растворы. Однако когда речь идет о водных растворах, воду считают растворителем и в тех случаях, когда ее меньше. Например, говорят о 96%-ном растворе этилового спирта в воде, а не о 4 %-ном растворе воды в спирте.
Растворение. Попадая в воду, молекулы сахара, находящиеся на поверхности кристаллов сахарного песка, образуют с молекулами воды межмолекулярные (водородные) связи. При этом с одной молекулой сахара связывается несколько молекул воды. Тепловое движение молекул воды заставляет связанные с ними молекулы сахара отрываться от кристалла и переходить в толщу 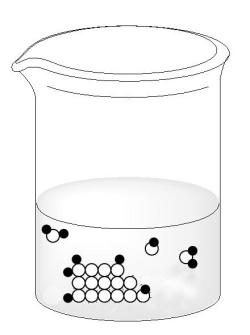 молекул растворителя (рис).
молекул растворителя (рис).
Молекулы сахара (белые кружочки), находящиеся на поверхности кристалла сахара, окружены молекулами воды (темные кружочки). Между молекулами сахара и воды возникают межмолекулярные связи, благодаря которым молекулы сахара отрываются от поверхности кристалла.
 Молекулы сахара, перешедшие из кристалла в раствор, могут передвигаться по всему объему раствора вместе с молекулами воды благодаря тепловому движению. Это явление называется диффузией. Диффузия происходит медленно, поэтому около поверхности кристаллов находится избыток уже оторванных от кристалла, но еще не диффундировавших в раствор молекул сахара. Они мешают новым молекулам воды подойти к поверхности кристалла, чтобы связаться с его молекулами водородными или другими межмолекулярными связями. Если раствор перемешивать, то диффузия происходит интенсивнее и растворение сахара идет быстрее. Молекулы сахара распределяются равномерно и раствор становится одинаково сладким по всему объему.
Молекулы сахара, перешедшие из кристалла в раствор, могут передвигаться по всему объему раствора вместе с молекулами воды благодаря тепловому движению. Это явление называется диффузией. Диффузия происходит медленно, поэтому около поверхности кристаллов находится избыток уже оторванных от кристалла, но еще не диффундировавших в раствор молекул сахара. Они мешают новым молекулам воды подойти к поверхности кристалла, чтобы связаться с его молекулами водородными или другими межмолекулярными связями. Если раствор перемешивать, то диффузия происходит интенсивнее и растворение сахара идет быстрее. Молекулы сахара распределяются равномерно и раствор становится одинаково сладким по всему объему. 
Например, при комнатной температуре мы не можем растворить в 100 мл воды более 200 г сахара или более 35,9 г поваренной соли. В таких случаях говорят, что раствор стал насыщенным.
Раствор, в котором данное вещество при данной температуре уже больше не растворяется, называется НАСЫЩЕННЫМ.
Если вернуться к примеру со школьными столами, то там тоже возможно образование "насыщенного раствора". Это может произойти в том случае, если столов окажется слишком много и для них в классах уже не будет хватать места. В этом случае часть учеников будет просто-напросто вынуждена вернуться и поставить столы в тот же штабель, откуда они были взяты. Таким образом, количество мебели в спортзале перестанет уменьшаться. Разумеется, ученики гораздо умнее молекул воды и не станут дальше делать бесполезную работу. В реальном растворе, где есть тепловое движение молекул, молекулы продолжают “трудиться”, транспортируя частицы растворенного вещества из кристалла в раствор и обратно.
Такая ситуация называется ДИНАМИЧЕСКИМ равновесием (равновесием в движении). В связи с этим можно дополнить определение насыщенного раствора:
