Материальный баланс массообменных процессов
Основы составления материальных балансов, в том числе и массообменных процессов, были рассмотрены в гл. 1. Материальные балансы конкретных массообменных процессов будут даны ниже в соответствующих главах. В этом разделе будет рассмотрен подход к составлению материальных балансов массообменных процессов с учетом их специфики.
Материальные балансы массообменных процессов зависят от способа их проведения. Различают однократное, непрерывное и ступенчатое взаимодействие фаз.
Однократное взаимодействие характерно для периодических процессов, как правило при малой производительное! и. При этом фазы смешиваются, а после завершения процесса разделяются (например, проведение периодического процесса жидкостной экстракции в аппарате с мешалкой).
Материальный баланс такою процесса в целом и по i-му компоненту имеет вид
GH + LH = GK + LK , (15.7)
GH · yiH + LH · xiH = GK · yiK + LK · xiK , (15.8)
где Сн и Gк начальное и конечное количество фазы Фу; Lн и Lк –начальной и конечное количество фазы Фх; уin и xin , уiк и xiк –начальные и конечные концентрации i-гo компонента в фазах Фу и Фх соответственно.
Если величины С и L мало изменяются с изменением состава, т. е. Gн ≈ Gк и Lн ≈Lк, то из уравнения (15.8) получаем
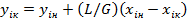 . (15.9)
. (15.9)
Уравнение (15.9) выражает составы получаемых продуктов разделения в зависимости от относительного расхода фаз L/G и является уравнением рабочей линии.
В массообменных аппаратах непрерывного действия процесс может происходить при непрерывном контакте фаз (например, в абсорбционных аппаратах пленочного типа, представляющих собой, по существу, кожухотрубчатый теплообменник, по внутренним поверхностям трубок которого течет пленка жидкости, а навстречу этой жидкости движется газ). При этом концентрации распределяемого вещества в фазах изменяются монотонно.
В массообменных аппаратах ступенчатого типа (например, в вертикальных аппаратах с горизонтальными перегородками-тарелками) в каждой ступени происходит взаимодействие фаз (см. разд. 16.53), а по выходе из ступени –их разделение. Проведение процесса при непрерывном и ступенчатом взаимодействии фаз существенно зависит от направления относительного движения фаз (прямоток, противоток и др.) и гидродинамической структуры их потоков.
При непрерывном противотоке, наиболее часто используемом в технике (рис. 15-1, а), материальный баланс для произвольного сечения аппарата при бесконечно малом пути выражается следующими соотношениями:
по всему потоку -dG = dL,
по i-му компоненту -d(Gуi) = d(Lxi).
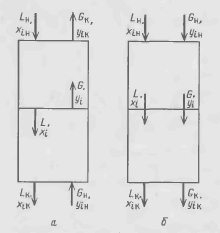
Рис. 15-1. К соединению материального баланса при непрерывном контакте фаз в условиях противотока (а) и прямотока (б)
Интегрирование в пределах от начальных значений входящих в это соотношение величин до их значений в произвольном сечении дает
Gн - Lк = Gк - Lн = G - L
и
Gнyiн - Lкxiк = Gкyiк - Lнxiн = Gyi - Lxi . (15.10)
При малом изменении величин G и L по высоте аппарата
yi = yiн + (L/G)(xi-xiк) = yiк + (L/G)(xi - xiн). (15.11)
Соотношение (15.11) называют уравнением рабочей линии непрерывного противоточного массообменного процесса. Оно выражает связь cocтавов взаимодействующих фаз в произвольном сечении аппарата. При L/G = const рабочая линия прямая. Если L/G ¹ const, то рабочая линия отклоняется от прямой.
При непрерывном прямотоке фазы движутся в одном направлении (рис. 15-1,6). На рис. 15-1,6 показано движение фаз сверху вниз, но в принципе может осуществляться и противоположное совместное их движение -снизу вверх, при котором между фазами идет процесс массопереноса. Как и в случае противотока, уравнения материального баланса имеют вид (для бесконечно малого пути)
для всего потока -dG = -dL,
для i-го компонента -d (Gуi) = -d(Lxi).
Итерирование этих уравнений в пределах изменения переменных (от начальных на входе в аппарат до конечных на выходе из него) дает уравнение материальных балансов по потокам и любому i-му компоненту:
Gк - Gн = Lн - Lк, Gнyiн = Lнxiн - Lкxiк
откуда
Gн + Lн = Gк + Lк, Gнyiн + Lнxiн = Gкyiк + Lкxiк
Для получения более общего уравнения, описывающего изменение состава фаз но высоте массообменного аппарата, проинтегрируем исходные уравнения в пределах от начальных (или конечных) значений величин, входящих в эти уравнения, до их значений в произвольном сечении (см. рис 15-1,6). Тогда получим
Gн + Lн = G + L= const, Gyi + Lxi = Gнyiн + Lнxiк = const (15.12)
Уравнения (15.12) показывают, что по высоте массообменного аппарата происходит лишь перераспределение i-го компонента между фазами, общее же количество вещества и любого i-го компонента по высоте аппарата остаются неизменными. При условии, что величины G и L мало изменяются по высоте аппарата, из уравнений (15.12) получим выражение
yi = yiн-(L/G)(xi-xiн), (15.13)
которое является уравнением рабочей линии непрерывного прямоточного массообменного процесса. Сравнение этого уравнения- с уравнением (15.11) показывает, что они аналогичны по форме, отличаясь лишь знаком перед величиной (L/G)(xi — xiн).
Отметим, что уравнения (15,11) и (15.13) получены для условий отсутствия продольного перемешивания в массообменном аппарате, т. е. для модели идеального вытеснения.
МОЛЕКУЛЯРНАЯ ДИФФУЗИЯ
Ранее отмечалось (см. гл. 3), что в потоке идут два вида массопереноса—молекулярный и конвективный.
Молекулярная диффузия описывается первым законом Фика:
dM = - DdFdτдc/дn.(15.14)
Для всей поверхности F диффузии первый закон Фика выразится как
М = -DFτдc/дn, (15.14а)
где D - коэффициент молекулярной диффузии; F-поверхность, нормальная к направлению диффузии; дс/дп-градиент концентраций вещества на единицу длины пути п диффундирующего вещества; знак минус связан с уменьшением градиента концентраций дс/дп по длине пути диффузии.
Коэффициент молекулярной диффузии D зависит от природы диффундирующего вещества. Поэтому он не связан с динамикой процесса и характеризует способность вещества проникать в какую-либо среду. Найдем его размерность из выражения (15.14a):
 ,
,
откуда следует, что коэффициент молекулярной диффузии D показывает, какое количество вещества диффундирует в единицу времени через единицу поверхности при градиенте концентрации, равном единице. Коэффициент молекулярной диффузии D является аналогом коэффициента температуропроводности а.
Значения D находят по справочникам или рассчитывают. Например,
для газов
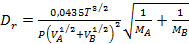 , (15.15)
, (15.15)
для жидкостей
 , (15.16)
, (15.16)
где Т -абсолютная температура, К; Р давление, Па; VA и VBмолярные объемы взаимодействующих веществ, см3 /моль; МА и МВ молярные массы, кг/кмоль; m-вязкость жидкости, в которой происходит диффузия, Па · с.
Таким образом, коэффициент диффузии зависит от температуры (увеличивается с повышением температуры) и для газов -от давления (с увеличением давления Dr снижается).
Для газовой среды Dr ≈ 1 см2/с, для конденсированной (жидкой) среды Dж ≈ 1 см2/сут, откуда следует, что молекулярная диффузия в жидкостях, а тем более в твердых телах -процесс очень медленный.
Строго говоря, движущей силой процесса молекулярной диффузии является градиент химического потенциала вещества (под химическим потенциалом, как известно, понимают частные производные характеристических функций по числам молей компонентов Ni при всех других постоянных параметрах состояния, например дH/дNi = mi = дU/дNi=дG/дNi ,где Н-энтальпия, V внутренняя энергия, G-энергия Гиббса. Но для случая переноса одного компонента mi=f(сi), где сi-концентрация i-го компонента в смеси. Тогда в качестве движущей силы можно использовать градиент концентраций, что намного упрощает расчеты. При невысоких концентрациях компонентов в реальных системах также можно использовать градиент концентраций в качестве движущей силы. Для достаточно концентрированных реальных систем при использовании в качестве движущей силы градиента концентраций следует учитывать влияние на величину коэффициента молекулярной диффузии состава системы (разделяемой смеси).
