Помните, что информация о молярных массах вещества находится в справочной таблице.
| А 1 | Уравнение Клапейрона - Менделеева |
| | 1) связывает между собой макропараметры газа 2) связывает между собой микропараметры газа 3) связывает макропараметры газа с его микропараметрами 4) не связано ни с микропараметрами, ни с макропараметрами |
| |
Масса газа
| А 2 | Кислород находится в сосуде вместимостью 0,4 м3 под давлением 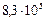 Па и при температуре 320 К. Чему равна масса кислорода? Молярная масса кислорода 0,032 кг/моль. Па и при температуре 320 К. Чему равна масса кислорода? Молярная масса кислорода 0,032 кг/моль. |
| | 1) 2 кг 2) 0,4 кг | 3) 4 кг 4) 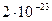 кг кг |
| А 3 | Азот массой 0,3 кг при температуре 280 К оказывает давление на стенки сосуда, равное 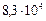 Па. Чему равен объём газа? Молярная масса азота 0,028 кг/моль. Па. Чему равен объём газа? Молярная масса азота 0,028 кг/моль. |
| | 1) 0,3 м3 | 2) 3,3 м3 |
| | 3) 0,6 м3 | 4) 60 м3 |
| А 4 | В резервуаре находится 20 кг азота при температуре 300 К и давлении 100 кПа. Чему равен объём резервуара? Молярная масса азота 0,028 кг/моль. |
| | 1) 17,8 м3 | 2) 0,018 м3 |
| | 3) 35,6 м3 | 4) 0,036 м3 |
| А 5 | В баллоне объёмом 1,66 м3 находится 2 кг азота при давлении 100 кПа. Чему равна температура этого газа? Молярная масса азота 0,028 кг/моль. |
| | 1) 280°С 2) 140°С | 3) 7°С 4) -13°С |
| А 6 | В сосуде находится жидкий азот 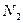 массой 10 кг. Какой объём займет этот газ при нормальных условиях (273 К; 100кПа)? Молярная масса азота 0,028 кг/моль. массой 10 кг. Какой объём займет этот газ при нормальных условиях (273 К; 100кПа)? Молярная масса азота 0,028 кг/моль. |
| | 1) 4,05 м3 2) 8,1 м3 | 3) 16,2 м3 4) 24,3 м3 |
Плотность
| А 7 | При температуре 200 К и давлении 166 кПа плотность газа 2,4 кг/м3. Молярная масса этого газа равна |
| | 1) 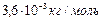 | 2) 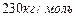 |
| | 3) 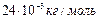 | 4) 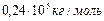 |
| А 8 | При температуре 100 К и давлении 100 кПа плотность газа равна 3,85 кг/м3. Молярная масса этого газа равна |
| | 1) 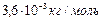 | 2) 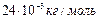 |
| | 3) 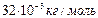 | 4) 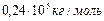 |
| А 9 | Газ при температуре 200 К и давлении 200 кПа имеет плотность 3,85 кг/ м3. Что это за газ? |
| | 1) водород 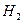 | 2) неон 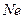 |
| | 3) кислород 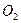 | 4) азот 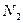 |
| В 1 | В баллоне находится 20 кг азота при температуре 300 К и давлении 100 кПа. Каков объём баллона? Молярная масса азота 0,028 кг/моль. Ответ округлите до целых. |
| В 2 | В колбе объемом 1 л находится воздух при атмосферном давлении 100 кПа и температуре 300 К. На сколько уменьшиться массы колбы с воздухом, если воздух из неё откачать. Ответ выразить в граммах и округлить до сотых. Молярная масса воздуха 0,029 кг/моль. |
| В 3 | В колбе объемом 2 л находится аргон при нормальном атмосферном давлении 100 кПа и температуре 300 К. На сколько уменьшиться масса колбы с газом, если газ из нее откачать. Ответ выразить в граммах и округлить до десятых. Молярная масса аргона 0,04 кг/моль. |
| В 4 | В колбах одинакового объема находятся аргон и воздух при нормальном атмосферном давлении и комнатной температуре. Каково отношение массы аргона в первой колбе к массе воздуха по второй? Ответ округлить до десятых. Молярная масса аргона 0,04 кг/моль, а воздуха 0,029 кг/моль. |
| В 5 | В 1 л колбу с воздухом при нормальном атмосферном давлении 100 кПа налили 1 г жидкого азота и закрыли плотной крышкой. Во сколько раз возросло давление в колбе после полного испарения азота и прогрева колбы до комнатной температуры (300 К). Ответ округлить до десятых. Молярная масса азота 0,028 кг/моль. |
Графические задачи
| В 6 | На рисунке показан график изменения давления идеального газа при его расширении. Какое количество газообразного вещества (в молях) содержится в этом сосуде, если температура газа равна 300 К? Ответ округлите до целого числа. | 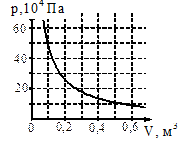 |
| В 7 | На рисунке показан график изотермического сжатия газа при температуре 150 К. Какое количество газообразного вещества (в моль) содержится в этом сосуде? Ответ округлите до целого числа. | 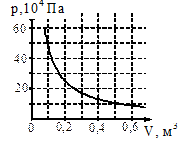 |
| В 8 | На рисунке показан график изотермического расширения водорода. Масса водорода 40 г. Определите его температуру. Молярная масса водорода 0,002 кг/моль. Ответ округлите до целого числа. | 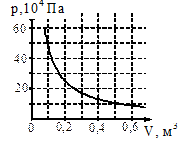 |
| В 9 | На рисунке показан график зависимости давления газа в запаянном сосуде от его температуры. Объем сосуда равен 0,4 м3. Сколько моль газа содержится в этом сосуде? Ответ округлите до целого числа. | 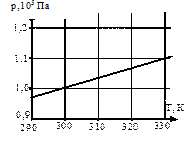 |
| В 10 | На рисунке показан график изохорного нагревания газа в сосуде объемом 10-2 м3. Какое количество газообразного вещества содержится в этом сосуде? Ответ округлите до десятых. | 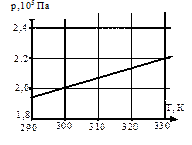 |
| С 1 | Есть фотография При исследовании уравнения состояния газа ученик соединил сосуд (1) объёмом 150 мл с манометром (2) тонкой трубкой и опустил сосуд в горячую воду. Чему равна плотность воздуха в сосуде? Начальные показания манометра равны 0 мм рт. ст. Шкала манометра и нижняя шкала барометра (3) проградуированы в мм рт. ст. Верхняя шкала барометра проградуирована в кПа. Объём измерительного механизма манометра и соединительной трубки значительно меньше 150 мл. Молярная масса воздуха 0,029 кг/моль. (на фотографии видно, что барометр показывает 746 мм рт. ст.; манометр 40 мм рт. ст.; термометр 45 °С.) |
| С 2 | Стоящий вертикально цилиндрический закрытый сосуд высотой 0,8 м разделен на две части невесомым, скользящим без трения тонким поршнем. На какой высоте установится поршень, если в верхней масти сосуда находится гелий (молярная масса 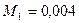 кг/моль), а в нижней – азот (молярная масса кг/моль), а в нижней – азот (молярная масса 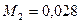 кг/моль)? Массы газов и температуры в обеих частях равны. кг/моль)? Массы газов и температуры в обеих частях равны. |
Воздухоплавание
| С 3 | Воздушный шар имеет газонепроницаемую оболочку массой 400 кг и содержит 100 кг гелия. Какой груз он может удерживать в воздухе на высоте, где температура воздуха 17°С и давление 105 Па? Молярная масса воздуха 0,029 кг/моль, а гелия 0,004 кг/моль. Считать, что оболочка шара не оказывает сопротивления изменению объема шара. |
| С 4 | Воздушный шар с газонепроницаемой оболочкой массой 400 кг заполнен гелием. На высоте, где температура воздуха 17°С и давление 105 Па, шар может удерживать груз массой 225 кг. Какова масса гелия в оболочке шара? Молярная масса воздуха 0,029 кг/моль, гелия 0,004 кг/моль. Считать, что оболочка шара не оказывает сопротивления изменению объема шара. |
Наши рекомендации
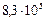 Па и при температуре 320 К. Чему равна масса кислорода? Молярная масса кислорода 0,032 кг/моль.
Па и при температуре 320 К. Чему равна масса кислорода? Молярная масса кислорода 0,032 кг/моль. 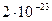 кг
кг 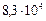 Па. Чему равен объём газа? Молярная масса азота 0,028 кг/моль.
Па. Чему равен объём газа? Молярная масса азота 0,028 кг/моль. 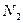 массой 10 кг. Какой объём займет этот газ при нормальных условиях (273 К; 100кПа)? Молярная масса азота 0,028 кг/моль.
массой 10 кг. Какой объём займет этот газ при нормальных условиях (273 К; 100кПа)? Молярная масса азота 0,028 кг/моль. 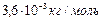
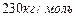
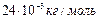
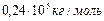
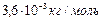
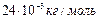
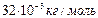
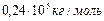
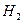
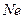
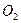
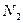
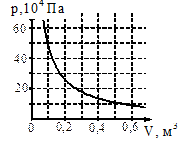
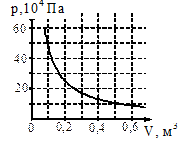
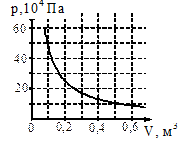
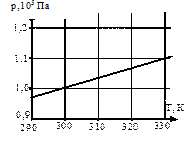
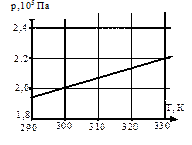
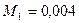 кг/моль), а в нижней – азот (молярная масса
кг/моль), а в нижней – азот (молярная масса 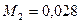 кг/моль)? Массы газов и температуры в обеих частях равны.
кг/моль)? Массы газов и температуры в обеих частях равны. 