Приведенное количество теплоты. Неравенство Клаузиуса. Энтропия и ее статистическое толкование.
Рассматривая процессы превращения тепла в работу, Р. Клаузиус сформулировал термодинамическое неравенство (неравенство Клаузиуса): «Приведенное количество тепла, полученное системой в ходе произвольного кругового процесса, не может быть больше нуля».
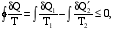
где Q – количество тепла, полученное системой при температуре Т, Q1 количество тепла, получаемое системой от участков окружающей среды с температурой Т1, Q2 – количество тепла, отдаваемое системой участкам окружающей среды при температуре Т2. Неравенство Клаузиуса позволяет установить верхний предел термического КПД при переменных температурах нагревателя и холодильника.
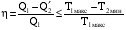 ,где Т1 макс – максимальная температура участка среды, от которого система получает тепло; Т2 мин – минимальная температура участка среды, которому система отдает тепло.
,где Т1 макс – максимальная температура участка среды, от которого система получает тепло; Т2 мин – минимальная температура участка среды, которому система отдает тепло.
Из выражения для обратимого цикла Карно следует, что
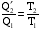 или ,
или , 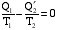
т.е. для обратимого цикла неравенство Клаузиуса переходит в равенство. Это означает, что приведенное количество тепла, полученное системой в ходе обратимого процесса, не зависит от вида процесса, а определяется только начальным и конечным состояниями системы. Поэтому приведенное количество тепла, полученное системой в ходе обратимого процесса, служит мерой изменения функции состояния системы, называемой энтропией.
Энтропия системы – функция ее состояния, определенная с точностью до произвольной постоянной. Приращение энтропии равно приведенному количеству тепла, которое нужно сообщить системе, чтобы перевести ее из начального состояния в конечное по любому обратимому процессу.
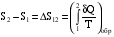 , .
, .
Энтропия впервые введена Клаузиусом в термодинамике в 1865 году для определения меры необратимого рассеивания энергии, меры отклонения реального процесса от идеального.
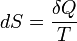
Энтропия в изопроцессах идеального газа.
Энтропия системы является функцией ее состояния, определенная с точностью до произвольной постоянной.
Найдем изменения энтропии в процессах идеального газа.
Так как при Т = const, ,
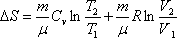 .
.
Таким образом, изменение энтропии S1-2 идеального газа при переходе его из состояния 1 в состояние 2 не зависит от вида перехода 1 - 2.
Каждый из изопроцессов идеального газа характеризуется своим изменением энтропии, а именно:
изохорический: 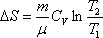 , т.к.
, т.к. 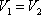 ;
;
изобарический: 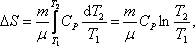 т.к. Р1 = Р2;
т.к. Р1 = Р2;
изотермический: 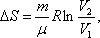 т.к.
т.к. 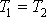 ;
;
адиабатический: 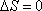 , т.к.
, т.к. 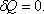
Отметим, что в последнем случае адиабатический процесс называют изоэнтропийным процессом, т.к. 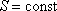 .
.
Статистический смысл энтропии. Термодинамическая вероятность.
Статистический анализ поведения системы свидетельствует о том, что вероятность состояния и энтропия ведут себя схожим образом, а именно: при переходе системы к равновесному состоянию и энтропия, и вероятность возрастают. Для установления точного соотношения между ними необходимо ввести статистическое описание системы с микроскопической и макроскопической точек зрения. Это возможно путем введения фазового пространства, в котором движутся частицы системы. Фазовое пространство – шестимерное пространство, по осям которого откладываются значения координат и проекций импульсов частиц (x, y, z, px, py, pz). Учитывая, что динамические переменные изменяются непрерывно, вести описание состояний с указанием точных значений координат и импульсов для каждой частицы невозможно. Поэтому все фазовое пространство разбивается на фазовые ячейки объемом. Теперь состояние каждой частицы может быть определено указанием того, в какой фазовой ячейке она находится. Состояние системы, заданное указанием того, какие частицы находятся в каждой фазовой ячейке, называется микросостоянием системы.
С макроскопической точки зрения состояние системы зависит от того, сколько частиц имеют то или иное значение энергии или сколько частиц находится вблизи данной точки системы, но не какие именно это частицы. Поэтому состояние системы, заданное указанием того, сколько частиц находится в каждой фазовой ячейке, называется макросостоянием системы.
При подобном описании состояния системы перемещения частиц в пределах фазовой ячейки не изменяют ни микро- ни макросостояние. Переходы частиц из одной ячейки в другую при неизменном их числе в каждой фазовой ячейке изменяют микросостояние, но оставляют прежнее макросостояние. Таким образом, одно и то же макроскопическое состояние может быть реализовано при самых различных микросостояниях. Это приводит к тому, что вероятность возникновения того или иного макросостояния системы зависит от числа микросостояний, реализующих данное макросостояние.
Количество различных микросостояний, реализующих данное макросостояние системы, называется статистическим весом или термодинамической вероятностью макросостояния.
Все микросостояния системы равновероятны, а вероятность (математическая) макросостояния определяется ее статистическим весом. Анализ значений статистических весов различных макросостояний показывает, что в равновесном состоянии статистический вес максимален. Это означает, что все макроскопические процессы обладают односторонней направленностью. Переход между двумя макроскопическими состояниями возможен только в том случае, если конечное состояние является более вероятным, чем начальное. В этом заключается механизм необратимости тепловых процессов, которая проявляется в стремлении всех макроскопических тел перейти в равновесное состояние. С другой стороны, статистика не исключает самопроизвольных переходов в неравновесные состояния, просто эти переходы маловероятны (статистические флуктуации).
Получим выражение для статистического веса макросостояния. Пусть в системе имеется N частиц, а все фазовое пространство (область возможных значений координат и импульсов) разбито на m ячеек. Рассчитаем статистический вес состояния, при котором: в 1ой ячейке находится N1 частиц; во 2ой ячейке – N2 частиц и т.д.; в mой ячейке Nm частиц. Для этого достаточно рассчитать число возможных перестановок частиц между ячейкам (они не изменяют числа частиц в ячейках). Это можно сделать, если из общего числа перестановок N частиц N! исключить перестановки в пределах каждой ячейки Ni! (они ничего не изменяют).
Если в системе создать искусственно неравновесное состояние, то в подавляющем большинстве случаев система самопроизвольно будет переходить в состояние с большей вероятностью. С другой стороны, согласно термодинамике, все самопроизвольные процессы в замкнутой системе сопровождаются возрастанием энтропии. Поэтому следует ожидать, что между энтропией системы S в каждом состоянии и вероятностью того же состояния должна существовать однозначная связь. Эта связь была установлена Больцманом (формула Больцмана):
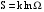 ,где k – постоянная Больцмана.
,где k – постоянная Больцмана.
Последнее соотношение можно рассматривать как определение энтропии. При таком понимании энтропии закон ее возрастания утрачивает свою абсолютность и становится статистическим законом. Энтропия замкнутой системы может не только возрастать, но и убывать. Это можно трактовать следующим образом: если система находится в неравновесном состоянии, то переход ее в более вероятное состояние будет происходить в подавляющем большинстве случаев, переходы же в менее вероятные состояния (с меньшей энтропией) настолько маловероятные, что практически не имеют никакого значения. Тогда закон возрастания энтропии оправдывается на практике с абсолютной достоверностью.
