Методичні вказівки до розрахунку
ЗАГАЛЬНІ ВКАЗІВКИ
Розрахунково-графічна робота з курсу «Технічна термодинаміка» виконується студентами спеціальності 7.090510 «Теплоенергетика».
При вивченні дисципліни позитивним моментом є придбання студентами навичок використання теоретичних основ курсу при рішенні прикладних інженерних завдань.
Систематизація і цілеспрямованість самостійної роботи сприяють підвищенню ефективності навчання, а рішення конкретних технічних завдань числовими методами допоможе не тільки засвоєнню теоретичних основ курсу, але й практичному їхньому використанню.
Основними завданнями розрахунку являються закріплення і поглиблення знань, отриманих при вивченні курсу, придбання навичок аналізу здійснюваних технічних розрахунків, розширення знань в області термодинамічних циклів теплових двигунів, а також удосконалювання вміння користуватися спеціальною технічною літературою і довідниками.
ЗМІСТ РОЗРАХУНКОВО-ГРАФІЧНОЇ РОБОТИ І ПОЯСНЮВАЛЬНОЇ ЗАПИСКИ
Розрахунково-пояснювальна записка повинна бути написана на аркушах формату А4 і містити:
а) титульний аркуш (див. додаток А);
б) реферат - короткий виклад змісту і результатів виконаної роботи;
в) зміст;
г) введення, у якому описуються цикл і термодинамічні процеси, що складають цей цикл, виконуються початковий аналіз вихідних даних і графічна ілюстрація циклу.
д) розрахункова частина, що включає до себе два основних розділа, які виконуються відповідно до завдання. У першому розділі складається послідовність термодинамічного аналізу циклу у вигляді формул (алгоритм розрахунку), із вказівкою розмірностей всіх величин і, з огляду на можливість взаємного контролю розрахунків, виконуються обчислення. У другому розділі виконується графічний розрахунок по T - S діаграмі;
е) виводи;
ж) список використаної літератури.
ТЕМАТИКА ЗАВДАННЯ
Основне призначення теплового двигуна складається в перетворенні теплоти в механічну роботу. Теплота, необхідна для перетворення в роботу, виділяється в теплових двигунах при спалюванні рідкого, твердого і газоподібного палива.
Перетворення теплоти в роботу відбувається за допомогою теплоносіїв, які можна називати робочими тілами. Як правило, робочими тілами є пари і гази, які при зміні температури і тиску можуть значно змінювати свій питомий об’єм і при цьому робити набагато більшу роботу, ніж рідкі і тверді тіла.
Принцип дії всіх теплових двигунів можна умовно розділити на наступні основні процеси: підведення теплоти до робочого тіла; перетворення теплоти в механічну енергію; відвод теплоти від робочого тіла.
Через розходження протікання зазначених процесів теплові двигуни класифікують на двигуни зовнішнього згоряння і двигуни внутрішнього згоряння. До першого класу відносять теплові двигуни, у яких продукти згоряння є тільки нагрівачем (тепловіддатчиком), а функції робочого тіла виконують рідка і парова фази (парові машини). Теплові двигуни, у яких газоподібні продукти згоряння є одночасно робочим тілом, називаються двигунами внутрішнього згоряння.
Крім того, особливостями теплового двигуна є: періодичність дії; наявність двох джерел теплоти - вищого (нагрівача) і нижчого (холодильника) і робочого тіла.
УМОВА ЗАВДАННЯ
Сухе повітря масою 1 кг робить прямий термодинамічний цикл, що складається із чотирьох послідовних термодинамічних процесів. Дані, необхідні для розрахунку залежно від варіанта, наведені в додатку Б.
Потрібно:
1. Розрахувати всі термічні параметри стану робочого тіла (p, [Па]; V, [м3/кг]; T, [К]) у характерних крапках циклу.
2. Для кожного із процесів визначити значення показників політропи n, теплоємності 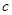 , [кДж/(кг∙ К)], обчислити зміну внутрішньої енергії
, [кДж/(кг∙ К)], обчислити зміну внутрішньої енергії 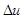 , (кДж/кг), энтальпии
, (кДж/кг), энтальпии 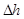 , (кДж/кг), ентропії ∆S, [кДж/(кг∙ К)], теплоту процесу
, (кДж/кг), ентропії ∆S, [кДж/(кг∙ К)], теплоту процесу 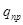 , (кДж/кг), роботу процесу
, (кДж/кг), роботу процесу 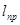 , (кДж/кг), розположену роботу
, (кДж/кг), розположену роботу 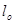 , (кДж/кг) , коефіцієнти
, (кДж/кг) , коефіцієнти 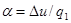 і
і 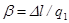 .
.
3. Визначити сумарні кількості теплоти підведеної 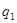 і відведеної
і відведеної 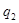 в циклі, роботу циклу lц, розположену роботу циклу lоц, термічний коефіцієнт корисної дії циклу
в циклі, роботу циклу lц, розположену роботу циклу lоц, термічний коефіцієнт корисної дії циклу 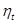 , середній індикаторний тиск pi.
, середній індикаторний тиск pi.
4 Побудувати цикл у координатах: 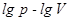 .
.
Використовуючи цю побудову, знайти координати трьох- чотирьох проміжних крапок на кожному із процесів.
Використовуючи значення проміжних крапок, побудувати цикл у координатах p- V і T- S після нанесення основних крапок циклу і складових його процесів.
5. Використовуючи p- V і T- S діаграми, графічно визначити величини , зазначені в п. 2 і п. 3, і порівняти результати графічного і аналітичного розрахунків.
6. Для процесів циклу привести схему їхнього графічного розрахунку по T- S діаграмі, зобразивши на схемі лінію процесу, допоміжні лінії ізохорного і ізобарного процесів, значення температур на початку і наприкінці процесу, відрізки, що відповідають зміні ентропії в основному і допоміжному процесах, площини, що відповідають теплоті процесу, зміні внутрішньої енергії і энтальпії, і вказати числові значення величин, взявши їх з T- S діаграми.
Для полегшення розрахунків і їхнього аналізу пропонується роботу теплових двигунів деякою мірою ідеалізувати. Ця ідеалізація зводиться до того, що в ідеальних термодинамічних циклах:
процеси протікають у всіх стадіях з постійною кількістю робочого тіла, тобто цикл є замкнутим і робоче тіло за час одного циклу повертається у вихідний стан, а не викидається в атмосферу;
процес згоряння замінюється підведенням теплоти до робочого тіла крізь стінки циліндра від деякого фіктивного гарячого джерела теплоти;
видалення робочого тіла, що відробило, не враховується і заміняється відводом теплоти від робочого тіла через стінки циліндра до так званого холодного джерела теплоти (холодильника);
теплоємності робочих тіл приймаються не залежними від температури;
робочим тілом є ідеальний газ;
механічні втрати на тертя, гідравлічні втрати відсутні.
При таких припущеннях можна вважати, що теплові машини працюють по зворотних термодинамічних циклах.
Таким чином, при розрахунках будемо вважати повітря ідеальним газом, а його властивості не залежними від температури. Приймемо газову постійну Rв рівної
287 Дж/(кг∙К).
Результати розрахунку представити у вигляді таблиць, вказавши в чисельнику значення отримані аналітично, а в знаменнику - графічно.
МЕТОДИЧНІ ВКАЗІВКИ ДО РОЗРАХУНКУ
Як приклад приведемо розрахунок циклу із заданими наступними параметрами в характерних крапках: р1 = 0,3 МПа; V1 = 0,3 м3/кг; p2 = 1,0 МПа; T3 = 473 К і наступним типом термодинамічних процесів, що складають даний цикл:
1–2 ® S = const
2–3 ® V = const
3–4 ® T = const
4–1 ® p = const
Ескіз термодинамічного циклу представлений на рис. 1.
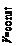
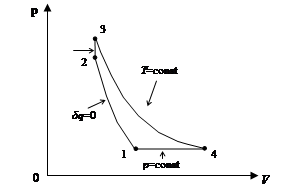 Термодинамічний цикл, що розраховується
Термодинамічний цикл, що розраховується
містить наступні процеси:
1-2 адіабатний
2-3 ізохорний
3-4 ізотермічний
4-1 ізобарний
Рис. 1 - Термодинамічний цикл
Визначимо температуру робочого тіла в крапці 1 (Т1)
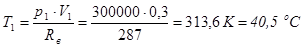
Вибираємо по додатку В теплоємність при постійному тиску 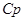 = 1,005 кДж/(кг∙ К), теплоємність при постійному об’ємі
= 1,005 кДж/(кг∙ К), теплоємність при постійному об’ємі 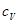 = 0,718 кДж/(кг∙ К), що відповідає властивостям сухого повітря при t1 = 40
= 0,718 кДж/(кг∙ К), що відповідає властивостям сухого повітря при t1 = 40 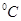 .
.
Визначимо показник адіабати 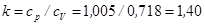 .
.
Визначимо показник політропи n і теплоємність С для кожного із процесів. Показник політропи n для процесів знайдемо з виразу
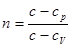 (1)
(1)
у яке замість теплоємності 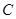 підставимо відповідні значення теплоємностей для даного процесу. Як відомо, для ізохорного процесу
підставимо відповідні значення теплоємностей для даного процесу. Як відомо, для ізохорного процесу 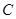 =
= 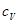 , для ізобарного
, для ізобарного 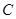 =
= 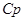 , для ізотермічного
, для ізотермічного 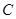 = ∞, для адіабатного
= ∞, для адіабатного 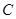 = 0. Підставивши відповідні значення
= 0. Підставивши відповідні значення 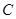 у вираження (1) і виконавши перетворення, одержимо: для ізохорного процесу
у вираження (1) і виконавши перетворення, одержимо: для ізохорного процесу 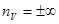 , для ізобарного
, для ізобарного 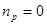 , для ізотермічного
, для ізотермічного 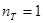 , для адіабатного
, для адіабатного 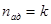 .
.
Отже, вихідними даними для розрахунку є:
р1 = 0,30 МПа; р2 = 1,0 МПа; V1 = 0,3 м3/кг; Т1 = 313,6 К; Т3 = 473 К;
RВ = 287 кДж/(кг∙ К); k = 1,40; 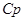 = 1,005 кДж/(кг∙ К);
= 1,005 кДж/(кг∙ К); 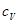 = 0,718 кДж/(кг∙ К);
= 0,718 кДж/(кг∙ К);
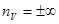 ;
; 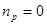 ;
; 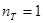 ;
; 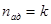 ;
; 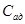 = 0; сТ = ∞
= 0; сТ = ∞
4.1. Розрахунок р, V, Т у основних крапках циклу проведемо використовуючи співвідношення, що визначають зв'язок між основними термодинамічними параметрами робочого тіла, які можна представити в такий спосіб:
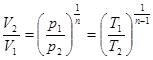 , (2)
, (2)
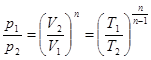 , (3)
, (3)
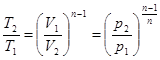 . (4)
. (4)
Крім того, для розрахунку також буде необхідно і рівняння стану ідеального газу, що має наступний вид
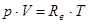 . (5)
. (5)
Отже, для т. 2 дано р2 =1,0 МПа, визначимо V2 і T2.
Для визначення V2 використаємо рівняння зв'язку параметрів в адіабатному процесі 1–2:
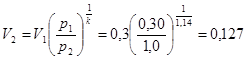 м3/кг.
м3/кг.
Для визначення T2 використаємо рівняння Клапейрона – Менделєєва
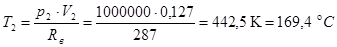
Для т. 3 дано Т3 =473 К = 200 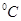 , а також V2 = V3 = 0,127 м3/кг.
, а також V2 = V3 = 0,127 м3/кг.
Визначимо р3 з рівняння співвідношення параметрів ізохорного процесу 2–3:
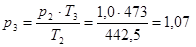 МПа.
МПа.
Для т. 4 дано р4 = р1 = 0,30 МПа, Т4 = Т3 = 473 К = 200 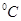 . Визначимо V4 з рівняння співвідношення параметрів ізотермічного процесу 3-4:
. Визначимо V4 з рівняння співвідношення параметрів ізотермічного процесу 3-4:
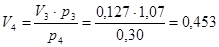 м3/кг.
м3/кг.
Результати розрахунків p, V, T, зведемо в табл. 1.
Таблиця 1 - Результати розрахунку основних параметрів
| Параметри Крапки | р, МПа | V, м3/кг | Т, К |
| 0,30/0,30 | 0,3/0,3 | 313,6/315 | |
| 1,0/1,0 | 0,127 /0,125 | 442,5/ 445 | |
| 1,07/1,07 | 0,127 0,125 | 473/475 | |
| 0,30/0,30 | 0,453 /0,455 | 473/475 |
4.2. Визначимо ∆u, ∆h, ∆S, q, l, lo, α, 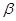 для кожного із чотирьох процесів.
для кожного із чотирьох процесів.
Всі вищевказані параметри визначимо використовуючи залежності, які представлені в Додатку Г.
Процес адіабатний 1-2
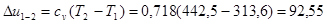 кДж/кг;
кДж/кг;
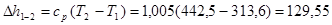 кДж/кг;
кДж/кг;
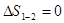 ;
;
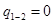 ;
;
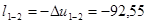 кДж/кг;
кДж/кг;
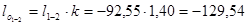 кДж/кг.
кДж/кг.
Величини α і 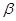 не визначаємо, тому що в адіабатному процесі теплообмін відсутній, тобто
не визначаємо, тому що в адіабатному процесі теплообмін відсутній, тобто 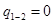
Процес ізохорний 2-3
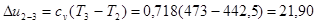 кДж/кг;
кДж/кг;
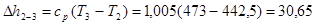 кДж/кг;
кДж/кг;
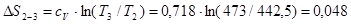 кДж/(кг∙ К)
кДж/(кг∙ К)
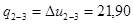 кДж/кг;
кДж/кг;
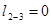 ;
;
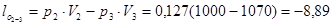 кДж/кг;
кДж/кг;
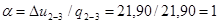 ;
;
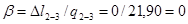 .
.
Процес ізотермічний 3-4
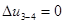 ;
;
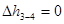 ;
;
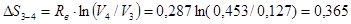 кДж/(кг∙ К);
кДж/(кг∙ К);
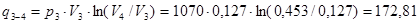 кДж/кг;
кДж/кг;
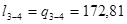 кДж/кг;
кДж/кг;
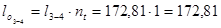 кДж/кг;
кДж/кг;
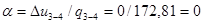 ;
;
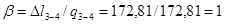 .
.
Процес ізобарний 4-1
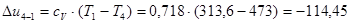 кДж/кг;
кДж/кг;
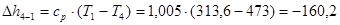 кДж/кг;
кДж/кг;
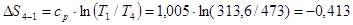 кДж/(кг∙ К);
кДж/(кг∙ К);
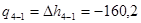 кДж/кг;
кДж/кг;
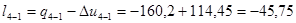 кДж/кг;
кДж/кг;
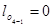 ;
;
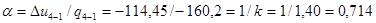 ;
;
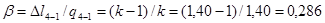 .
.
Розраховані значення n, c, ∆u, ∆h, ∆S, q, l, lo , α, 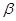 для кожного із процесів зведемо в табл. 2.
для кожного із процесів зведемо в табл. 2.
Таблиця 2. - Значення параметрів процесів циклу
| Параметри Процеси | N | с, 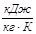 | 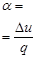 | 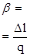 | ∆u, 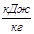 | ∆h, 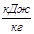 | ∆S, 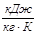 | q, 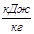 | l, 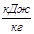 | lo, 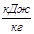 |
| 1 – 2 | 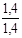 | – | – | 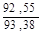 | 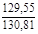 | 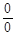 | 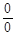 | 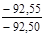 | 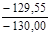 | |
| 2 – 3 | 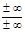 | 0,718 | 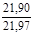 | 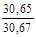 | 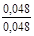 | 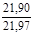 | 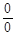 | 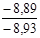 | ||
| 3 – 4 | 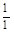 | ∞ | 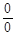 | 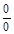 | 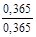 | 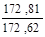 | 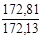 | 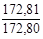 | ||
| 4 – 1 | 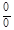 | 1,005 | 0,714 | 0,286 | 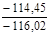 | 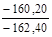 | 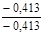 | 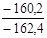 | 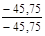 | 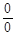 |
| СУМА | 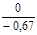 | 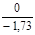 | 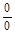 | 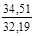 | 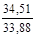 | 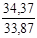 |
4.3. Визначаємо сумарну кількість підведеної q1 і відведеної q2 теплот у циклі, роботу циклу lц, розположену роботу циклу lоц , термічний к.к.д циклу 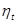 , індикаторний тиск pi.
, індикаторний тиск pi.
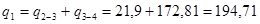 кДж/кг;
кДж/кг;
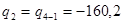 кДж/кг;
кДж/кг;
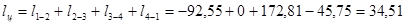 кДж/кг;
кДж/кг;
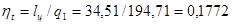 ;
;
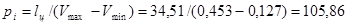 кПа.
кПа.
4.4. Будуємо цикл у координатах:
а) у координатах 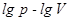 цикл представлений на рис. 2 і табл. 3.
цикл представлений на рис. 2 і табл. 3.
Таблиця 3. - Значення параметрів в основних крапках
| Крапки Параметри | ||||
| р, МПа | 0,3 | 1,0 | 1,07 | 0,3 |
| lg p | - 0,523 | 0,029 | - 0,523 | |
| V, м3/кг | 0,3 | 0,127 | 0,127 | 0,453 |
| lg V | - 0,523 | - 0,896 | - 0,896 | - 0,344 |
б) у координатах p – V цикл представлений на рис. 3 і табл. 4.
Проміжні крапки а, а', а″, а'″ для адіабати 1–2 і крапки в, в', в″, в″' для ізотерми 3–4 отримані в такий спосіб: у логарифмічних координатах адіабата 1–2 і ізотерма 3–4 являють собою прямі лінії (рис. 2), тому для цих проміжних крапок відповідні величини тисків і питомих об’ємів одержують потенцируванням їхніх значень, узятих з координат lg p і lg V.
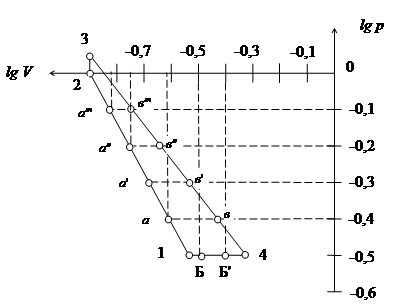 |
Рис. 2 - Цикл у координатах lg p – lg V
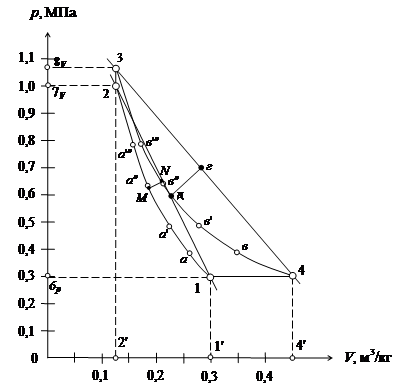
Рис. 3. – Цикл у координатах p-V
Таблиця 4 - Значення параметрів у проміжних крапках
| Крапки Параметри | а | а' | а″ | а'″ | в | в' | в″ | в″' |
| р, МПа | 0,398 | 0,501 | 0,631 | 0,794 | 0,398 | 0,501 | 0,631 | 0,794 |
| lg p | -0,4 | -0,3 | -0,2 | -0,1 | -0,4 | -0,3 | -0,2 | -0,1 |
| V, м3/кг | 0,243 | 0,207 | 0,176 | 0,148 | 0,339 | 0,269 | 0,221 | 0,170 |
| lg V | -0,615 | -0,685 | -0,755 | -0,830 | -0,470 | -0,570 | -0,665 | -0,770 |
в) у координатах T – S цикл представлений на рис. 4.
Для коректної побудови циклу в координатах T – S аналогічним образом визначаємо значення тисків і питомих об’ємів проміжних крапок Б и Б' для ізобари 4-1 (значення представлені в табл. 5), за допомогою яких визначимо температури в цих крапках і відповідні значення зміни ентропії (значення представлені в табл. 5).
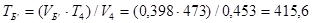 К;
К;
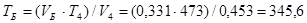 К;
К;
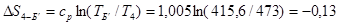 кДж/(кг∙ К);
кДж/(кг∙ К);
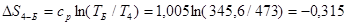 кДж/(кг∙ К).
кДж/(кг∙ К).
Таблиця 5 - Значення параметрів у проміжних крапках
| Параметри Крапки | р, Мпа | lg p | V, м3/кг | lg V | T, К | ∆S, кДж/(кг К) |
| Б | 0,30 | - 0,523 | 0,331 | - 0,48 | 345,6 | - 0,130 |
| Б' | 0,30 | - 0,523 | 0,398 | - 0,40 | 415,6 | - 0,315 |
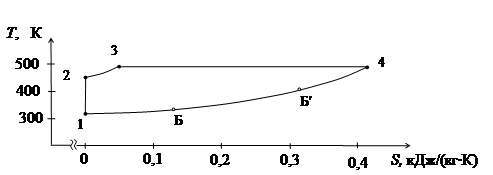
Рис. 4 – Цикл у координатах T-S
4.5 Використовуючи p- V – і T - S діаграми, графічно визначимо величини, зазначені в п. 2 і п. 3 і порівняємо результати графічного й аналітичного розрахунків:
а) Роботи розширення, стиску й розположені знайдемо по графіках процесів, представленим на рис. 3. При цьому треба мати на увазі, що знак δl визначається з вираження δl= 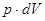 , тому що тиск p – величина позитивна, то знак δl визначається знаком dV. Якщо об’єм зменшується, то dV також має знак мінус, тобто робота відбувається над робочим тілом і δl також має знак мінус і навпаки.
, тому що тиск p – величина позитивна, то знак δl визначається знаком dV. Якщо об’єм зменшується, то dV також має знак мінус, тобто робота відбувається над робочим тілом і δl також має знак мінус і навпаки.
Процес адіабатний 1-2
Площа, обмежена процесом 2-М–1, ординатами 2–2¢ і 1–1¢, а також віссю абсцис, еквівалентна роботі стиску l1-2 . Після проведення додаткової лінії 2-N-1 на діаграмі циклу (рис. 3) ця площа може бути представлена як різниця площ прямокутної трапеції 2-N-1- 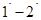 і сегменти 2-N-1-М-2. Звісно, що цілком справедливим буде наступний запис
і сегменти 2-N-1-М-2. Звісно, що цілком справедливим буде наступний запис
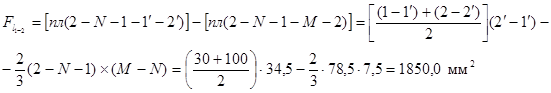
де 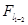 – площа на діаграмі циклу еквівалентна роботі процесу, мм2;
– площа на діаграмі циклу еквівалентна роботі процесу, мм2;
(1-1'), (2-2'), (2'-1'), (2-N-1), (M-N) – Довжини відрізків на p – V діаграмі (рис. 3) мм.
Звідки 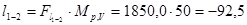 кДж/кг
кДж/кг
де Mp,v – масштаб p – V діаграми, що по рис. 3 дорівнює 50 Дж/(кг∙ мм2), тобто 1мм2= 50 Дж/кг
Знак мінус, тому що процес 1-2 це стиск, отже dV негативна.
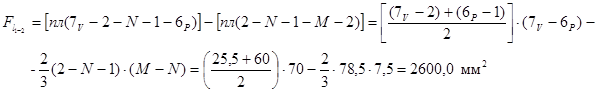
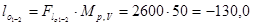 кДж/кг.
кДж/кг.
Процес ізохорний 2-3
l2-3= 0; тому що 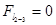
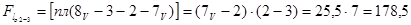 мм2;
мм2;
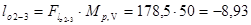 кДж/кг.
кДж/кг.
Процес ізотермічний 3-4
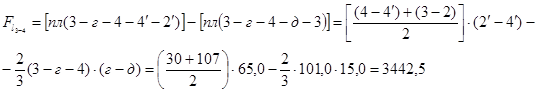
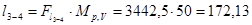 кДж/кг,
кДж/кг,
т. к. процес 3–4 – розширення, то і dV має знак плюс, отже й d l має знак плюс.
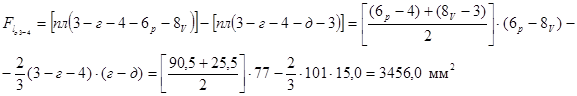
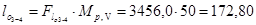 кДж/кг.
кДж/кг.
Процес ізобарний 4-1
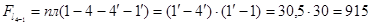 мм2;
мм2;
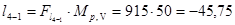 кДж/кг,
кДж/кг,
т. к. процес 4-1 – стиск, то dV має знак мінус, отже й d l має знак мінус.
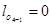 , тому що
, тому що 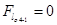 .
.
Розраховані значення l і lo графічним шляхом зведемо в табл. 2 у знаменники відповідних колонок;
б) Для кожного процесу, що становить цикл, дамо схему в T–S координатах і графічним методом визначимо Du, Dh, q, n.
При графічному дослідженні процесів в T - S діаграмі для простоти їх приймають за прямі лінії.
Крім того необхідно мати на увазі наступне:
1. Знак теплоти визначається з вираження 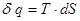 . Тому що абсолютна температура Т – величина завжди позитивна, то знак dq визначається знаком dS. Якщо dS має знак плюс і dq також буде мати знак плюс і навпаки.
. Тому що абсолютна температура Т – величина завжди позитивна, то знак dq визначається знаком dS. Якщо dS має знак плюс і dq також буде мати знак плюс і навпаки.
2. Знак Du визначається з вираження 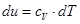 . Тому що
. Тому що 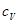 - величина позитивна, то знак Du визначається знаком dT. Температура зменшується, значить dT має знак мінус і Du також має знак мінус і навпаки.
- величина позитивна, то знак Du визначається знаком dT. Температура зменшується, значить dT має знак мінус і Du також має знак мінус і навпаки.
3. Знак ∆h визначається з вираження 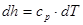 . Тому що cp – величина позитивна, то знак ∆h визначається знаком dT. Якщо температура збільшується, значить dT має знак плюс і ∆h також має знак плюс і навпаки.
. Тому що cp – величина позитивна, то знак ∆h визначається знаком dT. Якщо температура збільшується, значить dT має знак плюс і ∆h також має знак плюс і навпаки.
Процес адіабатний 1-2 (рис. 5)
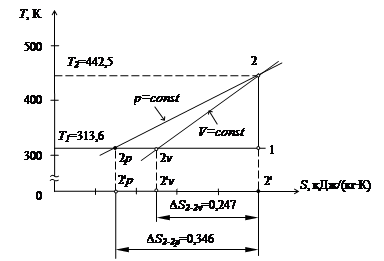
Рис. 5 – Схема розрахунку процесу 1–2 в T - S діаграмі
При визначенні Du, ∆h і n необхідно нанести додатково процеси: ізобарний і ізохорний. Для визначення зміни ентропії для ізохорного і ізобарного процесів в інтервалі зміни температур адіабатного процесу 1-2
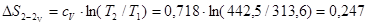 кДж/(кг∙ К)
кДж/(кг∙ К)
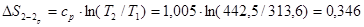 кДж/(кг∙ К)
кДж/(кг∙ К)
Як видно з рис. 5 процес 1-2 є адіабатним. Площа під изохорой 2–2V еквівалентна зміні внутрішньої енергії в процесі 1–2.
Таким чином, маємо:
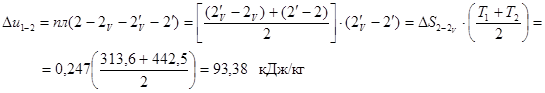
Площа під ізобарою 2-2р еквівалентна зміні энтальпии в процесі 1-2, тобто
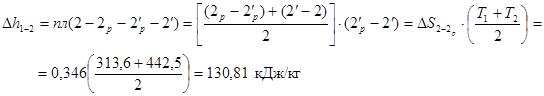
З рис. 5 слідує, що q1-2 = 0.
Показник політропи n графічно по T - S діаграмі може бути визначений у такий спосіб.
З початкової крапки процесу т. 1 (рис. 5) проводиться ізотерма, а з кінцевої т. 2 – ізобара і изохора до перетинання із проведеною ізотермою в т. 2р и т.2v Відношення відрізків 1–2р до 1–2v і дає чисельне значення. Дійсно, відрізки 1–2р і 1–2v можна розглядати, як зміна ентропії в ізотермічних процесах 1–2р і 1–2v .
Показник політропи позитивний, якщо т. 2р и т.2v розташовуються по одну сторону від т. 1. Причому, якщо т. 2р и т.2v розташовуються ліворуч від т. 1, то n>1, а якщо праворуч, то 0 < n < 1. Якщо ж т. 1 розташовується між т. 2р и т.2v , то n < 0.
Це легко одержати з вираження (1). Як відомо, теплота підведена в ізобарному процесі 2-2р може бути розрахована по формулі 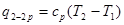 , але у свою чергу q2-2p можна виразити і як
, але у свою чергу q2-2p можна виразити і як 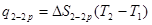 . Дорівнюючи ліві частини q2-2p цих виражень, одержимо
. Дорівнюючи ліві частини q2-2p цих виражень, одержимо 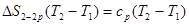 . Звідки
. Звідки 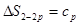 . Аналогічно одержимо співвідношення
. Аналогічно одержимо співвідношення 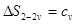 і для ізохорного процесу 2–2v .
і для ізохорного процесу 2–2v .
З огляду на, що 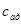 = 0, і підставивши відповідні значення
= 0, і підставивши відповідні значення 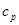 і сv у вираження (1), одержимо:
і сv у вираження (1), одержимо:
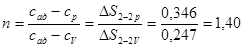 .
.
Процес ізохорний 2-3 (рис. 6).
Для ізохорного процесу 2-3, як відомо, площа під изохорой 2-3 чисельно Дорівнює теплоті процесу 2-3 і одночасно зміні внутрішньої енергії цього ж процесу.
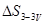 з табл. 2 дорівнює 0,048 кДж/(кг К);
з табл. 2 дорівнює 0,048 кДж/(кг К);
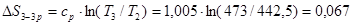 кДж/(кг∙ К)
кДж/(кг∙ К)
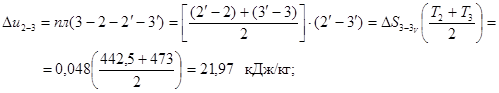
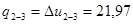 кДж/кг;
кДж/кг;
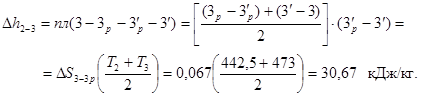
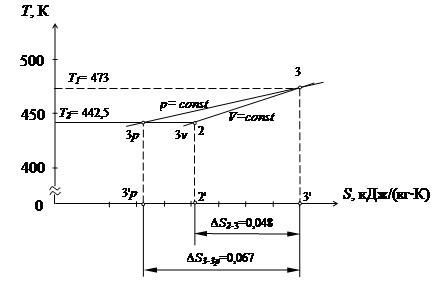
Рис. 6 – Схема розрахунку процесу 2–3 в T- S діаграмі
Показник політропи n для ізохорного процесу 2–3 визначимо в такий спосіб
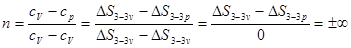 .
.
Отже, в T- S діаграмі графічне визначення показника політропи n змісту не має, тому що в знаменнику дробі нуль.
Процес ізотермічний 3-4 (рис. 7)
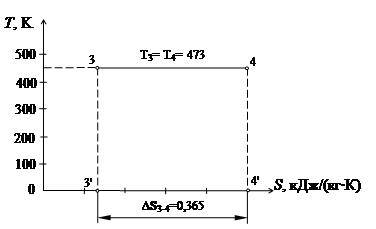
Рис. 7 – Схема розрахунку процесу 3–4 в T - S діаграмі
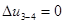 ;
;
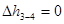 ;
;
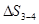 з табл. 2 дорівнює 0,365 кДж/(кг К);
з табл. 2 дорівнює 0,365 кДж/(кг К);
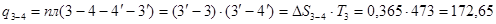 кДж/кг.
кДж/кг.
Показник політропи n для ізотермічного процесу 3–4 визначимо в такий спосіб.
Тому що Т4 = Т3 , то зміна ентропії для ізохорного і ізобарного процесів у цьому інтервалі температур буде дорівнювати нулю, (∆S4V = 0; ∆S4p = 0). Це слідує з виражень

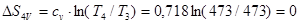 ;
;
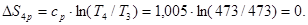
Отже, провести изохору і ізобару з т. 4 для ізотермічного процесу 3–4 не можна. Тому, підставивши відповідні значення 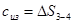 ;
; 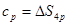 ;
; 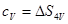 у формулу (1), маємо:
у формулу (1), маємо:
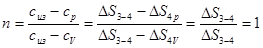 .
.
Процес ізобарний 4-1 (рис. 8)
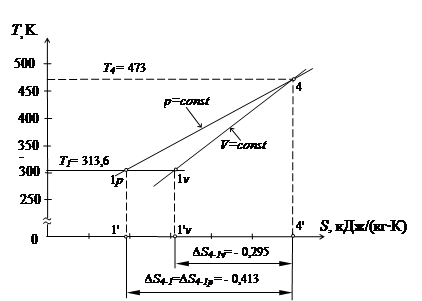
Рис.8 – Схема розрахунку процесу 4–1 в T- S діаграмі
Для ізобарного процесу як відомо, вся підведена теплота витрачається на зміну энтальпии. Отже, під ізобарою 4-1 площа 4-1-1'-4' еквівалентна теплоті процесу 4-1 і зміні энтальпии процесу 4-1
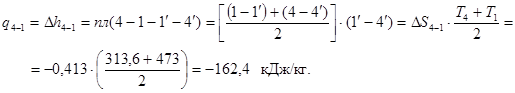
де з табл. 2 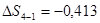 кДж/(кг∙ К).
кДж/(кг∙ К).
Під изохорой 4-1v площа еквівалентна внутрішньої енергії процесу 4-1
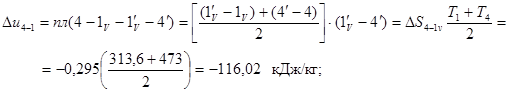
де 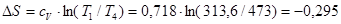 кДж/( кг∙ К).
кДж/( кг∙ К).
Показник політропи n для ізобарного процесу 4–1 знайдемо в такий спосіб:
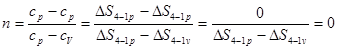 .
.
Отже, в T- S діаграмі графічне визначення показника політропи n змісту не має, тому що в чисельнику дробі 0.
Додаток А
