Завдання 3. «розрахунок константи хімічної рівноваги і рівноважного
Завдання 3. «Розрахунок константи хімічної рівноваги і рівноважного
складу газової фази»
Для заданого варіанту розрахувати 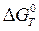 (наближеним ентропійним методом), константу рівноваги і рівноважний склад газової фази (в % об.) Зробити висновок про відновлюваність заданого оксиду газовою сумішшю СО-СО2 . Обрати склад відновної газової суміші.
(наближеним ентропійним методом), константу рівноваги і рівноважний склад газової фази (в % об.) Зробити висновок про відновлюваність заданого оксиду газовою сумішшю СО-СО2 . Обрати склад відновної газової суміші.
SnO + CO = Sn + CO2 Т = 1100 К
Завдання 4. «Термодинаміка процесів утворення –дисоціації оксидів»
Визначити нормальну хімічну спорідненість металу до кисню при утворенні відповідного оксиду для 298, 1000, 1500 та 1900 К. Розрахунок провести по рівнянню 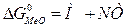 . Побудувати графік залежності
. Побудувати графік залежності 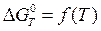 . Визначити температуру початку дисоціації оксиду в атмосфері повітря і зробити висновок про термодинамічну міцність оксиду.
. Визначити температуру початку дисоціації оксиду в атмосфері повітря і зробити висновок про термодинамічну міцність оксиду.
| № п/п | Реакция | 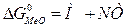 | Пределы температур, К | |
| М, Дж | N, Дж/К | |||
| 2Al + 3/2 O2 = Al2O3 | - 1 687 909 | 325,15 | 932-2303 |
Завдання 5. «Розрахунок константи рівноваги реакцій відновлення
оксидів металів газами»
Розрахувати 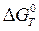 (наближеним ентропійним методом) і константу рівноваги реакції непрямого відновлення заданого оксиду для 298, 600, 1000 та 1500 К. Построїти графік залежності КР=f(T) або lgКР=f(T). Зробити висновокпро вплив температури на рівновагу реакції і можливість відновлення заданого оксиду газовою сумішшю СО-СО2 (Н2 – Н2О).
(наближеним ентропійним методом) і константу рівноваги реакції непрямого відновлення заданого оксиду для 298, 600, 1000 та 1500 К. Построїти графік залежності КР=f(T) або lgКР=f(T). Зробити висновокпро вплив температури на рівновагу реакції і можливість відновлення заданого оксиду газовою сумішшю СО-СО2 (Н2 – Н2О).
½ WO2 + CO = ½ W + CO2
Завдання 1. «Тепловий ефект хімічних реакцій»
Виразити залежність теплового ефекту реакції від температури і обчислити тепловий ефект для заданої температури, скориставшись рівнянням Кірхгофа. Порівняти тепловий ефект DН0Т з тепловим ефектом при 298 К. Оцінити відносну зміну теплового ефекту (%) реакції при переході від 298 К до Т, К.
CO + H2O = CO2 + H2 Т = 900 К
Завдання 2. «Змінення ентропії хімічних реакцій»
Обчислити значення DS0 реакції для заданої температури, інтегруючи рівняння 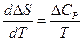 з урахуванням всіх агрегатних перетворень реагентів. Порівняти величину ентропії DS0Т з аналогічною величиною при 298 К. Оцінити в % по відношенню до DS0298 змінення ентропії при переході до Т, К.
з урахуванням всіх агрегатних перетворень реагентів. Порівняти величину ентропії DS0Т з аналогічною величиною при 298 К. Оцінити в % по відношенню до DS0298 змінення ентропії при переході до Т, К.
PbS + O2 = Pb + SO2 Т = 1200 К
Завдання 3. «Розрахунок константи хімічної рівноваги і рівноважного
складу газової фази»
Для заданого варіанту розрахувати 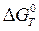 (наближеним ентропійним методом), константу рівноваги і рівноважний склад газової фази (в % об.) Зробити висновок про відновлюваність заданого оксиду газовою сумішшю СО-СО2 . Обрати склад відновної газової суміші.
(наближеним ентропійним методом), константу рівноваги і рівноважний склад газової фази (в % об.) Зробити висновок про відновлюваність заданого оксиду газовою сумішшю СО-СО2 . Обрати склад відновної газової суміші.
SnO + CO = Sn + CO2 Т = 1100 К
Завдання 4. «Термодинаміка процесів утворення –дисоціації оксидів»
Визначити нормальну хімічну спорідненість металу до кисню при утворенні відповідного оксиду для 298, 1000, 1500 та 1900 К. Розрахунок провести по рівнянню 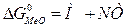 . Побудувати графік залежності
. Побудувати графік залежності 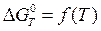 . Визначити температуру початку дисоціації оксиду в атмосфері повітря і зробити висновок про термодинамічну міцність оксиду.
. Визначити температуру початку дисоціації оксиду в атмосфері повітря і зробити висновок про термодинамічну міцність оксиду.
| № п/п | Реакция | 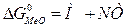 | Пределы температур, К | |
| М, Дж | N, Дж/К | |||
| 2Al + 3/2 O2 = Al2O3 | - 1 687 909 | 325,15 | 932-2303 |
