Вищі енергетичні рівні – це орбіти більш віддалені від ядра,це рівні з більшою енергією. Нижчі енергетичні рівні – це орбіти ближчі до ядра, це рівні з меншою енергією.
Будова атома. Квантові постулати Бора.
Резерфорд запропонував ядерну («планетарну») модель атома:
1) атоми будь-якого елемента складаються з позитивно зарядженої частинки, що дістала назву ядра;
2) до складу ядра входять позитивно заряджені елементарні частинки — протони (пізніше було встановлено, що й нейтральні нейтрони);
3) навколо ядра по орбітах рухаються негативно заряджені електрони (їх кількість Z), що утворюють так звану електронну оболонку.
Атом, який утратив (чи набув) один або кілька електронів, уже не буде нейтральним, а матиме позитивний (або негативний) заряд. Його називають позитивним (або негативним) іоном.
Основні дослідні факти, на які спирався Бор
· атом має планетарну структуру і разом з тим дуже стійкий (атоми можуть існувати необмежено довго, не випромінюючи електромагнітних хвиль);
· атоми випромінюють і поглинають світло квантами (фотонами), енергія яких дорівнює Е = hv;
· ізольовані атоми в збудженому стані випромінюють певний набір частот — дають лінійчаcтий спектр.
Перший постулат Бора (постулат стаціонарних станів): існують особливі стани атома з відповідними значеннями енергії перебуваючи в яких, він не випромінює і не поглинає енергії. Такі стани називають стаціонарними станами.
Цим стаціонарним станам відповідають цілком визначені (стаціонарні) орбіти, по яких рухаються електрони, які, незважаючи на наявність у них прискорення електромагнітних хвиль не випромінюють.
Кожний стаціонарний (дозволений) стан атома позначають лінією, яку називають енергетичним рівнем.Нижчий рівень називають енергетичним рівнем основного стану. Стани n>1 називають збудженими і час перебування атома у них дуже малий.
Другий постулат Бора (правило частот): при переході атома з одного стаціонарного стану в інший випромінюється або поглинається енергія.
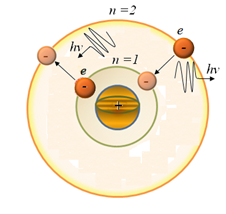 Енергія фотона дорівнює різниці енергій стаціонарних станів. Частота коливань, яка відповідає випущеному (чи поглинутому) кванту випромінювання, визначається формулою:
Енергія фотона дорівнює різниці енергій стаціонарних станів. Частота коливань, яка відповідає випущеному (чи поглинутому) кванту випромінювання, визначається формулою: 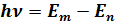
де m і п — головні квантові числа (номери його стаціонарних станів).
При Еm > Еп відбувається випромінювання фотона, а при Еm < Еп — його поглинання.
Коли електрони переходять з нижчих енергетичних рівнів на вищі, атом поглинає енергію. Коли електрони переходять з вищих енергетичних рівнів на нижчі, атом випромінює енергію.
Вищі енергетичні рівні – це орбіти більш віддалені від ядра,це рівні з більшою енергією. Нижчі енергетичні рівні – це орбіти ближчі до ядра, це рівні з меншою енергією.
Набір можливих частот квантових переходів і визначає лінійчатий спектр атома.
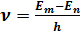
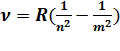 R=1,1.107м-1- стала Рідберга.
R=1,1.107м-1- стала Рідберга.
Третій постулат Бора (правило квантування орбіт): в стаціонарному стані атома електрон, рухаючись по коловій орбіті, повинен мати квантові значення моменту імпульсу, які задовольняють умову
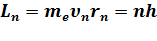
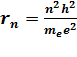
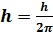 h=6,58.10-16 еВ.с h=10,551.10-35 Дж
h=6,58.10-16 еВ.с h=10,551.10-35 Дж
де me – маса електрона, 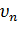 – швидкість електрона,
– швидкість електрона, 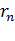 – радіус орбіти електрона, h– зведена (приведена) стала Планка
– радіус орбіти електрона, h– зведена (приведена) стала Планка
