Первое начало термодинамики - невозможен вечный двигатель первого рода, то есть двигатель, который совершал бы работу в большем количестве, чем получаемая им извне энергия
План
Внутренняя энергия.
Первое начало термодинамики.
Изопроцессы.
Работы при изопроцессах.
Адиабатический процесс.
Теплоемкость.
1. Внутренняя энергия тела.
Внутренняя энергия тела слагается из кинетической энергии поступательного и вращательного движения молекул, кинетической и потенциальной энергии колебательного движения атомов в молекулах, потенциальной энергии взаимодействия между молекулами и внутримолекулярной энергии (внутриядерной).
Кинетическая и потенциальная энергия тела как целого не входит во внутреннюю энергию.
Внутренняя энергия термодинамической системы тел слагается из внутренней энергии взаимодействия между телами и внутренней энергии каждого тела.
Работа термодинамической системы над внешними телами заключается в изменении состояния этих тел и определяется количеством энергии, которую термодинамическая система передает внешним телам.
Теплота - это количество энергии, представляемое системой внешним телам при теплообмене. Работа и теплота не являются функциями состояния системы, а функцией перехода из одного состояния в другое.
Термодинамической системой – называют такую систему, совокупность макроскопических тел, которые могут обмениваться энергией между собой и с внешней средой (с другими телами) (Например, жидкость и находящийся над ней пар). Термодинамическая система характеризуется параметрами:
P, V, T, ρ и т.д.
Состояния системы, когда хотя бы один из параметров изменяется, называется неравновесными.
Термодинамические системы, которые не обмениваются с внешними телами энергией, называются замкнутыми.
Термодинамический процесс – переход системы из одного состояния (P1,V1,T1) в другое (P2,V2,T2) – нарушение равновесия в системе.
2. Первое начало термодинамики.
Количество теплоты, сообщенное системе, идет на приращение внутренней энергии системы и на совершение системой работы над внешними телами.
Первый закон термодинамики - это специальный случай закона сохранения энергии, учитывающий внутреннюю энергию системы:
Q=U2-U1+A;
U1, U2 - начальное и конечное значения внутренней энергии тела.
A - работа, совершаемая системой.
Q - Количество теплоты, сообщаемое системе.
В дифференциальном виде:
d 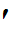 Q=dU+d
Q=dU+d 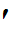 A;
A;
DU - есть полный дифференциал, и он зависит от разности начального и конечного состояния системы.
d 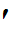 Q и d
Q и d 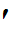 A – неполные дифференциалы, зависят от самого процесса, то есть от пути совершения процесса. Работа совершается тогда, когда изменяется объем:
A – неполные дифференциалы, зависят от самого процесса, то есть от пути совершения процесса. Работа совершается тогда, когда изменяется объем:
d 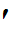 A=Fdx=pSdx =pdV;
A=Fdx=pSdx =pdV;
 | |||||
| |||||
| |||||




|
d 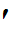 A=pdV;
A=pdV;
Первое начало термодинамики - невозможен вечный двигатель первого рода, то есть двигатель, который совершал бы работу в большем количестве, чем получаемая им извне энергия.
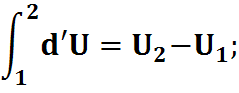
- не зависит от пути интегрирования.
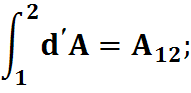
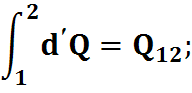
- зависит от пути интегрирования функции процесса и нельзя записать:
A2 - A1; Q2 - Q1;
