Термодинамическая система (ТС), термодинамические параметры, термодинамический процесс
ТЕХНИЧЕСКАЯ ТЕРМОДИНАМИКА
Основная цель курса – освоение студентами основных законов и методов технической термодинамики.
Данная дисциплина является одной из фундаментальных дисциплин при подготовке бакалавров по направлениям «Энергомашиностроение» и «Теплоэнергетика».
РАЗДЕЛ 1
ОСНОВНЫЕ ЗАКОНЫ ТЕХНИЧЕСКОЙ ТЕРМОДИНАМИКИ
Прежде чем приступить к конкретному рассмотрению вопросов дадим несколько определений.
ТЕРМОДИНАМИКА — раздел физики, изучающий соотношения и превращения теплоты и других форм энергии. В отдельные дисциплины выделились химическая термодинамика, изучающая физико-химические превращения, связанные с выделением или поглощением тепла, а также теплотехника и техническая термодинамика.
ТЕПЛОТЕХНИКА – это общетехническая дисциплина, изучающая методы получения, преобразования, передачи и использования теплоты, а также принципы действия и конструктивные особенности тепло- и парогенераторов, тепловых машин, аппаратов и устройств.
ТЕХНИЧЕСКАЯ ТЕРМОДИНАМИКА – это дисциплина, изучающая закономерности взаимного превращения тепловой и механической энергии и являющаяся вместе с теорией теплообмена теоретическим фундаментом теплотехники.
На основе технической термодинамики осуществляется расчет и проектирование всех тепловых двигателей – паровых и газовых турбин, реактивных и ракетных двигателей, двигателей внутреннего сгорания, а также компрессорных и холодильных машин, тепловых насосов и различного теплообменного оборудования.
ТЕМА 1
ОСНОВНЫЕ ПОНЯТИЯ И ОПРЕДЕЛЕНИЯ ТЕХНИЧЕСКОЙ ТЕРМОДИНАМИКИ
Вопрос 1
Термодинамическая система (ТС), термодинамические параметры, термодинамический процесс
Объектом изучения в термодинамике являются термодинамические системы.
ТЕРМОДИНАМИЧЕСКАЯ СИСТЕМА – это совокупность материальных тел, взаимодействующих друг с другом и с окружающей средой в виде обмена энергией и веществом.
Есть две формы передачи энергии: энергия может передаваться в виде работы и в виде теплоты.
ТС отделяют от окружающей среды контрольной поверхностью (оболочкой). Например, для газа, находящегося в цилиндре под поршнем, окружающей (внешней) средой является окружающий воздух, а контрольными поверхностями - стенки цилиндра и поршень.
Механическое и тепловое взаимодействие ТС с окружающей средой происходит через контрольные поверхности. При механическом взаимодействии самой системой или над системой совершается работа. Тепловое взаимодействие заключается в переходе теплоты между отдельными телами системы и между системой и окружающей средой. Для примера с поршнем механическая работа совершается при перемещении поршня и сопровождается изменением объема, занимаемого газом, а теплота может подводиться к газу или отводится от него через стенки цилиндра.
В самом общем случае ТС может обмениваться с окружающей средой и энергией, и веществом. Примером таких систем являются потоки газа в турбинах, компрессорах, трубопроводах. Но есть и частные случаи ТС, поэтому различают следующие ТС:
1) закрытая ТС – система, которая не обменивается с окружающей средой веществом, а обменивается только энергией;
2) открытая ТС – система, которая обменивается с окружающей средой, как веществом, так и энергией;
3) адиабатная ТС – система, которая не обменивается с окружающей средой теплотой, т.е. энергия в окружающую среду может передаваться только в виде работы;
4) изолированная ТС – система, которая не обменивается с окружающей средой ни веществом, ни энергией.
Система, имеющая во всех своих частях одинаковый состав и физические свойства, называется однородной. Однородная ТС, внутри которой нет поверхностей раздела, называется гомогенной (лед, вода, газ). Система, состоящая из нескольких макроскопических частей с различными физическими свойствами, отделенных одна от другой видимыми границами раздела, называется гетерогенной. Гомогенные части гетерогенной системы называются фазами.
Термодинамическими системами в термодинамике обычно являются рабочие тела. Рабочее тело – это газообразное, жидкое или плазменное вещество, с помощью которого происходит преобразование энергии для получения механической работы или теплоты. Рабочими телами служат воздух, водяной пар, природный газ и другие вещества.
Величины, которые определяют состояние термодинамической системы в данный момент времени, называются параметрами состояния. Различают термодинамические (термические) и калорические параметры состояния ТС.
Основными термодинамическими параметрами являются давление, температура и удельный объем.
Основными калорическими параметрами являются внутренняя энергия, энтальпия и энтропия.
Параметры, не зависящие от массы рабочего тела или числа частиц в системе, называются интенсивными параметрами состояния(например, давление, температура). Параметры, значения которых пропорциональны массе рабочего тела, называютсяэкстенсивными параметры состояния(например, внутренняя энергия, энтальпия и энтропия).
Рассмотрим поле подробно основные термодинамические параметры ТС.
Давление, р, Па. Различают абсолютное давление, атмосферное давление, избыточное давление и вакуум (разрежение).
Абсолютное давление, р – это величина, характеризующая взаимодействие молекул рабочего тела с контрольной поверхностью, численно равная силе, действующей на единицу площади поверхности тела по нормали к этой поверхности
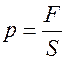 .
.
В соответствии с молекулярно-кинетической теорией давление газа определяется следующим соотношением
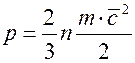
где n - число молекул в единице объема;
m - масса молекулы;
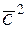 - средняя квадратичная скорость поступательного движения молекул.
- средняя квадратичная скорость поступательного движения молекул.
Атмосферное давление, ратм – это давление воздуха на поверхности земли.
Избыточное давление, ризб – это разность между абсолютным и атмосферным давлением, т. е. избыток давления над атмосферным
ризб = р - ратм.
Тогда абсолютное давление равно
р = ратм + ризб
Вакуум (разрежение) , рвак –это разность между атмосферным и абсолютным давлением, т. е. недостаток давления до атмосферного
рвак = ратм - р
Тогда абсолютное давление равно
р = ратм - рвак.
Единицы измерения давления.
В Международной Системе единиц (СИ) давление выражается в Паскалях
1 Па=1 Н/м2.
Часто применяют также 1 кПа=1000 Па и 1 МПа=106 Па.
Единицей давления в технической системе МКГСС является 1кГс/м2. В технике часто применяют также величину 1кГс/см2, называемую технической атмосферой (ат).
Давление можно измерять высотой столба h какой либо жидкости (воды, ртути и др.) с плотностью r. При этом давление в Па получается из соотношения
p=rgh,
где g- ускорение свободного падения.
Соотношения между единицами давления:
Физическая атмосфера:
1 атм = 101325 Па = 1,0332 кГс/см2 =760 мм рт. ст = 10332 мм вод. ст = 1.013 бар
Техническая атмосфера:
1 ат = 1 кгс/см2 = 98066.5 Па (≈98100 Па) = 735.6 мм рт. ст. = 104 мм вод. ст. = 0.981 бар;
Из этих соотношений следует, что
1 мм рт. ст = 133,32 Па;
1 мм вод. ст = 9,81 Па;
1 бар = 100000 Па = 750 мм рт. ст
Приборы для измерения давления.
Приборы для измерения избыточного давления называются манометрами, поэтому избыточное давление часто называют манометрическим давлением.
Приборы для измерения вакуума называются вакуумметрами, поэтому вакуум часто называют вакуумметрическим давлением.
Приборы для измерения атмосферного давления называются барометрами, поэтому атмосферное давление часто называют барометрическим давлением.
Параметром состояния ТС является абсолютное давление и именно оно используется в расчетах. Абсолютное давление обычно не измеряется, а рассчитывается через атмосферное давление и избыточное давление или вакуум.
Температура, Т, К. Температура является основной характеристикой теплового состояния ТС.
С точки зрения молекулярно-кинетической теории температура является мерой интенсивности теплового движения молекул тела и определяется средней кинетической энергией движения молекул согласно формуле
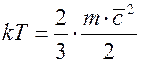
где k - постоянная Больцмана, равная 1,380662´10–23 Дж/К.
Температура, определенная таким образом, называется абсолютной или термодинамической и именно она используется в уравнениях термодинамики.
Из приведенного выражения видно, что абсолютная температура всегда положительна, а нулевое значение ее соответствует состоянию полного покоя молекул и называется абсолютным нулем температур. Шкала, в которой температура отсчитывается от этого состояния, называется термодинамической шкалой или шкалой Кельвина. Измеряемая по этой шкале температура обозначается T, а единицей измерения этой абсолютной температуры является кельвин (K).
В быту и технике принята также международная стоградусная шкала, шкала Цельсия, в которой за ноль градусов принимается температура тающего льда, а за 100 градусов – температура кипения воды при нормальном давлении 101325 Па. Измеряемая по шкале Цельсия температура обозначается t, а единицей измерения температуры является градус Цельсия (ОC).
Величина градуса, т.е. цена деления, в обеих шкалах одинакова, поэтому пересчет с одной шкалы в другую производится по формуле
Т,К = t,оС + 273,15 ≈ t,оС + 273
За рубежом, в основном, в США используется шкала Фаренгейта. Температура, определенная по этой шкале связана с температурой в градусах Цельсия зависимостью
t,°F = 1,8∙t,°С + 32
С понятием температуры связан нулевой закон (нулевое начало) термодинамики, который утверждает, что вне зависимости от начального состояния изолированной системы, в конце концов в ней установится термодинамическое равновесие, и все части системы при достижении этого равновесия будут иметь одинаковую температуру. Этот закон имеет также следующую формулировку: если две системы находятся в термодинамическом (термическом) равновесии с третьей системой, то они находятся в термодинамическом равновесии между собой; при этом температуры всех систем будут одинаковы. Тем самым этот закон фактически вводит и определяет понятие температуры.
(Слово «температура» возникло в те времена, когда люди считали, что в более нагретых телах содержится большее количество особого вещества — теплорода, чем в менее нагретых. Поэтому температура воспринималась как крепость смеси вещества тела и теплорода. По этой причине единицы измерения крепости спиртных напитков и температуры называются одинаково — градусами.)
Удельный объем, v, м3/кг– это объем единицы массы вещества, т. е. если тело массой М, занимает объем V, то
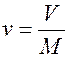 , м3/кг.
, м3/кг.
Величина, обратная удельному объему называется плотностью:
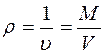 , кг/м3.
, кг/м3.
Свойства термодинамических систем часто определяют при нормальных физических условиях (н.ф.у) или нормальных технических условиях (н.т.у):
- нормальные физические условия:
р = 760 мм рт. ст. = 101 325 Па; Т = 273.15 К (t = 0 0C);
- нормальные технические условия:
р = 735.6 мм рт. ст. = 98100 Па; Т = 288.15 К (t = 15 0C).
Если все термодинамические параметры постоянны во времени и одинаковы во всех точках системы, то такое состояние системы называется равновесным, а система равновесной термодинамической системой.
Если между различными точками в системе существуют разность температур, давлений и других параметров, то она является неравновесной. В неравновесной системе под действием разности параметров возникают потоки теплоты и вещества, стремящиеся вернуть систему в состояние равновесия.
Самопроизвольное возвращение системы в состояние равновесия называется релаксацией, а промежуток времени, в течение которого система возвращается в состояние равновесия, называется временем релаксации.
Любое изменение состояния ТС во времени называется термодинамическим процессом. Термодинамические процессы могут быть равновесными и неравновесными, обратимыми и необратимыми.
Равновесный термодинамический процесс – это процесс при протекании, которого все параметры системы меняются достаточно медленно по сравнению с соответствующим процессом релаксации, то есть равновесный процесс может быть осуществлен только при бесконечно медленном изменении условий и протекает и с бесконечно малой скоростью: ΔТ, Δр, с →0. Такой равновесный процесс состоит из непрерывного ряда последовательных состояний равновесия.
Реальные процессы являются неравновесными, так как под влиянием внешних условий протекают с конечной скоростью и в рабочем теле не успевает устанавливаться равновесное состояние. Реальные процессы могут лишь в той или иной степени приближаться к равновесным процессам. В термодинамике для описания реальных процессов принимается квазиравновесная модель процесса, которая предполагает, что параметры тела постоянны по объему и равны средним их значениям; при этом дополнительно учитывается энергия диссипации в форме работы или теплоты трения. Такой подход позволяет показывать действительные процессы в термодинамических координатах.
Термодинамика в первую очередь рассматривает равновесные состояния и равновесные термодинамические процессы.
Обратимый термодинамический процесс – это процесс, при совершении которого в прямом и обратном направлениях, ТС приходит в исходное состояние и при этом не происходит никаких изменений в окружающей среде, т.е. этот процесс происходит в равновесии с окружающей средой.
Необратимым называется процесс, который нельзя провести в обратном направлении через все те же самые промежуточные состояния.
Все равновесные процессы являются обратимыми. Все неравновесные проц+ессы являются необратимыми.
Круговой процесс, осуществляемый ТС, называется циклом. Циклический характер работы имеют тепловые двигатели и холодильные установки.
Вопрос 2
