Тепловые двигатели и холодные машины
Н.Л.С. Карно (1796-1832) - французский физик, инженер, показал, что для работы теплового двигателя необходимо не менее двух источников теплоты с различными температурами, иначе это противоречило бы второму началу термодинамики.
 Второе начало термодинамики исторически возникло из анализа работы тепловых двигателей. Из формулировки второго начала термодинамики по Кельвину следует, что вечный двигатель второго рода - периодически действующий двигатель, совершающий работу за счет охлаждения одного источника теплоты, - невозможен.
Второе начало термодинамики исторически возникло из анализа работы тепловых двигателей. Из формулировки второго начала термодинамики по Кельвину следует, что вечный двигатель второго рода - периодически действующий двигатель, совершающий работу за счет охлаждения одного источника теплоты, - невозможен.
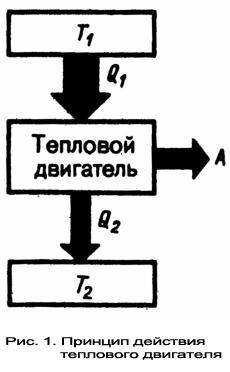
Принцип действия теплового двигателя приведём на примере (рис.1): от термостата с более высокой температурой Т1, называемого нагревателем, за цикл отнимается количество теплоты Q1, а термостату с более низкой температурой Т2, называемому холодильником, за цикл передаётся количество теплоты Q2, при этом совершается работа A = Q1 - Q2.
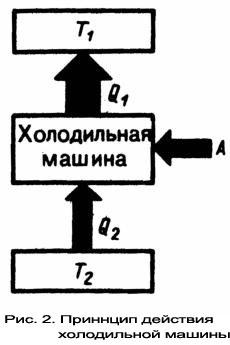
Процесс, обратный происходящему в тепловом двигателе, используется в холодильной машине, принцип действия которой представим на примере (рис.2): системой за цикл от термостата с более низкой температурой T2 отнимается количество теплоты Q2 и отдаётся термостату с более высокой температурой T1 количество теплоты Q1. Для кругового процесса Q=A, но по условию, Q=Q2-Q1<0, поэтому A<0 и Q2-Q1=-A илиQ1=Q2+A, т. е. количество теплоты Q1, отданное системой источнику теплоты при более высокой температуре T1, больше количества теплоты Q2 полученного от источника теплоты при более низкой температуре T2, на величину работы, совершенной над системой. Следовательно, без совершения работы нельзя отбирать теплоту от менее нагретого тела и отдавать её более нагретому. Это утверждение есть не что иное, как второе начало термодинамики в формулировке Клаузиуса.
 Однако вторе начало термодинамики не следует представлять так, что оно совсем запрещает переход теплоты от менее нагретого тела к более нагретому. Ведь именно такой переход осуществляется в холодильной машине. Но при этом надо помнить, что внешние силы совершают работу над системой, т. е. этот переход не является единственным результатом процесса.
Однако вторе начало термодинамики не следует представлять так, что оно совсем запрещает переход теплоты от менее нагретого тела к более нагретому. Ведь именно такой переход осуществляется в холодильной машине. Но при этом надо помнить, что внешние силы совершают работу над системой, т. е. этот переход не является единственным результатом процесса.
Основываясь на втором начале термодинамики, Карно вывел теорему, носящую теперь его имя: из всех периодически действующих тепловых машин, имеющих одинаковые температуры нагревателей (T1) и холодильников(T2), наибольшим к.п.д. обладают обратимые машины; при этом к.п.д. обратимых машин, работающих при одинаковых температурах нагревателей (T1) и холодильников (T2) равны друг другу и не зависят от природы рабочего тела (тела, совершающего круговой процесс и обменивающегося энергией с другими телами), а определяются только температурами нагревателя и холодильника.
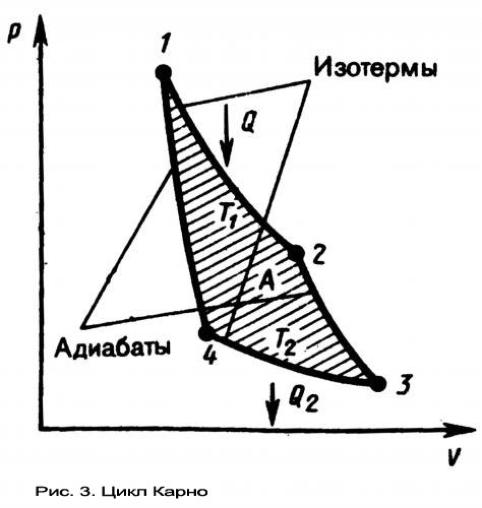
Карно теоретически проанализировал обратимый наиболее экономичный цикл, состоящий из двух изотерм и двух адиабат. Его называют циклом Карно.
Рассмотрим принцип действия изотермического и адиабатического процессов. При изобарическом расширении только часть получаемого телом тепла тратится на работу. Остальная часть переходит во внутреннюю энергию. Если работа, совершенная газом, точно равна поглощенному теплу, то внутренняя энергия газа остаётся без изменения. Температура при этом тоже не будет меняться. Такой процесс называется изотермическим.
Теплоотдача - не единственный способ увеличения внутренней энергии газа. Её можно увеличить, сжимая газ. Если такое сжатие или расширение не сопровождается передачей тепла каким-либо телам, то процесс называется адиабатным. При адиабатном процессе работа сжатия целиком переходит во внутреннюю энергию тела. Полностью устранить теплообмен газа с окружающими телами невозможно. Но можно вести сжатие в условиях, когда этим теплообменом можно пренебречь. Так, если быстро сжать газ в каком-либо объеме, то теплоотдачей через стенки объема можно пренебречь, а процесс можно считать адиабатным.
Рассмотрим прямой цикл Карно, в котором в качестве рабочего тела используется идеальный газ, заключенный в сосуд с подвижным поршнем.
Цикл Карно можно изобразить на графике (рис.3), где изотермические расширение и сжатие заданы соответственно кривыми 1-2 и 3-4, а адиабатические расширение сжатие - кривыми 2-3 и 4-1 . При изотермическом процессе U=const, поэтому количество теплоты Q1, полученное газом от нагревателя, равно работе расширения A12, совершаемой газом при переходе из состояния 1 в состояние 2:
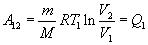 (1)
(1)
При адиабатическом расширении 2-3 теплообмен с окружающей средой отсутствует, и работа расширения A23 совершается за счет изменения внутренней энергии и:
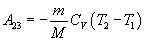 (2)
(2)
Количество теплоты Q2, отданное газом холодильнику при изотермическом, сжатии равно работе сжатия A34:
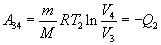 (3)
(3)
Работа адиабатического сжатия
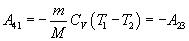 (4)
(4)
Работа, совершаемая в результате кругового процесса ,
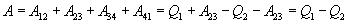 (5)
(5)
и, как можно показать определяется площадью, заштрихованной на рис.3.
Термический к.п.д. цикла Карно
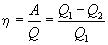 (6)
(6)
Применив уравнение для диабад 2-3 и 4-1, получим
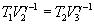
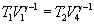
откуда
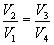 (7)
(7)
Подставляя (1) и (3) в формулу (6) получаем
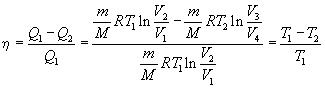
т. е. для цикла Карно к.п.д. действительно определяется только температурами нагревателя и холодильника. Для его повышения необходимо увеличивать разность температур нагревателя и холодильника. К.п.д. всякого реального теплового двигателя из-за трения и неизбежных тепловых потерь гораздо меньше вычисленного для цикла Карно.
Обратный цикл Карно положен в основу действия тепловых насосов. В отличие от холодильных машин тепловые насосы должны как можно больше тепловой энергии отдавать горячему телу, например, системе отопления. Часть этой энергии отбирается от окружающей среды с более низкой температурой, а часть - получается за счет механической работы, производимой, например, компрессором.
Теорема Карно послужила основанием для установления термодинамической шкалы температур. Для сравнения температур двух тел необходимо осуществить обратимый цикл Карно, в котором одно тело используется в качестве нагревателя, другое - холодильника. Отношение температур тел равно отношению отданного в этом цикле количества теплоты к полученному. Согласно теореме Карно химический состав рабочего тела не влияет на результаты сравнения температур, поэтому такая термодинамическая шкала не связана со свойствами какого-то определённого термодинамического тела. Отметим, что практически таким образом сравнивать температуры трудно, так как реальные термодинамические процессы, как уже указывалось, являются необратимыми.
