Основное уравнение молекулярно-кинетической теории идеальных газов
С позиций молекулярно-кинетической теории, находящийся в сосуде газ является совокупностью множества хаотически движущихся молекул. В процессе движения молекулы, ударяясь о стенки сосуда, действуют на них с некоторой силой. Отнесенная к единице площади, эта сила определяет давление газа. Итак, давление газа объясняется тепловым движением молекул и проявляется вследствие их ударов о стенки сосуда.
Рассмотрим сосуд объемом V, в котором находится N молекул, и определим давление, которое они оказывают на одну из стенок при направленном движении вдоль оси х. При каждом упругом столкновении i- ямолекула массой m0 передаст стенке импульс Δрi=2m0Vxi (рис.2.1).
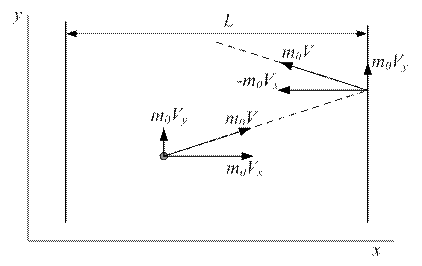
Рис.2.1
Молекула проходит расстояние L, двигаясь свободно вдоль оси х, за время L/Vx. Следовательно, за время dt молекула столкнется со стенкой Vxdt/2L раз и передаст ей импульс, 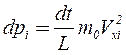 а все N молекул
а все N молекул
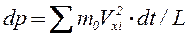
По второму закону Ньютона dp/dt = F. В нашем случае сила, с которой молекулы действуют на стенку, равна
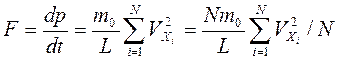
Введем обозначение
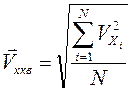 ,
,
называемоесредней квадратичной скоростью молекул в заданном направлении. Тогда
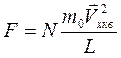 ,
,
или, разделив на площадь стенки S, найдем давление N молекул на стенку
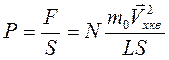
Произведение LS=V есть объем сосуда. Тогда
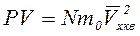 (2.2)
(2.2)
Так как в сосуде молекулы одинаково движутся по всем осям координат, то
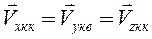 .
.
Поэтому
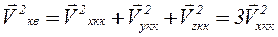
откуда:

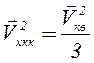
 Подставив величину
Подставив величину 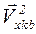 в уравнение (2.2), найдем:
в уравнение (2.2), найдем:

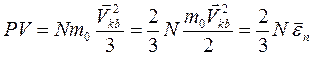
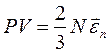 (2.3)
(2.3)
 где
где
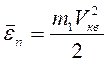 (2.4)
(2.4)
выражает среднюю кинетическую энергию поступательного движения молекулы.
 Сравнивая уравнение (2.3) с уравнением Менделеева - Клапейрона (2.1), получим
Сравнивая уравнение (2.3) с уравнением Менделеева - Клапейрона (2.1), получим
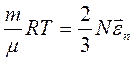 (2.5)
(2.5)
 Предположим, что в сосуде находится 1 моль идеального газа. Тогда
Предположим, что в сосуде находится 1 моль идеального газа. Тогда 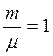 , число молекул N равно числу Авогадро NА и уравнение (2.5) для 1 моля газа примет вид
, число молекул N равно числу Авогадро NА и уравнение (2.5) для 1 моля газа примет вид
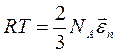 ,
,
откуда
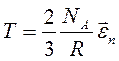 , (2.6)
, (2.6)
т.е. абсолютная температура Т газа пропорциональна средней кинетической энергии 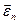 поступательного движения его молекул. Обозначив R/NA = k, которая является постоянной Больцмана k = 1,38 · 10-23 Дж/К, получим
поступательного движения его молекул. Обозначив R/NA = k, которая является постоянной Больцмана k = 1,38 · 10-23 Дж/К, получим
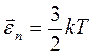 (2.7)
(2.7)
Подставляя формулу (2.7) в (2.3) найдем
PV = NkT
или
P = n0 kT, (2.8)
где 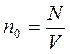 - число молекул в единице объема или их концентрация.
- число молекул в единице объема или их концентрация.
