Постулаты феноменологической термодинамики
II. Статистическая термодинамика.
Основные понятия
Квазистатический процесс; нулевой постулат феноменологической термодинамики; первый постулат феноменологической термодинамики; второй постулат феноменологической термодинамики; третий постулат феноменологической термодинамики; понятие внутренней энергии; функция состояния; функция процесса; основное термодинамическое равенство; понятие энтропии для изолированной неравновесной системы; понятие локальной неустойчивости фазовых траекторий (траекторий частиц); системы с перемешиванием; обратимый процесс; необратимый процесс; термодинамический потенциал; свободная энергия Гельмгольца; свободная энергия Гиббса; соотношения Максвелла; обобщённые координаты и обобщённые силы; принципы экстремума в термодинамике; принцип Ле-Шателье-Брауна.
Основные знания.
Статистическая интерпретация понятий: внутренняя энергия, работа подсистемы, количество теплоты; обоснование первого начала термодинамики с помощью канонического распределения Гиббса; статистическое обоснование третьего термодинамики; свойства макросистем при  ; физический смысл энтропии; условия устойчивости термодинамической системы.
; физический смысл энтропии; условия устойчивости термодинамической системы.
Основные умения.
Самостоятельно работать с рекомендованной литературой; определять понятия из п.1; уметь логично обосновывать с использованием математического аппарата элементы знаний из п.2; по известной статистической сумме (статистическому интегралу) определять внутреннюю энергию системы, свободную энергию Гельмгольца, свободную энергию Гиббса, энтропию, уравнение состояния и т.п.; определять направление эволюции открытой системы при постоянных 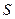 и
и 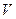 , постоянных
, постоянных 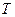 и
и 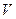 , постоянных
, постоянных 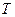 и
и 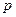 .
.
Постулаты феноменологической термодинамики.
Эти постулаты являются обобщением огромного числа наблюдений над термодинамическими системами.
а) Нулевое начало термодинамики.
При фиксированных внешних условиях термодинамическая система переходит в состояние термодинамического равновесия. (Фактически нулевое начало термодинамики постулирует существование температуры. Состояние термодинамического равновесия – такое состояние, при котором макроскопические параметры системы не изменяются с течением времени и в системе отсутствуют потоки любого типа.)
б) Первое начало термодинамики. (Закон сохранения и превращения энергии.)
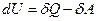 (2.1.1)
(2.1.1)
Бесконечно малое изменение внутренней энергии dU происходит за счёт того, что система поглощает количества тепла  и совершает работу
и совершает работу 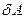 . (Если система совершает работу, то
. (Если система совершает работу, то 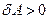 , если над системой совершается работа, то
, если над системой совершается работа, то 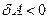 . Если система получает количество тепла, то
. Если система получает количество тепла, то  , если отдаёт, то
, если отдаёт, то  .) Первое начало термодинамики вводит в физику новую физическую величину – внутреннюю энергию.
.) Первое начало термодинамики вводит в физику новую физическую величину – внутреннюю энергию.
в) Второе начало термодинамики.
Постулат состоит из двух частей.
1. Для любой равновесной (то есть участвующей в квазистатическом процессе) термодинамической системы существует однозначная функция состояния S, называемая энтропией, её полный дифференциал  .
.
2. Для всякого неравновесного (неквазистатического) процесса, происходящего в термодинамической системе: 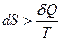 , где
, где  – количество поглощённой системой тепла в этом процессе.
– количество поглощённой системой тепла в этом процессе.
Второе начало имеет несколько различных, но эквивалентных формулировок. Приведём ещё некоторые из них:
1. Невозможно построить периодически действующую машину, которая совершала бы работу за счёт охлаждения некоторого источника тепла без каких-либо иных изменений в природе. (Томсон)
2. Тепло не может самопроизвольно (то есть без компенсации) переходить от тела менее нагретого к более нагретому. (Клаузиус)
3. Невозможно построить вечный двигатель второго рода. (Освальд)
в) Третье начало термодинамики.
Приведём две формулировки:
1. Термодинамический процесс, протекающий при температуре Т, сколь угодно близкой к абсолютному нулю, не сопровождается изменением энтропии S.
2. При  энтропия системы также стремится к нулю.
энтропия системы также стремится к нулю.
Следует иметь в виду, что в термодинамических системах силы взаимодействия между частицами либо короткодействующие, либо электромагнитные, которые могут экранироваться частицами противоположного знака. Системы для которых существенно гравитационное (неэкранируемое) взаимодействие, являются нетермодинамическими. В качестве примера рассмотрим мысленный эксперимент, предложенный астрофизиком Нарликаром.
Звёзды находятся в равновесии под действием двух сил: гравитационного сжатия и внутреннего давления, производимого направленным изнутри излучением и потоками нейтрино. Это давление зависит от температуры.
Поместим в окрестность холодной звезды горячую. Поток тепла от неё устремится к холодной. Внутреннее давление холодной звезды, получающей энергию, возрастает. Она расширяется и температура её понижается. Поскольку горячая звезда отдаёт энергию, внутреннее давление у неё уменьшается. Это приводит к её гравитационному сжатию и повышению температуры. Таким образом температура горячей звезды ещё больше повышается, холодной – понижается, что противоречит второму началу термодинамики.
Далее с помощью статистической физики, обоснуем законы термодинамики с точки зрения атомно-молекулярных представлений и выясним смысл введённых термодинамических параметров.
