Метод вимірювання і опис установки
На рис.4зображена установка визначення коефіцієнта Пуассона  .При закритому крані А повітря в сифоні займає його об'єм V при атмосферному тиску Н. За допомогою компресора нагнітають деяку кількість повітря у сифон. Тиску сифоні підвищується, збільшується його температура. Відкривають кран А, при цьому рідина у манометрі змінює свій рівень. Після закриття крану А знаходять різницю рівнів рідиниh в манометрі. Відкривши кран А, випускають частину повітря поки тиск в сифоні не зрівняється з атмосферним, після чого кран закривають. Так як вирівнювання тиску проходить досить швидко, теплообміном з навколишнім середовищем можливо знехтувати і рахувати процес адіабатичним.
.При закритому крані А повітря в сифоні займає його об'єм V при атмосферному тиску Н. За допомогою компресора нагнітають деяку кількість повітря у сифон. Тиску сифоні підвищується, збільшується його температура. Відкривають кран А, при цьому рідина у манометрі змінює свій рівень. Після закриття крану А знаходять різницю рівнів рідиниh в манометрі. Відкривши кран А, випускають частину повітря поки тиск в сифоні не зрівняється з атмосферним, після чого кран закривають. Так як вирівнювання тиску проходить досить швидко, теплообміном з навколишнім середовищем можливо знехтувати і рахувати процес адіабатичним.
Газ масою mт, що залишився в сифоні, займає об'єм сифона V2 при атмосферному тиску Н і температурі 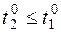
До відкриття крану А в сифоні знаходилось більше повітря, тому повітря масою m займало об'єм V1 < V2 при тиску Н+h, і кімнатній температурі t1.
Параметри газу масою m до відкриття крану А зв'язані з параметрами газу при відкритому крані А рівнянням Пуассона
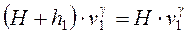 (8)
(8)
Після деякого часу температура повітря в сифоні внаслідок теплообміну знову стане рівною t1 і тиск з підвищенням температури зросте до H+h2 - різниця рівнів в манометрі. По закону Бойля – Маріота (t1=t2)
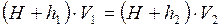 (9)
(9)
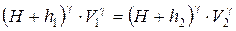 (10)
(10)
Поділимо почленно (10) на (9)
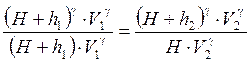
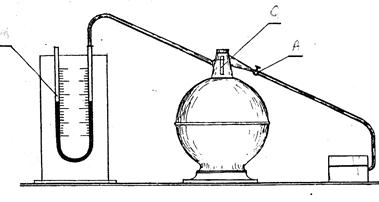
Рис.4 Установка для визначення відношення 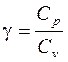
Прологарифмуємо обидві частини одержаного рівняння
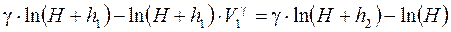 (11)
(11)
Якщо тиски Н, Н + h1 i H+h2 ненабагато відрізняються один від одного, то різниці їх логарифмів приблизно пропорційні різницям тисків
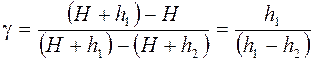 (12)
(12)
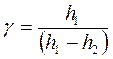 (13)
(13)
Хід роботи
1. Для подачі повітря у сифон необхідно включити компресор і через деякий час, приблизно через 20 с, відкрити клапан, натиснувши ручку сифона.
2. Зафіксувати різницю рівнів рідини в манометрі відпустивши ручку сифона і зняти покази h1 яке відповідає цій різниці.
3. Для сполучення сифона з атмосферою необхідно роз'єднавши трубку яка підведена до компресора, натиснути на ручку сифона на 1-2 секунди і знову відпустити.
4. Під'єднати трубку до сифона і після встановлення рівня рідини в манометрі, зняти показники h2 яке відповідає цій різниці.
5. Дослід-повторити 3 рази. Дані внести до таблиці:
Таблиця
| Nп/п | h1 | h2 | 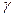 | 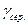 | 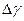 | 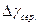 |
6. Значення 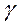 знаходиться за формулою (13) для кожного досліду окремо.
знаходиться за формулою (13) для кожного досліду окремо.
7. Знайти похибку для кожного досліду, кінцевий результат записати у вигляді: 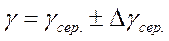
КОНТРОЛЬНІ ПИТАННЯ.
1. Який газ називається ідеальним? При яких умовах реальний газ можна вважати ідеальним?
2. Записати і пояснити рівняння Менделєєва – Клапейрона.
3. Який фізичний зміст універсальної газової сталої?
4. Який процес називається адіабатичним? Який вид має рівняння Пуассона?
5. Який процес називається ізобарним, ізохорним, ізотермічним? Рівняння що їх характеризують.
6. Що називається молярною теплоємністю газу?
7. Записати формулу Майера. Пояснити, чому Ср > Сv ?
8. Пояснити фізичний зміст методу адіабатичного розширення?
Тестові питання для захисту лабораторної роботи:
1. Формула Майера:
а) 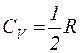 ;
;
б) 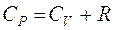 ;
;
в) 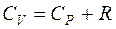 .
.
2. Рівняння Клапейрона-Менделєєва:
а) 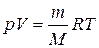 ;
;
б) 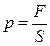 ;
;
в) 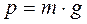 ;
;
3. Основне рівняння МКТ ідеального газу:
а) 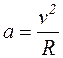 ;
;
б) 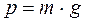 ;
;
в) 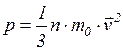 ;
;
4. Внутрішня енергія ідеального газу:
а) 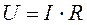 ;
;
б) 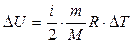 ;
;
в) 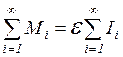 .
.
5. Рівняння Больцмана:
а) 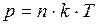 ;
;
б) 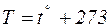 ;
;
в) 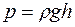 ;
;
6. Характеристики ізохорного процесу:
а) 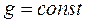 ;
; 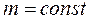 ;
; 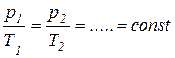 ;
;
б) 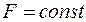 ;
; 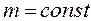 ;
; 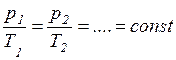 ;
;
в) V= const; 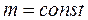 ;
; 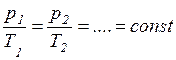 ;
;
7. Характеристики ізобарного процесу:
а) 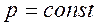 ;
; 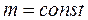 ;
; 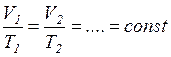 ;
;
б) 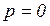 ;
; 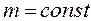 ;
; 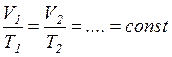 ;
;
в) 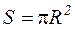 ;
; 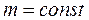 ;
; 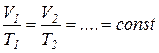 ;
;
8. Характеристики ізотермічного процесу:
а) 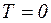 ;
; 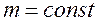 ; p1V1=p2V2=…=const;
; p1V1=p2V2=…=const;
б) 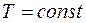 ;
; 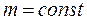 ; p1V1=p2V2=…=const;
; p1V1=p2V2=…=const;
в) 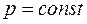 ;
; 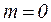 ; p1V1=p2V2=…=const;
; p1V1=p2V2=…=const;
9. Що називається ідеальним газом?
а) газ, в якому молекули не рухаються, Ер= 0;
б) газ при високих температурах і високому тиску;
в) газ , в якому взаємодією між молекулами нехтують, Ер= 0;
10.Який процес називається адіабатичним?
а) процес, що відбувається при постійній температурі;
б) процес, що відбувається при постійному тиску;
в) процес, що відбувається без теплообміну між газом і навколишнім середовищем.
11. Що називається теплоємністю газу?
а) кількість теплоти , що необхідна для нагрівання одного моля газу на один Кельвін;
б) кількість теплоти, що необхідна для нагрівання одиниці маси речовини на один Кельвін;
в) кількість теплоти , яка передана тілу.
ЛАБОРАТОРНА РОБОТА N 12
