Тема 2. Перший закон термодинаміки
МІНІСТЕРСТВО ОСВІТИ, НАУКИ, МОЛОДІ ТА СПОРТУ УКРАЇНИ
ДНІПРОДЗЕРЖИНСЬКИЙ ДЕРЖАВНИЙ ТЕХНІЧНИЙ УНІВЕРСИТЕТ
О.І.Полянчиков
КОНСПЕКТ ЛЕКЦІЙ
з дисципліни
«Фізична хімія »
для студентів напрямків
6.050802 „Електронні пристрої та системи” (ЕС),
6.050801 “Мікро та наноелектроніка” (ФБЕ).
Затверджено науково-методичною
радою ДДТУ „___”______2013 р.
протокол № ___
Дніпродзержинськ
Тема 1. Вступ до фізичної хімії. Будова речовини.
Історія розвитку фізичної хімії. Предмет і зміст фізичної хімії. Основні розділи фізичної хімії. Методи фізичної хімії – квантово-механічний, термодинамічний, метод статистичної механіки. Основи теорії будови речовини і тіла.
Хімічні реакції завжди пов'язані з різноманітними фізичними процесами: виділенням або поглинанням тепла, випромінюванням або поглинанням електромагнітних коливань, виникненням електричного струму при перебігу реакції в гальванічному елементі, перебігом хімічних реакцій при проходженні струму і т. д. Цей зв'язок між фізикою і хімією відзначав вже Ломоносов, який писав: «Хімік без знання фізики подібний людині, яка усього повинна шукати помацки. І ці дві науки так єдині між собою, що одна без іншої досконалими бути не можуть». Ломоносов назвав фізичною хімією науку, «що пояснює на основі дослідів фізичних причину того, що відбувається через хімічні процеси в складних тілах».
Однак лише більше як за століття після Ломоносова ідея про плідність злиття фізики і хімії в особливій науці — фізичній хімії — отримала глибоке визнання в працях багатьох видатних вчених.
У 1863 р. М. М. Бекетов організував у Харківському університеті відділення фізичної хімії і почав читати студентам курс лекцій з цієї дисципліни, визначивши її як науку, яка займається «співвідношенням фізичних і хімічних властивостей... Хоча ми і розрізнюємо фізичні і хімічні властивості тіл, проте і ті і інші суть вираження будови і властивостей найдрібніших частинок... У природі ці дві умови існування матерії, звичайно, не розділені».
У другій половині XIX ст. нова наука стала бурхливо розвиватися завдяки трудам блискучої плеяди хіміків (Оствальд, Вант-Гофф, Бекетов, Менделєєв, Арреніус, Коновалов, Рауль, Фарадей, Гіббс, Нернст і багато інших). Швидкий розвиток і зростаюче значення фізичної хімії пов'язані з її пограничним положенням між фізикою і хімією. Фізична хімія як суміжна наука охоплює явища, що вивчаються нею з різних боків, і таким шляхом пізнає складні і взаємопов'язані явища матеріального світу.
Фізична хімія приділяє головну увагу дослідженню законів перебігу хімічних процесів у часі і законів хімічної рівноваги. Основна загальна задача фізичної хімії — прогноз часового ходу хімічного процесу і кінцевого стану (стану рівноваги) в різних умовах на основі даних про будову і властивості молекул речовин, які складають систему, що вивчається.
Велике і постійно зростаюче значення мають фізико-хімічні дослідження в розвитку хімічної промисловості і багатьох інших галузей (основний органічний і неорганічний синтез, нафтохімія, виробництво пластмас і хімічного волокна, напівпровідників, розробка хімічних джерел струму і так далі), сільського господарства, біології і медицини тощо. Різноманітність об'єктів і явищ, що вивчаються фізичною хімією, складність зв'язків між властивостями речовин і характером процесів, які спостерігаються, привели до розподілу фізичної хімії на окремі основні розділи. Природно, що такий розподіл досить умовний, оскільки неможливо провести чіткі межі між різними розділами, але в той же час він є корисним і полегшує систематичне вивчення фізичної хімії.
Нижче коротко розглянемо ці основні розділи.
Будова речовини. Цей розділ включає в себе вчення про будову атомів, будову молекул і про агрегатні стани речовин.
Хімічна термодинаміка. У цьому розділі на основі законів загальної термодинаміки розглядаються закони хімічної рівноваги і вчення про фазову рівновагу, а також енергетику хімічних процесів.
Вчення про розчини. Метою цього розділу є пояснення і прогноз властивостей розчинів на основі властивостей речовин, що складають розчин.
Електрохімія. Вивчається взаємодія електричних явищ і хімічних реакцій (електроліз, хімічні джерела електричного струму). В електрохімію також звичайно включають вчення про властивості розчинів електролітів, іонні рівноваги, електричну провідність розчинів електролітів, корозію металів.
Хімічна кінетика і каталіз. У цьому розділі розглядається швидкість хімічних реакцій, її залежність від зовнішніх умов, зв'язок швидкості реакції з будовою і енергетичним станом реагуючих молекул, вплив каталізатора на швидкість.
Вчення про поверхневі явища. Розглядаються питання термодинаміки поверхневого шару і адсорбції. Більш детально поверхневі явища вивчаються в курсі колоїдної хімії.
В фізичній хімії використовують три метода. Перший з них – квантово-механічний, який покладено у основу вчення щодо будови окремих атомів і молекул і взаємодії між ними.
Другий метод – термодинамічний, дозволяє відповісти на питання – буде перебігати хімічна реакція в визначеному напрямку, якщо відомий початковий стан системи(наприклад Т, С) і коли настане хімічна рівновага( при яких кінцевих для даних умов концентраціях реагуючих речовин).
Третій метод – метод статистичної механіки, заснований на вчені молекулярної природи речовини.
Уся сукупність даних і теоретичних методів використовується для досягнення основної мети — з'ясування залежності напряму, швидкості і межі перебігу хімічних перетворень від зовнішніх умов і від будови молекул речовин, які беруть участь у реакції.
Питання, які розглядаються у розділі будови речовини значною мірою відносяться до фізики, а також розглядаються у курсі загальної хімії. Нагадаємо основні положення цього розділу.
Сучасні уявлення щодо будови атома базуються на роботах Резерфорда, Бора, Планка, ейнштейна, Луї де Бройля.
Атом — електронейтральна мікросистема, що складається з позитивно зарядженого ядра та негативно заряджених електронів. Ядра атомів складаються з двох типів мікрочастинок (нуклонів) — протонів 11рі нейтронів 01п, основні характеристики яких подано в табл. 1.1.
Основна маса атома зосереджена в ядрі і характеризується масовим числом А, яке дорівнює сумі чисел протонів (тобто заряду ядра) Z і нейтронів N: A = Z + N. Атом і ядро характеризуються такими лінійними розмірами: атома — =10-8 , ядра — =10-12 – 10-13 см.
Таблиця 1.1. Основні характеристики елементарних частинок, які входять до складу атома
| Частинка | Символ | Маса спокою | Заряд | ||
| абсолютна, кг | відносна, а.о.м. | електричний, Кл | відносний | ||
| Протон | 11р | 1,673-10-27 | 1,007276 | 1,602-10-19 | +1 |
| Нейтрон | 11п | 1,675-10-27 | 1,008665 | ||
| Електрон | е | 9,109-10-31 | 0,000549 | 1,602-10-19 | -1 |
Заряд ядра, як головна характеристика атома, визначає число електронів, що обертаються навколо нього і врівноважують позитивний заряд ядра. Отже, заряд ядра зумовлює належність атома до певного виду хімічних елементів і відповідає порядковому номеру елемента в періодичній системі елементів Д. І. Менделєєва. У позначенні елемента відображають масове число А і кількість протонів Z, наприклад 3216S.
Атоми з однаковими значеннями Z, але з різними значеннями А і N, наприклад 168О, 178О, 188О, називають нуклідами(ізотопами).
Хімічний елемент — сукупність атомів, що мають однаковий заряд ядра і характеризуються певною атомною масою. Кожний елемент має свої назву і символ, наприклад: Гідроген – Н, Алюміній Al і т.д.
Найтиповішою формою існування речовини є молекула. Молекула — найменша частинка речовини, яка здатна існувати самостійно і зберігає всі хімічні властивості речовини.
Хімічною сполукою, або складною речовиною, називають індивідуальну речовину, молекули або кристали якої складаються з атомів двох або більше елементів, наприклад НС1, NaBr, HN03,, СаС2,, Na2Cr04 тощо.
Валентність елемента — це здатність його атомів приєднувати певне число атомів іншого елемента.
Маси атомів хімічних елементів надзвичайно малі. Саме тому користуються не їх абсолютними значеннями (та ), а відносними (Аг).
Відносною атомною масою хімічного елементаназивають відношення маси його атома (та ) до 1/12 маси нукліда Карбону С, тобто 1/12 маси нукліда Карбону 612С прийнято за атомну одиницю маси (а.о.м):
Відносною молекулярною масою Мг речовини називають відношення маси молекули до 1/12 маси атома нукліда Карбону 612С або масу молекули цієї речовини, виражену в атомних одиницях маси. За одиницю виміру кількості речовини в міжнародній системі одиниць (SI) прийнято величину моль. Моль— кількість речовини, яка містить стільки структурних елементарних одиниць (атомів, молекул, іонів, електронів, еквівалентів), скільки атомів міститься в 0,012 кг нукліда Карбону 126С.
Число атомів NA в 0,012 кг Карбону (тобто в одному моль його) визначають, виходячи з маси атома Карбону та (С) = 1,993• 10-26 кг:
NА = 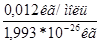 =6,02*1023 моль-1.
=6,02*1023 моль-1.
Цю величину називають сталою Авогадро (NA). Вона є однією з найважливіших універсальних сталих в усьому природознавстві і показує число структурних одиниць в одному моль будь-якої речовини, тобто відображає пропорційність між масою окремої молекули і молекулярною масою речовини. Слід зазначити, що стала Авогадро — це число частинок (атомів, молекул), які мають власний рух в об'ємі 22,4 м3 будь-якого газу за нормальних умов, тобто в мольному об'ємі газу.
Маса одного моля речовини називаєтьсямолярною масою М і визначається за співвідношенням маси (m) цієї речовини до її кількості ( 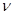 ):
):
М = m/v, кг/моль (або г/моль).
Згідно з квантово-механічній моделі атома електрон прийнято розглядати одночасно і як мікро матеріальну частинку, і як хвилю. Математично це положення описується рівнянням електронної хвилі де Бройля (1924), відповідно до якого частинці, що має масу і рухається зі швидкістю v, відповідає хвиля довжини А:
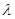 = h/mv,
= h/mv,
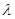 - довжина хвилі,
- довжина хвилі,
m – маса частинки,
v – її швидкість,
h — стала Планка (h = 6,626-10 -34 Дж • с).
Із поняття подвійної природи електрона випливає важливий висновок, відомий під назвою принципу невизначеності Гейзенберга: електрон з огляду на свою подвійну природу не допускає одночасної локалізації в координатному та імпульсному просторі. Звідси випливає, що рух електрона не можна описати за допомогою поняття про траєкторію.
З огляду на хвильову природу електрон характеризується хвильовою функцією 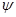 (псі), яка є амплітудою тривимірної електронної хвилі, тобто це амплітуда ймовірності перебування електрона у певній ділянці простору.
(псі), яка є амплітудою тривимірної електронної хвилі, тобто це амплітуда ймовірності перебування електрона у певній ділянці простору.
Електронна хмара, або атомна електронна орбіталь (АО), — квантово-механічна модель стану (руху) електрона в атомі — ділянка навколо-ядерного простору атома, що обмежена умовною поверхнею, яка не має чітких меж і де густина ймовірності наявності електрона (тобто електронна густина) досягає наперед заданої величини (як правило, 90 %).
Розрахунок хвильової функції у, тобто повне описування руху електрона в будь-якому тривимірному полі U(x, у, г), у квантовій механіці здійснюють за допомогою рівняння Шредінгера (1926).
Розв'язування рівняння Шредінгера (1.17), отже, математичне описування електронної орбіталі (АО) можливе лише за умови цілком визначених дискретних значень певних характеристик електрона, які називають квантовими числами: головним (п), орбітальним (/), магнітним (т1) і спіновим (ms). Головне квантове число визначає повний запас енергії електрона, тобто ступінь віддалення його від ядра або розмір електронної хмари (орбіталі). Воно набуває цілочислових значень 1, 2, 3, 4, 5, 6, 7..., які збігаються з нумерацією періодів у періодичній системі елементів Д. І. Менделєєва.
Орбітальне квантове число характеризує форму електронної хмари.
Магнітне квантове число характеризує просторову орієнтацію електронної хмари.
Спінове квантове число характеризує власний механічний момент електрона, зумовлений обертанням його навколо своєї осі.
Електронна конфігурація хімічних елементів залежить від положення елементу у періодичній таблиці і в значній мірі обумовлює фізичні, хімічні властивості елементів, а також їх сполук, і типи утворюваних в них зв’язків.
Тема 2. Перший закон термодинаміки
Хімічна термодинаміка. Основні поняття і визначення. Функції стану і функції процесу. Внутрішня енергія, теплота робота. Перший закон термодинаміки, його формулювання і аналітичний вираз. Робота 1 моль ідеального газу при різних процесах. Теплоємність. Емпіричні рівняння залежності теплоємності від температури. Теплові ефекти хімічних реакцій. Закон Гесса. Теплоти утворення, згоряння, розчинення, агрегатних перетворень. Таблиці стандартних ентальпій утворення речовин. Залежність теплового ефекту хімічної реакції від температури.
Термодинаміка являє собою наукову дисципліну, яка вивчає:
1) переходи енергії з однієї форми в іншу, від однієї частини системи до іншої;
2) енергетичні ефекти, які супроводжують різні фізичні або хімічні процеси, їх залежність від умов перебігу процесів;
3) можливість, напрям і межі перебігу самочинних (тобто без витрати енергії ззовні) процесів у заданих умовах.
Термодинаміка базується на кількох основних законах, з яких найважливішими є перший і другий закони (принципи) термодинаміки.
