Перший закон термодинаміки
Перший закон термодинаміки - це закон збереження енергії, поширений на теплові явища. Він показує, від яких причин залежить зміна внутрішньої енергії.
Закон збереження енергії управляє всіма явищами природи і пов'язує їх воєдино. Він завжди виконується абсолютно точно, не відомо жодного випадку, коли б цей великий закон не виконувався.
Цей закон був відкритий в середині XІХ ст. німецьким вченим, лікарем за освітою Р. Майєром (1814-1878), англійським ученим Дж. Джоулем (1818-1889) і отримав найбільш точне формулювання в працях німецького вченого Р. Гельмгольца (1821-1894).
І закон термодинаміки: Зміна внутрішньої енергії системи при переході з одного стану в інший дорівнює сумі роботи зовнішніх сил і кількості теплоти, переданої системі: 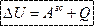
або: підведена до системи кількість теплоти йде частково на збільшення її внутрішньої енергії, а частково – на виконання системою (газом) роботи над зовнішніми тілами: 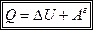
11. Застосування першого закону термодинаміки до різних процесів.
Ізобарний процес (р= const): 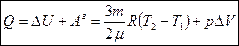 При нагріванні газу відбувається збільшення внутрішньої енергії та виконання роботи по розширенню газу. При ізобарному стисканні газу, необхідно зовнішнім силам виконати роботу, щоб тиск залишився постійним. Газ повинен віддати навколишнім тілам деяку кількість теплоти…
При нагріванні газу відбувається збільшення внутрішньої енергії та виконання роботи по розширенню газу. При ізобарному стисканні газу, необхідно зовнішнім силам виконати роботу, щоб тиск залишився постійним. Газ повинен віддати навколишнім тілам деяку кількість теплоти…
Ізотермічний процес (Т= const): Оскільки температура незмінна, то немає і зміни внутрішньої енергії, тому 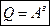 Вся підведена до ідеального газу енергія (тепло, кількість теплоти) витрачається на виконання роботи. Якщо газ віддає тепло (Q < 0), А' < 0. Робота зовнішніх сил над газом в цьому випадку позитивна ( Азов> 0).
Вся підведена до ідеального газу енергія (тепло, кількість теплоти) витрачається на виконання роботи. Якщо газ віддає тепло (Q < 0), А' < 0. Робота зовнішніх сил над газом в цьому випадку позитивна ( Азов> 0).
Ізохорний процес (V= const): Оскільки розширення газу відсутній, то робота дорівнює нулю, тому
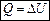 Вся підведена енергія іде на зміну його внутрішньої енергії.
Вся підведена енергія іде на зміну його внутрішньої енергії.
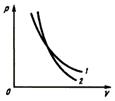
Адіабатний процес - процес, що відбувається без теплообміну з навколишнім середовищем. У чистому вигляді адіабатні процеси зустрічаються рідко, однак, багато швидких процесів, при яких теплообмін з навколишнім середовищем просто не встигає статися, близькі до адіабатного.(а) стискання повітря в повітряному огниве (дослід); б) стискання повітря у дизелі; в) утворення хмар.) 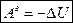 Робота виконується за рахунок внутрішньої енергії. (1 – ізотерма 2 – політропа (ізобара)). Температура повітря при адіабатному розширення знижується. Оскільки, при адіабатному стисканні газу підвищується температура, тиск зростає швидше, ніж при ізотермічному процесі. Зниження температури при адіабатному розширенні призведе до того, що тиск зменшується швидше. На графіку адіабата йде крутіше ізотерми.
Робота виконується за рахунок внутрішньої енергії. (1 – ізотерма 2 – політропа (ізобара)). Температура повітря при адіабатному розширення знижується. Оскільки, при адіабатному стисканні газу підвищується температура, тиск зростає швидше, ніж при ізотермічному процесі. Зниження температури при адіабатному розширенні призведе до того, що тиск зменшується швидше. На графіку адіабата йде крутіше ізотерми.
Дослід: вилітає з пляшки пробка що містить насичений водяний пар, при накачуванні в неї повітря, в ній утворюється туман.
