Основное уравнение молекулярно-кинетической теории идеальных газов
МОЛЕКУЛЯРНАЯ ФИЗИКА И ТЕРМОДИНАМИКА
Молекулярно-кинетическая теория идеальных газов
В физике для описания тепловых явлений используют два основных метода: молекулярно-кинетический (статистический) и термодинамический.
Молекулярно-кинетический метод (статистический) основан на представлении о том, что все вещества состоят из молекул, находящихся в хаотическом движении. Так как число молекул огромно, то можно, применяя законы статистики, найти определенные закономерности для всего вещества в целом.
Термодинамический метод исходит из основных опытных законов, получивших название законов термодинамики. Термодинамический метод подходит к изучению явлений подобно классической механике, которая базируется на опытных законах Ньютона. При таком подходе не рассматривается внутреннее строение вещества.
Основные положения молекулярно-кинетической теории
И их опытное обоснование. Броуновское движение.
Масса и размер молекул.
Теорию, которая изучает тепловые явления в макроскопических телах и объясняет зависимости внутренних свойств тел от характера движения и взаимодействия между частицами, из которых состоят тела, называют молекулярно-кинетической теорией (сокращённо МКТ) или просто молекулярной физикой.
В основе молекулярно-кинетической теории лежат три важнейшие положения:
Согласно первому положению МКТ, все тела состоят из огромного количества частиц (атомов и молекул), между которыми есть промежутки.
Атом – это электрически нейтральная микрочастица, состоящая из положительно заряженного ядра и окружающей его электронной оболочки. Совокупность атомов одного вида называют химическим элементом. В естественном состоянии в природе встречаются атомы 90 химических элементов, наиболее тяжёлым из которых является уран. При сближении атомы могут объединяться в устойчивые группы. Системы из небольшого числа связанных друг с другом атомов называют молекулой. Например, молекула воды состоит из трёх атомов (рис.): двух атомов водорода (Н) и одного атома кислорода (О), поэтому её обозначают Н2О. Молекулыявляютсянаименьшими устойчивыми частицами данного вещества, 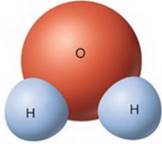 обладающими его основными химическими свойствами. Например, наименьшая частица воды – это молекула воды, наименьшая частица сахара – молекула сахара.
обладающими его основными химическими свойствами. Например, наименьшая частица воды – это молекула воды, наименьшая частица сахара – молекула сахара.
Про вещества, состоящие из атомов, не объединённых в молекулы, говорят, что они находятся в атомарном состоянии; в противном случае говорят о молекулярном состоянии. В первом случае мельчайшей частицей вещества является атом (например Не), во втором случае – молекула (например Н2О).
Если два тела состоят из одного и того же числа частиц, то говорят, что эти тела содержат одинаковое количество вещества. Количество вещества обозначается греческой буквой ν(ню) и измеряется в молях. За 1 моль принимают количество вещества в 12 г углерода. Так как в 12 г углерода содержится приблизительно 6∙1023 атомов, то для количества вещества (т.е. числа молей) в теле, состоящем из N частиц, можно написать
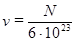 моль. (1)
моль. (1)
Если ввести обозначения NA= 6∙1023 моль-1.
то соотношение (1) примет вид следующей простой формулы:
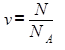 (2)
(2)
 Таким образом, количество вещества— это отношение числа N молекул (атомов) в данном макроскопическом теле к числу NA атомов в 0,012 кг атомов углерода:
Таким образом, количество вещества— это отношение числа N молекул (атомов) в данном макроскопическом теле к числу NA атомов в 0,012 кг атомов углерода:
В 1 моле любого вещества содержится NA = 6,02·1023 молекул. Число NA называют постоянной Авогадро.Физический смысл постоянной Авогадро заключается в том, что её значение показывает число частиц (атомов- в атомарном веществе, молекул –в молекулярном), содержащееся в 1 моле любого вещества.
Массу одного моля вещества называют молярной массой. Если молярную массу обозначить буквой μ, то для количества вещества в теле массой m можно записать:
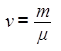 (3)
(3)
Из формул (2) и (3) следует, что число частиц в любом теле можно определить по формуле:
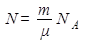 (4)
(4)
Молярная масса определяется по формуле
М=Мг ·10-3кг/моль
Здесь через Мг обозначена относительная молекулярная (атомная) масса вещества, измеренная в а.е.м. (атомные единицы массы), которой в молекулярной физике принято характеризовать массу молекул (атомов).Относительную молекулярную массуМг можно определить, если среднюю массу молекулы ( mm) данного вещества разделить на 1/12 массы изотопа углерода 12С:
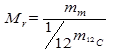
1/12 m12C = 1а.е.м =1,66·10-27 кг.
 При решении задач эту величину находят с помощью таблицы Менделеева. В этой таблице указаны относительные атомные массы элементов. Складывая их в соответствии с химической формулой молекулы данного вещества, и получают относительную молекулярную Мг.Например, для
При решении задач эту величину находят с помощью таблицы Менделеева. В этой таблице указаны относительные атомные массы элементов. Складывая их в соответствии с химической формулой молекулы данного вещества, и получают относительную молекулярную Мг.Например, для
углерода (С) Мг=12·10-3кг/моль
воды (Н2О)Мг=(1·2+16)=18·10-3кг/моль.
Аналогично определяется и относительная атомная масса.
Моль газа при нормальных условиях занимает объем V0 = 22,4·1023 м3
Следовательно, в 1 м3 любого газа при нормальных условиях (определяемых давлением Р=101325 Па =105Па=1атм; температурой 273ºК (0ºС), объёмом 1 моля идеального газа V0=22,4 10-3м3) содержится одинаковое число молекул:
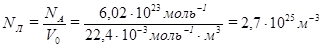
Это число получило название постоянной Лошмидта.
Чётких границ молекулы (как и атомы) не имеют. Размеры молекул твёрдых тел можно ориентировочно оценить следующим образом:
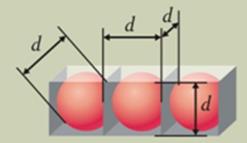
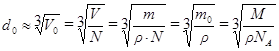
где 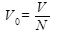 - объём приходящийся на 1 молекулу,
- объём приходящийся на 1 молекулу, 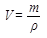 - объём всего тела,
- объём всего тела,
m и ρ – его масса и плотность, N – число молекул в нём.
Атомы и молекулы нельзя увидеть невооружённым глазом или с помощью оптического микроскопа. Поэтому сомнения многих учёных конца XIX в. в реальности их существования понять можно. Однако в XX в. ситуация стала иной. Сейчас с помощью электронного микроскопа, а также средств голографической микроскопии можно наблюдать изображение не только молекул, но даже отдельных атомов.
Данные рентгеноструктурного анализа показывают, что диаметр любого атома имеет порядок d = 10-8 см (10-10 м). Размеры молекул больше размеров атомов. Поскольку молекулы состоят из нескольких атомов, то чем больше количество атомов в молекуле, тем больше её размер. Размеры молекул лежат в пределах от 10-8 см (10-10 м) до 10-5 см (10-7 м).
Массы отдельных молекул и атомов очень малы, например абсолютное значение массы молекулы воды порядка 3·10-26 кг. Массу отдельных молекул экспериментально определяют с помощью специального прибора – масс-спектрометра.
Кроме прямых экспериментов, позволяющих наблюдать атомы и молекулы, в пользу их существования говорит и множество других косвенных данных. Таковы, например, факты, касающиеся теплового расширения тел, их сжимаемости, растворения одних веществ в других и т.д.
Согласно второму положению молекулярно-кинетической теории,частицы непрерывно и хаотически (беспорядочно) движутся.
Это положение подтверждается существованием диффузии, испарения, давление газа на стенки сосуда, а также явлением броуновского движения.
Хаотичность движения означает, что у молекул не существует каких-либо предпочтительных путей и их движения имеют случайные направления.
Диффузия (от латинского diffusion – растекание, распространение) – явление, когда в результате теплового движения вещества происходит самопроизвольное проникновение одного вещества в другое (если эти вещества соприкасаются). Согласно молекулярно-кинетической теории, такое перемешивание происходит в результате того, что беспорядочно движущиеся молекулы одного вещества проникают в промежутки между молекулами другого вещества. Глубина проникновения зависит от температуры: чем выше температура, тем больше скорость движения частиц вещества и тем быстрее протекает диффузия. Диффузия наблюдается во всех состояниях вещества – в газах, жидкостях и твёрдых телах. Наиболее быстро диффузия происходит в газах (именно поэтому так быстро распространяется запах в воздухе). В жидкостях диффузия происходит медленнее, чем в газах. Это объясняется тем, что молекулы жидкости расположены значительно гуще, и потому «пробираться» через них значительно труднее. Медленнее всего диффузия происходит в твёрдых телах. В одном из опытов гладко отшлифованные пластины свинца и золота положили одна на другую и сжали грузом. Через пять лет золото и свинец проникли друг в друга на 1мм. Диффузия в твёрдых телах обеспечивает соединение металлов при сварке, пайке, хромировании и т.п. Диффузия имеет большое значение в процессах жизнедеятельности человека, животных и растений. Например, именно благодаря диффузии кислород из лёгких проникает в кровь человека, а из крови - в ткани.
Броуновским движением называют беспорядочное движение взвешенных в жидкости или газе мелких частичек другого вещества. Это движение было открыто в 1827 г. английским ботаником Р.Броуном, который наблюдал в микроскоп движение цветочной пыльцы, взвешенной в воде. В наше время для таких наблюдений используют маленькие части краски гуммигут, которая не растворяется в воде. В газе броуновское движение совершают, например, взвешенные в воздухе частицы пыли или дыма. Броуновское движение частицы возникает потому, что импульсы, с которыми молекулы жидкости или газа действуют на эту частицу, не компенсируют друг друга. Молекулы среды (то есть молекулы газа или жидкости) движутся хаотично, поэтому их удары приводят броуновскую частицу в беспорядочное движение: броуновская частица быстро меняет свою скорость по направлению и по величине (рис.1).
 |
В ходе изучения броуновского движения было обнаружено, что его интенсивность: а) увеличивается с ростом температуры среды; б) увеличивается при уменьшении размеров самих броуновских частиц; в)уменьшается в более вязкой жидкости и г) совершенно не зависит от материала (плотности) броуновских частиц. Кроме того, было установлено, что это движение универсально (поскольку наблюдается у всех веществ, взвешенных в распыленном состоянии в жидкости), непрерывно (в закрытом со всех сторон кювете, его можно наблюдать неделями, месяцами, годами) и хаотично (беспорядочно).
Согласно третьему положению МКТ, частицы вещества взаимодействуют друг с другом: притягиваются на небольших расстояниях и отталкиваются, когда эти расстояния уменьшаются.
Наличие сил межмолекулярного взаимодействия (сил взаимного притяжения и отталкивания) объясняет существование устойчивых жидких и твёрдых тел.
Этими же причинами объясняется малая сжимаемость жидкостей и способность твёрдых тел сопротивляться деформациям сжатия и растяжения.
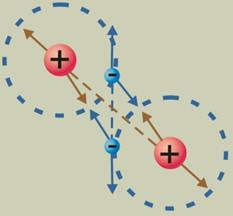 Силы межмолекулярного взаимодействия имеют электромагнитную природу и сводятся к двум типам: притяжению и отталкиванию. Эти силы проявляются на расстояниях, сравнимых с размерами молекул. Причиной этих сил является то, что молекулы и атомы состоят из заряженных частиц с противоположными знаками зарядов – отрицательных электронов и положительно заряженных атомных ядер. В целом молекулы электрически нейтральны. На рисунке 2.2 с помощью стрелок показано, что ядра атомов, внутри которых находятся положительно заряженные протоны, отталкиваются друг от друга, так же ведут себя и отрицательно заряженные электроны. А вот между ядрами и электронами действуют силы притяжения.
Силы межмолекулярного взаимодействия имеют электромагнитную природу и сводятся к двум типам: притяжению и отталкиванию. Эти силы проявляются на расстояниях, сравнимых с размерами молекул. Причиной этих сил является то, что молекулы и атомы состоят из заряженных частиц с противоположными знаками зарядов – отрицательных электронов и положительно заряженных атомных ядер. В целом молекулы электрически нейтральны. На рисунке 2.2 с помощью стрелок показано, что ядра атомов, внутри которых находятся положительно заряженные протоны, отталкиваются друг от друга, так же ведут себя и отрицательно заряженные электроны. А вот между ядрами и электронами действуют силы притяжения.
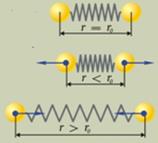 Зависимость сил взаимодействия молекул от расстояния между ними качественно объясняет молекулярный механизм появления сил упругости в твёрдых телах. При растяжении твёрдого тела частицы удаляются друг от друга. При этом появляются силы притяжения молекул, которые возвращают частицы в первоначальное положение. При сжатии твёрдого тела частицы сближаются на расстояния. Это приводит к увеличению сил отталкивания, которые возвращают частицы в первоначальное положение и препятствуют дальнейшему сжатию.
Зависимость сил взаимодействия молекул от расстояния между ними качественно объясняет молекулярный механизм появления сил упругости в твёрдых телах. При растяжении твёрдого тела частицы удаляются друг от друга. При этом появляются силы притяжения молекул, которые возвращают частицы в первоначальное положение. При сжатии твёрдого тела частицы сближаются на расстояния. Это приводит к увеличению сил отталкивания, которые возвращают частицы в первоначальное положение и препятствуют дальнейшему сжатию.
Поэтому при малых деформациях (в миллионы раз превышающих размер молекул) выполняется закон Гука, согласно которому сила упругости пропорциональна деформации. При больших смещениях закон Гука не действует
О справедливости этого положения свидетельствует сопротивляемость всех тел сжатию, а также (за исключением газов) –их растяжению.
Основное уравнение молекулярно-кинетической теории идеальных газов
Объем газа всегда совпадает с объемом того сосуда, который он занимает.
Давление возникает в результате ударов молекул о стенки сосудов. Рассмотрим поведение одной произвольно выбранной молекулы и идеального газа, находящейся в сосуде, имеющем форму куба (рис. 2.8). Пусть υi-ее скорость, направленная перпендикулярно стенке сосуда, а mi — масса. При упругом ударе молекула сообщает стенке импульс miυi после удара ее импульс станет равным - miυi. Следовательно, импульс молекулы изменится на miυi-(-miυi)= 2miυi. По второму закону Ньютона,
Fiti =2 miυi. (2.22)
Если в кубе, длина ребра которого равна ℓ, находится n молекул, то вследствие беспорядочного движения молекул и равновероятности всех направлений можно считать, что 1/3N молекул движется вдоль оси X, 1/3N— вдоль оси Y, 1/3N молекул — вдоль оси Z. Чтобы найти среднюю силу давления газа, следует подсчитать сумму импульсов всех молекул, ударяющихся о стенку за определенное время. От удара до следующего удара о ту же грань молекула проходит путь, в среднем равный 2ℓ. Интервал времени между двумя этими ударами равен ti = 2ℓ/υi. Определим теперь среднюю силу, с которой действует на одну из стенок сосуда одна молекула. В уравнение (2.22) подставим время ti между двумя ударами:
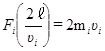
откуда
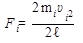 или
или 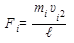
Молекулы газа движутся с различной скоростью (υ1, ..., υi, ..., υn); следовательно, они сообщают стенке сосуда и различные импульсы. Выберем какое-либо одно направление движения молекул (например, вдоль оси X). Между двумя противоположными гранями куба в этом направлении движется 1/3 всех молекул, и суммарная сила ударов об одну грань
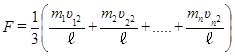
В идеальном газе m1 = m2 = ... = mn = m, поэтому
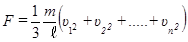
Умножив и разделив правую часть равенства на N, получим
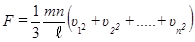
Выражение, стоящее в скобках, есть квадрат средней квадратической скорости движения молекул 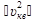 . Таким образом,
. Таким образом,
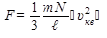
Cледовательно,
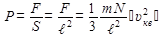
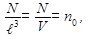
Тогда
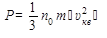
Это основное уравнение молекулярно-кинетической теории.
Оно определяет макроскопическую величину — давление газа через концентрацию n0 молекул, массу m отдельных молекул и среднюю квадратическую скорость 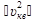 их движения.
их движения.
Если через 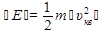 обозначить среднюю кинетическую энергию поступательного движения некой «средней» молекулы, то уравнение (2.25) можно записать в виде
обозначить среднюю кинетическую энергию поступательного движения некой «средней» молекулы, то уравнение (2.25) можно записать в виде
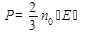
Давление газа равно 2/3 от средней кинетической энергии поступательного движения всех молекул, которые содержатся в единичном объеме газа.
Следствия, вытекающим из основного уравнения молекулярно-кинетической теории газов.
Ø Возьмем 1 моль газа, который занимает объем V. Плотность молекул газа 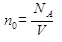 и уравнение (2.26) можно записать в виде
и уравнение (2.26) можно записать в виде 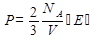
Но для 1 моль справедливо уравнение состояния рV = RТ, откуда
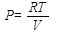
Подставив это выражение для давления в уравнение (2.27) и решив его относительно Т или 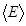 , получим:
, получим:
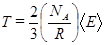 (2.28)
(2.28)
Из уравнения (2.28) следует, что термодинамическая температура пропорциональна средней кинетической энергии хаотического движения молекул газа.
Ø Чем быстрее движутся молекулы, тем выше температура. Из уравнения (2.28) находим
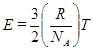 (2.28а)
(2.28а)
для любого газа, откуда следует:средняя кинетическая энергия молекул разных газов, находящихся при одинаковой температуре, равна между собой.
Из равенства средних кинетических энергий газовых молекул следует, что при перемешивании различных газов, имеющих одинаковые температуры, не происходит преимущественной передачи энергии от молекул одного газа молекулам другого.
Величина 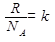 получила название постоянной Больцмана и представляет собой газовую постоянную, отнесенную к одной молекуле:
получила название постоянной Больцмана и представляет собой газовую постоянную, отнесенную к одной молекуле:
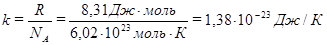
Следовательно, выражение (2.28а) можно представить в виде
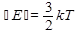 (229)
(229)
Ø Подставляя (2.29) в (2.26), находим выражение для давления газа:
Р = n0kТ (230)
Давление газа пропорционально произведению числа молекул в единице объема на его термодинамическую температуру.
Анализ уравнения (2.29) показывает, что при Т=0К кинетическая энергия поступательного движения молекул Е=0, а следовательно, и 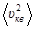 = 0. Таким образом, при Т = 0 К отсутствует поступательное движение молекул.
= 0. Таким образом, при Т = 0 К отсутствует поступательное движение молекул.
Однако это не означает, что при Т=0К прекращается движение вообще. Сохраняются вращательное и колебательное движения атомов и молекул. По современным представлениям, при Т=0К у атомов и еще более мелких частиц остается некоторая энергия, называемая нулевой.
Представим теперь формулу (2.29) в виде
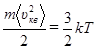
откуда средняя квадратическая скорость
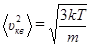 (2.31)
(2.31)
Отсюда следует: средняя квадратическая скорость молекул пропорциональна корню квадратному из термодинамической температуры.
На основании выражения (2.29) можно установить определение температуры: термодинамическая температура с точностью до постоянного множителя 3/2k равна средней кинетической энергии поступательного движения молекулы идеального газа.
