Заряд, размер и масса атомного ядра. Массовое и зарядовое числа. Состав ядра. Нуклоны.
Э. Резерфорд, исследуя прохождение a-частиц с энергией в несколько мегаэлектрон-вольт через тонкие пленки золота (см. § 208), пришел к выводу о том, что атом состоит из положительно заряженного ядра и окружающих его электронов. Проанализировав эти опыты, Резерфорд также показал, что атомные ядра имеют размеры примерно 10–14 — 10–15 м (линейные размеры атома примерно 10–10 м).
Атомное ядро состоит из элементарных частиц —протонов и нейтронов (протонно-нейтронная модель ядра была предложена российским физиком Д. Д. Иваненко (р. 1904), а впоследствии развита В. Гейзенбергом).
Протон (р) имеет положительный заряд, равный заряду электрона, и массу покоя тр=1,6726×10–27кг » 1836 тe, где тe — масса электрона. Нейтрон (n) — нейтральная частица с массой покоя тп=1,6749×10–27кг »1839 тe. Протоны и нейтроны называютсянуклонами (от лат. nucleus — ядро). Общее число нуклонов в атомном ядре называется массовым числом А.
Атомное ядро характеризуется зарядом Ze, гдеZ —зарядовое число ядра, равное числу протонов в ядре и совпадающее с порядковым номером химического элемента в Периодической системе элементов Менделеева. Известные в настоящее время 107 элементов таблицы Менделеева имеют зарядовые числа ядер от Z= 1 до Z= 107.
Ядро обозначается тем же символом, что и нейтральный атом: 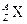 , гдеХ — символхимического элемента, Z атомный номер (число протонов в ядре), А —массовоечисло (число нуклонов в ядре).
, гдеХ — символхимического элемента, Z атомный номер (число протонов в ядре), А —массовоечисло (число нуклонов в ядре).
Сейчас протонно-нейтронная модель ядра не вызывает сомнений. Рассматривалась также гипотеза о протонно-электронном строении ядра, но она не выдержала экспериментальной проверки. Так, если придерживаться этой гипотезы, то массовое число А должно представлять собой число протонов в ядре, а разность между массовым числом и числом электронов должна быть равна зарядовому числу. Эта модель согласовывалась со значениями изотопных масс и зарядов, но противоречила значениям спинов и магнитных моментов ядер, энергии связи ядра и т. д. Кроме того, она оказалась несовместимой с соотношением неопределенностей (см. § 215). В результате гипотеза о протонно-электронном строении ядра была отвергнута.
Так как атом нейтрален, то заряд ядра определяет и число электронов в атоме. От числа же электронов зависит их распределение по состояниям в атоме, от которого, в свою очередь, зависят химические свойства атома. Следовательно, заряд ядра определяет специфику данного химического элемента, т.е. определяет число электронов в атоме, конфигурацию их электронных оболочек, величину и характер внутриатомного электрического поля.
Ядра с одинаковыми Z, но разными А (т. е. с разными числами нейтронов N=A–Z) называютсяизотопами, а ядра с одинаковыми А, но разными Z—изобарами. Например, водород (Z=1) имеет три изотопа: 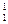 Н—протий (Z=1, N=0),
Н—протий (Z=1, N=0), 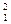 Н—дейтерий (Z=1, N=1),
Н—дейтерий (Z=1, N=1), 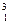 Н — тритий (Z=1, N=2), олово—десять, и т. д. В подавляющем большинстве случаев изотопы одного и того же химического элемента обладают одинаковыми химическими и почти одинаковыми физическими свойствами (исключение составляют, например, изотопы водорода), определяющимися в основном структурой электронных оболочек, которая является одинаковой для всех изотопов данного элемента. Примером ядер-изобар могут служить ядра
Н — тритий (Z=1, N=2), олово—десять, и т. д. В подавляющем большинстве случаев изотопы одного и того же химического элемента обладают одинаковыми химическими и почти одинаковыми физическими свойствами (исключение составляют, например, изотопы водорода), определяющимися в основном структурой электронных оболочек, которая является одинаковой для всех изотопов данного элемента. Примером ядер-изобар могут служить ядра 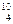 Ве,
Ве, 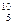 В,
В, 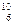 С. В настоящее время известно более 2500 ядер, отличающихся либо Z, либо А, либо тем и другим.
С. В настоящее время известно более 2500 ядер, отличающихся либо Z, либо А, либо тем и другим.
Радиус ядра задается эмпирической формулой 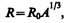 где R0=(1,3¸1,7)10–15 м.
где R0=(1,3¸1,7)10–15 м.
