Активна потужність залежить лише від величини активного опору 4 страница
3. l

| |
L
5. DE ~ l 2
533.
n?
Як залежить енергія електрона Е в потенціальній ямі від головного квантового числа
E ~ n2

| |
2. n
3. E ~ n
4. E ~ n3
 E ~ 1
E ~ 1
5. n
534.
Яка імовірність D проходження електрона через потенціальний бар’єр шириною a?

|
1. è h ø
 D ~ exp æ - 2a
D ~ exp æ - 2a
2m (U- E ) ö
ç ÷
2. è h ø

|
3. è h ø

|
4. è h ø

|
5. è h ø
535.
Запишіть формулу для визначення енергетичних рівнів квантового осцилятора
1. E = hw(u +1/ 2)
2. E = hwu
E = hw
3. 2
4. E = hw
5. E = hwn
536.
Яка енергія «нульових» коливань квантового осцилятора?
1. E = hw(u+1/ 2)
E = hw
2. 2
3. E = hwu
4. E = hw
5. E = hwn
537.
Як виглядає рівняння Шредінгера для хвильової функції F(f)
електрона в атомі
водню?
h2 d 2F

| |
1. 2m dj
|
|
 2
2
2. 2m dj
D 2F

| |
3. dj

| |
4. dj
|
 2
2
5. dj
538.
Як квантується квадрат моменту кількості руху в теорії Шредінгера?
|
|
1.
2. M 2 = nl
 M 2 = h
M 2 = h
3.
4. M 2 = hl2
l(l+1)
|
5.
539.
Як квантується момент кількості руху в теорії Шредінгера
1.  M = njh
M = njh
2. M = h
3. M = nl2
l (l+1)
4. M = hl(l+1)
5. M = nl
540.
Які значення приймає орбітальне квантове число
lв теорії Шредінгера?
1. l= 0, 1, 2, 3... n -1
2. l = 1, 2, 3... n
3. l = -m, 0, m
4. l = 2n +1
5. l = -n, 0, n
541.
Які електрони можуть проникати в ядро?
1. s – електрони
2. р – електрони
3. f – електрони
4. q – електрони
5. h – електрони
542.
Для якого електрона квадрат радіальної хвильової функції не дорівнює нулю в ядрі
атома?
1. для f – електрона
2. для q – електрона
3. для s – електрона
4. для р – електрона
5. для d – електрона
543.
Який орбітальний момент
l мають s – електрони ?
1. l = 0
2. l = 1
3. l = 2
4. l = 3
5. l = 4
544.
На скільки компонент розщепиться пучок атомів із зовнішнім s – електроном у досліді
Штерка-Герлага?
1. на 2
2. на 3
3. на 5
4. на 4
5 не розщепиться
545.
1. 1
2. 3
3. 2
4. 5
5. 6
Скільки різних просторових орієнтацій може мати р –електрон?
546.
1. 1
2. 2
3. 5
4. 4
5. 6
Скільки різних просторових орієнтацій має d- електрон?
547.
n2
Яка кількість електронів утворює електронний шар із головним квантовим числом n?
1.
2. 2n
3. 2n2
4. n
5. 2n + 1
548.
Яка кількість електронів утворює електронну оболонку з орбітальним квантовим
числом
l ?
1. l2
2. 2l2
3. 2l
4. 2l + 1
2 (2l+1)
5.
549.
1. 2
2. 1
3. 4
4. 5
5. 6
Скільки електронів формують К- шар атома?
550.
1. 2
2. 10
3. 6
4. 4
5. 8
Скільки електронів знаходяться на оболонці з l = 2 ?
551.
1. 1
2. 2
3. 6
4. 8
5. 10
Скільки електронів міститься на р – оболонці?
552.
1. 1
2. 2
3. 6
4. 8
5. 10
Скільки електронів міститься в шарі з n=2?
553.
Запишіть електронну конфігурацію атома Na.
|
2. 1s22s
|
|
|
554.
1s2
Запишіть електронну конфігурацію атома Ne.
1.
2. 1s22s2
|
|
|
555.
Запишіть вираз для визначення повного моменту одноелектронного атома:
1. j = s
2. j = 2l +1
3. j = 2l + m
4. j = l ± s
5. j = l
556.
1. 1
2. 2
3. 3
4. 4
5. 5
Яка мультиплетність станів одноелектронних атомів:
|
Як визначається мультиплетність енергетичних станів атомів Lj
1. c = 2s +1
2. c = l + s
3. c = 2 j
4. c = 2m +1
5. c = l +1
558.
Як залежить від порядкового номера атома величина спін-орбітального розщеплення?
 DE ~ 1
DE ~ 1
1. Z

| |
2. Z
3. DE ~ Z
4. DE ~ Z 3
5. DE ~ Z 4
559.
Які енергетичні рівні утворює (sd) - конфігурація?
1. D2
3 3 3
2. D1,
3.
| |
D2, D3
1 3 3 3
4. P1 ,
P0 ,
P1 , P2
1 3 3 3
5. D2,
D1,
D2, D3
560.
Взаємодія яких електронів із електромагнітним вакуумом приводить до зсуву Лемба
(рівня
S1/ 2 )
1. s – електронів
2. p – електронів
3. d – електронів
4. f – електронів
5. q – електронів
561.
Які правила відбору для переходів в атомі по орбітальному квантовому числу:
1. Dl = ±1
2. Dl = 0, ±1
3. Dl = 1
4. Dl = 0
5. Dl = -1
562.
Які правила відбору по спіну для оптичних переходів у легких атомах?
1. Ds = 0
2. Ds = ±1
3. Ds = 0, ±1
4. Ds = 1
5. Ds = -1
563.
У позначенні енергетичного терму
c L
|
1. мультиплетність
2. спін атома
3. орбітальний момент
4. повний момент
5. виродженість
564.
1. спін
У позначенні енергетичного терму
|
2. повний момент атома
3. виродженість
4. орбітальний момент
5. мультиплетність
565.
Як поляризовані компоненти Зеєманівського розщеплення у випадку поперечного
розщеплення?
1. лінійно
2. циркулярно
3. еліптично
566.
Які енергетичні стани має електронна конфігурація (sp)?
| |
1. 2
|
2. 1
3 3 3
3. P0,
P1 , P2
1 3 3 3
4. P1 ,
P0 ,
P1 , P2
| |
5. 1
567.
Які стани за мультиплетністю мають двоелектронні атоми?
1. дублетні
2. дублетні та триплетні
3. синглетні та триплетні
4. триплетні
5. синглетні
568.
Які правила відбору по спіну для інтеркомбінаційних переходів?
1. Ds = 2
2. Ds = -1
3. Ds = 1
4. Ds = 0
5. Ds = ±1
569.
1. s=1
2. s=0
Який спін станів, що відповідають так званому «ортогелію»?
3. s=1/2
4. s=2
5. s=3
570.
1. s=1
2. s=0
Який спін станів, що відповідають так званому «парагелію»?
3. s=1/2
4. s=2
5. s=3
571.
1. 3
2. 2
3. 4
4. 1
5. 5
На скільки компонент в магнітному полі розщепиться рівень 1P1
572.
Скільки спектральних компонент спостерігають у випадку повздовжнього
1. 1
2. 2
3. 4
4. 5
5. 3
нормального ефекту Зеємана?
573.
1. 4
2. 2
3. 1
4. 3
5. 5
На скільки компонент в магнітному полі розщепиться рівень 1D2
574.
Яка величина розщеплення енергетичних рівнів у випадку аномального ефекту
Зеємана?
1. DE = mБ× m
2. DE = mБ× В × m
3. DE = mБ× h
DE =
4.
e hB
 2m ;
2m ;
5. DE = mБ g × В × m .
575.
1. 2
2. 4
3. 5
4. 1
5. 3
На скільки компонент в магнітному полі розщепиться рівень 2S1/2
576.
Характеристичне Х-випромінювання виникає :
1. при рекомбінації електронів внутрішніх оболонок з дірками К-оболонки
2. при гальмуванні е- електронним полем речовини
3. при рекомбінації електронів зони провідності із дірками валентної зони
4. при створенні дірки в К-оболонці
5. у випадку Оже-рекомбінації
577.
1. 1
2. 5
3. 4
4. 3
5. 2
На скільки компонент в магнітному полі розщепиться рівень 2P1/2
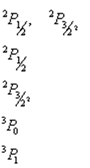 578.
578.
1.
2.
3.
4.
5.
Які стани має електрон в атомі, якщо 
579.
1. 5
2. 1
3. 4
4. 3
5. 2
На скільки компонент в магнітному полі розщепиться рівень 2P3/2
580.
1. 1
2.1/2
3. 0
4. 2
5. 3
Який спін електронного стану, що описується термом 2F5/2
581.
Які правила відбору для магнітного квантового числа для p -компонент, які
спостерігаються в ефекті Зеємана?
1. Δm = 0
2. Δm = 1
3. Δm = - 1
4. Δm = ±1
582.
Які правила відбору для магнітного квантового числа для s - компонент, які
спостерігаються при Зеєманівському розщепленні?
1. Δm=
2. Δm=±1
3. Δm=1
4. Δm= -1
583.
1. 1
2. 3
3. 4
4. 5
5. 6
Скільки спектральних компонент спостерігається у випадку ефекту Пашена-Бака?
584.
Кαлінії рентгенівського характеристичного випромінювання виникають при
переходах:
1. L→K
2. М→K
3. N→K
4. K→N
5. O→L
585.
Гальмівне Х-випромінювання виникає:
1. при рекомбінації електронів внутрішніх оболонок з дірками К-оболонки
2. при гальмуванні електронів електричним полем речовини
3. при рекомбінації електронів зони провідності із дірками валентної зони
4. при створенні дірки в К-оболонці
5. у випадку Оже-рекомбінації
586.
У результаті розсіяння Х-квантів на електронах атома довжина хвилі Х-променів
змінюється на:
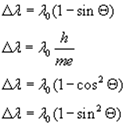 1.
1. 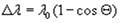
2.
3.
4.
5.
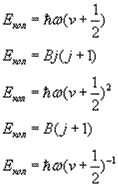 587.
587.
1.
2.
3.
4.
5.
Формула для визначення коливної енергії молекул:
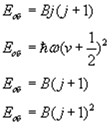 588.
588.
1.
2.
3.
4.
Формула для визначення обертової енергії молекули:
589.
Що розуміють під поняттям «гіромагнітне відношення»?
1. ексцентриситет орбіти електрона
2. відношення механічного моменту електрона до спінового моменту
3. відношення магнітного моменту ядра до магнітного моменту атома
4. відношення магнітного моменту електрона до його механічного моменту
5. величина спін-орбітальної взаємодії
590.
За що відповідає магнітне квантове число?
1. за величину магнітного поля в ядрі
2. за спін електрона
3. за форму орбіти електрона
4. за просторову орієнтацію атомної орбіталі
5. за механічний момент електрона
591.
Яку енергію треба надати електрону в атомі водню, щоб його енергія стала
додатньоюАшре?
1. 27,2 еВ
2. 13,6 еВ
3. 10,2 еВ
4. 16,3 еВ
5. 13,2 еВ
592.
Яка розмірність постійної Планка?
1. Дж/с2
2. Дж·с·кг-2
3. Дж-1·с·кг2
4. Дж·с-1·кг2
5. Дж·с
593.
Що продемонстрували досліди Франка-Герца?
1. наявність магнітного моменту ядра
2. наявність спін-орбітальної взаємодії в атомі
3. дискретність енергетичних рівнів електрона в атомі
4. наявність магнітного квантового числа
5. структуру ядра атома
594.
За що відповідає азимутальне квантове число?
1. за величину магнітного поля в ядрі
2. за спін електрона
3. за форму орбіти електрона
4. за просторовий розподіл атомної орбіталі
5. за механічний момент електрона
595.
Як зміниться енергія атома водню при переході з основного в перший збуджений
стан?
1. зменшиться в 3/4 раз
2. збільшиться в 4 рази
3. зменшиться в 4 рази
4. збільшиться на R
5. збільшиться на 3/4 R
596.
Електрон на рівні n=2 рухається по коловій орбіті. Яке значення азимутвльного
1. 0
2. 1
3. 2
4. 3
5. 4
квантового числа для такого електрона?
597.
З прізвищем якого вченого зв’язана планетарна модель атома
1. Томпсон
2. Резерфорд
3. Бальмер
4. Ньютон
5. Коперник
598.
1. 0
2. 1
3. 2
4. 3
5. 4
На рівень з яким n відбуваються переходи в серії Бальмера?
599.
Електрон рухається в потенціальному полі з енергією (-e2/r). Запишіть одномірне
рівняння Шредінгера
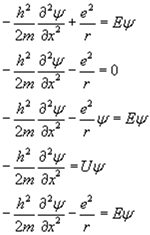 1.
1.
2.
3.
4.
5.
600.
Яке мінімальне значення приймає величина ∆x∆p ?
1. 0,001ħ
2. h
3. 1000h
4. 0,01ħ
601.
Ядерна фізика
Частинки, які володіють півцілим спіном, називаються:
1 гіперонами
2 баріонами
3 лептонами
4 бозонами
5 ферміонами
602.
Дробовими значеннями електричного заряду (в одиницях електронних зарядів)
володіють:
1 кварки ?
2 електрони
3 томи
4 мезони
5 нуклони
603.
Для яких значень заряду ядер розсіюючих атомів перерізи розсіяння електронів на
ядрах і електронних оболонках атомів є однаковими?
1 Z=1 ?
2 Z=10
3 Z=17
4 Z=2
5 Z=92
604.
В експериментах Р.Хофштадтера з пружного розсіяння електронів вивчалася
структура:
1 кварків
2 електронів
3 атомів
4 мезонів
5 нуклонів
605.
Відповідно до теорії ядерних взаємодій Х.Юкави взаємодія між нуклонами
здійснюється за участю
1 каонів
2 мюонів
3 гіперонів
4 пі-мезонів
5 етонів
606.
Ефект Мессбауера пов’язаний з резонансним поглинанням:
1 гамма-квантів
2 електронів
3 світлових квантів
4 позитронів
5 кварків
607.
Бетатрон використовується для прискорення:
1 важких ядер
2 електронів
3 іонів
4 протонів
5 кварків
608.
Масове число ядер для основних радіоактивних рядів можна виразити формулою (де
С – стале для ряду число; n – ціле число):
1 А=3n+С
2 А=5n+С
3 А=n+С
4 А=3n+n2+С
5 А=4n+С
609.
Який ізотоп не використовується,як ядерне паливо?
1 U-235
2 U-233
3 U-238
4 Pu-239
5 О-16 ?
610.
Термоядерним реакціям, що відбувається в зорях, притаманний цикл:
1 Гелієвий ?
2 кисневий
3 вуглецевий
4 кремнієвий
5 титановий
611.
Ядра, які володіють однаковим числом протонів, називаються:
1 ізобарами
2 ізотонами
3 ізотопами
4 бозонами
5 ферміонами
612.
Яке з перелічених чисел можна віднести до магічних:
1 7
2 13
3 25
4 4 ?
5 111
613.
«Грей» є одиницею вимірювання:
1 експозиційної дози
2 еквівалентної дози
3 активності
4 ефективного перерізу реакції
5 поглинутої дози ?
614.
В експериментах Ц.Ву виявлено:
1 втрату парності при слабких ядерних взаємодіях
