Анализ политропного процесса
Политропными называется класс термодинамических процессов, при протекании которых неизменно одно и тоже количество подводимого тепла идет на изменение внутренней энергии.
Термодинамический процесс, при протекании которого теплоемкость остается постоянной, относится к политропным:
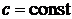 .
.
Политропные процессы – это процессы, которые протекают при постоянном для данного процесса показателе политропы  .
.
Найдем уравнение политропного процесса. Для этого запишем уравнение первого начала термодинамики через внутреннюю энергию и энтальпию:
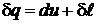 ,
, 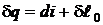 . (5.1)
. (5.1)
Вспоминая, что 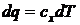 ,
, 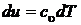 , а
, а 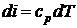 , перепишем уравнения в виде, считая термодинамическую систему, состоящую из идеального газа
, перепишем уравнения в виде, считая термодинамическую систему, состоящую из идеального газа 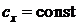 и
и 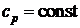
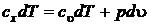 ,
, 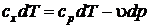 .
.
Выразим из (5.1) теплоемкость процесса 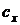 :
:
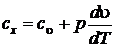 ,
, 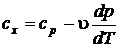 .
.
После несложных преобразований получим
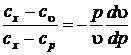 ;
; 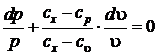 . (5.2)
. (5.2)
Введём обозначение
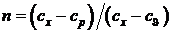 . (5.3)
. (5.3)
Тогда дифференциальное уравнение политропного процесса (5.2) с учетом обозначений (5.3) запишется в виде
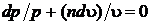 .
.
Проинтегрируем полученное дифференциальное уравнение
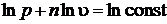 .
.
Откуда после потенциирования получим уравнение политропного процесса:
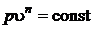 , (5.4)
, (5.4)
где  – показатель политропы (5.3)
– показатель политропы (5.3)
Выражение (5.3) можно решить относительно теплоемкости процесса « 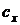 »:
»:
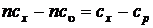 ;
; 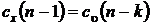 .
.
Тогда выражение для расчета теплоемкости любого произвольного политропного процесса может быть найден из зависимости (5.5)
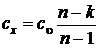 . (5.5)
. (5.5)
Изобразим политропный процесс в р, u – и T, S – диаграммах
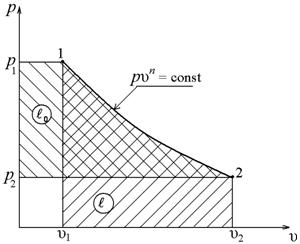 Рисунок 5.1 р, u – диаграмма политропы Рисунок 5.1 р, u – диаграмма политропы |
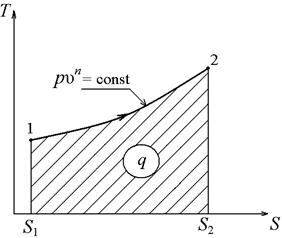 Рисунок 5.2 T, S – диаграмма политропы Рисунок 5.2 T, S – диаграмма политропы |
Изменение внутренней энергии за процесс
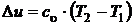 . (5.6)
. (5.6)
Изменение энтальпии за процесс
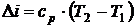 . (5.7)
. (5.7)
Количество тепла подведенное (отведенное) в процессе
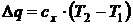 . (5.8)
. (5.8)
Запишем выражение для расчета элементарной работы за процесс 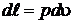 .
.
Если состояние системы в процессе изменяется от удельного объема 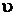 , до
, до 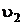 то результирующую работу найдем интегрированием.
то результирующую работу найдем интегрированием.
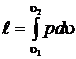 .
.
Из уравнения процесса 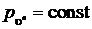 выразим давление
выразим давление  , подставим его в выражение интеграла и проинтегрируем:
, подставим его в выражение интеграла и проинтегрируем:
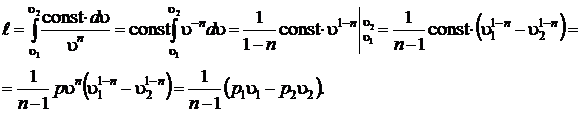
Таким образом удельная работа расширения в политропных процессах определяется выражением (5.9)
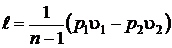 . (5.9)
. (5.9)
Удельная величина располагаемой работы равна 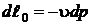 .
.
Конечная за процесс величина располагаемой работы может быть найдена интегрированием бесконечно малого изменения 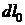 от начального давления
от начального давления 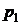 системы до его конечного значения в процессе
системы до его конечного значения в процессе 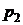 .
.
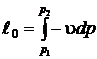 .
.
Запишем удельный объем 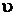 через параметр
через параметр 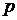 воспользовавшись опять уравнением процесса
воспользовавшись опять уравнением процесса
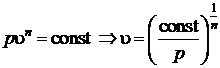
Подставим полученное выражение в интеграл для расчета располагаемой работы и проинтегрируем
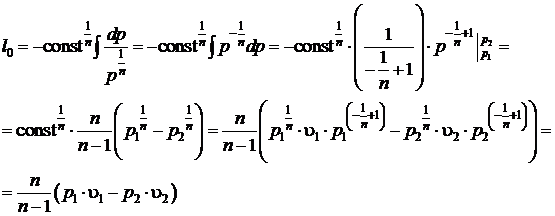

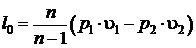 (5.10)
(5.10)
Таким образом сопоставляя выражения для расчета работы расширения (5.9) в политропном процессе с располагаемой работой (5.10) отметим, что последнее в  раз больше
раз больше 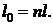
Найдем изменение энтропии в процессе. Для этого воспользуемся уравнением первого начала термодинамики в дифференциальной форме
 .
.
Перепишем его в виде объединенного уравнения 1го и 2го начал через внутреннюю энергию 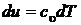 и энтальпию
и энтальпию 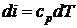 ,
, 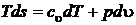 ,
, 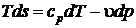 . Выразим из последних выражений дифференциал энтропии
. Выразим из последних выражений дифференциал энтропии
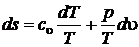 ,
, 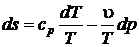 .
.
Воспользуемся уравнением состояния идеального газа 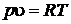 и выразим давление
и выразим давление 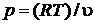 и удельный объем
и удельный объем 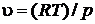 . После подстановки полученных выражений в зависимости для расчета энтропии получим
. После подстановки полученных выражений в зависимости для расчета энтропии получим
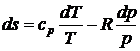 ,
, 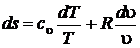 ,
,
или после интегрирования
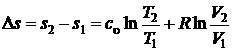 , (5.11)
, (5.11)
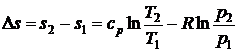 . (5.12)
. (5.12)
Часть тепла, пошедшая на изменение внутренней энергии
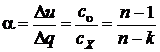 . (5.13)
. (5.13)
