Эффект Джоуля-Томпсона. Сжижение газов. Фазовые переходы первого и второго родов.
Адиабатическое расширение реального газа с совершением внешними силами положительной работы—осуществили английские физики Джоуль Томсон.
Рассмотрим эффект Джоуля — Томсона. На рис. 93 представлена схема их опыта. В теплоизолированной трубке с пористой перегородкой находятся два поршня, которые могут перемешаться без трения. Пусть сначала слева от перегородки газ под поршнем 1 находится под давлением р1, занимает объем V1 при температуре Т1, а справа газ отсутствует (поршень 2 придвинут к перегородке). После прохождения газа через пористую перегородку в правой части газ характеризуется параметрами р2, V2, T2. Давления p1 и p2 поддерживаются постоянными (p1>p2).
Так как расширение газа происходит без теплообмена с окружающей средой (адиабатически), то на основании первого начала термодинамики
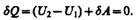

Внешняя работа, совершаемая газом, состоит из положительной работы при движении поршня 2 (А2=р2V2) и отрицательной при движении поршня 1 (A1=p1V1), т. е. dA=A2—A1. Подставляя выражения для работ в формулу, получаем
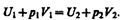
Таким образом, в опыте Джоуля — Томсона сохраняется (остается неизменной) величина U+pV. Она является функцией состояния и называется энтальпией.
Ради простоты рассмотрим 1 моль газа. Подставляя в формулу выражение и рассчитанные из уравнения Ван-дер-Ваальса значения p1V2и р2V2 (символ «m» опять опускаем) и производя элементарные преобразования, получаем
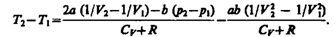
Из выражения следует, что знак разности (T2—T1)зависит от того, какая из поправок Ван-дер-Ваальса играет бóльшую роль. Проанализируем данное выражение, сделав допущение, что p2<<p1 и V2>>V1:
1) а »0 — не учитываем силы притяжения между молекулами, а учитываем лишь размеры самих молекул. Тогда
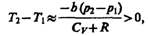
т. е. газ в данном случае нагревается;
2) b»0 — не учитываем размеров молекул, а учитываем лишь силы притяжения между молекулами. Тогда
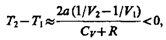
т. е. газ в данном случае охлаждается;
3) учитываем обе поправки. Подставив в выражение вычисленное из уравнения Ван-дер-Ваальса значение р1, имеем
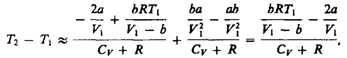
т. е. знак разности температур зависит от значений начального объема V1 и начальной температуры Т1.
Изменение температуры реального газа в результате его адиабатического расширения, или, как говорят,адиабатического дросселирования — медленного прохождения газа под действием перепада давления сквозьдроссель (например, пористую перегородку), называетсяэффектом Джоуля—Томсона. Эффект Джоуля — Томсона принято называтьположительным, если газ в процессе дросселирования охлаждается (DT<0), иотрицательным, если газ нагревается (DT> 0).
В зависимости от условий дросселирования для одного и того же газа эффект Джоуля — Томсона может быть как положительным, так и отрицательным. Температура, при которой (для данного давления) происходит изменение знака эффекта Джоуля — Томсона, называетсятемпературой инверсии. Ее зависимость от объема получим, приравняв выражение нулю:
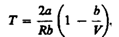
Кривая, определяемая уравнением, — кривая инверсии. Область выше этой кривой соответствует отрицательному эффекту Джоуля — Томсона, ниже — положительному. Отметим, что при больших перепадах давления на дросселе температура газа изменяется значительно. Так, при дросселировании от 20 да 0,1 МПа и начальной температуре 17° С воздух охлаждается на 35° С.
Эффект Джоуля — Томсона обусловлен отклонением газа от идеальности. В самом деле, для моля идеального газа рVm=RТ, поэтому выражение примет вид
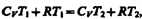
откуда следует, что Т1 = T2.
§ 65. Сжижение газов
Превращение любого газа в жидкость — сжижение газа — возможно лишь при температуре ниже критической . При ранних попытках сжижения газов оказалось, что некоторые газы (Cl, СО2, NH3) легко сжижались изотермическим сжатием, а целый ряд газов (O2, N2, H2, He) сжижению не поддавался. Подобные неудачные попытки объяснил Д. И. Менделеев, показавший, что сжижение этих газов производилось при температуре, большей критической, и поэтому заранее было обречено на неудачу. Впоследствии удалось получить жидкий кислород, азот и водород (их критические температуры равны соответственно 154,4, 126,1 и 33 К), а в 1908 г. нидерландский физик Г. Камерлинг-Оннес (1853—1926) добился сжижения гелия, имеющего самую низкую критическую температуру (5,3 К).
Для сжижения газов чаще применяются два промышленных метода, в основе которых используется либо эффект Джоуля—Томсона, либо охлаждение газа при совершении им работы.
Схема одной из установок, в которой используется эффект Джоуля—Томсона, — машины Линде* — представлена на рис. 95. Воздух в компрессоре (К) сжимается до давления в десятки мегапаскаль и охлаждается в холодильнике (X) до температуры ниже температуры инверсии, в результате чего при дальнейшем расширении газа наблюдается положительный эффект Джоуля — Томсона (охлаждение газа при его расширении). Затем сжатый воздух проходит по внутренней трубе теплообменника (ТО) и пропускается через дроссель (Др), при этом он сильно расширяется и охлаждается. Расширившийся воздух вновь засасывается по внешней трубе теплообменника, охлаждая вторую порцию сжатого воздуха, текущего по внутренней трубе. Так как каждая следующая порция воздуха предварительно охлаждается, а затем пропускается через дроссель, то температура понижается все больше. В результате 6—8-часового цикла часть воздуха (»5%), охлаждаясь до температуры ниже критической, сжижается и поступает в дьюаровский сосуд (ДС), а остальная его часть возвращается в теплообменник. 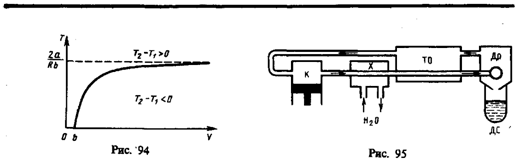
Второй метод сжижения газов основан на охлаждении газа при совершении им работы. Сжатый газ, поступая в поршневую машину (детадер), расширяется и совершает при этом работу по передвижению поршня. Taк как работа совершается за счет внутренней энергии газа, то его температура при этом понижается.
Фазовые переходы I и П рода
Фазой называется термодинамически равновесное состояние вещества, отличающееся по физическим свойствам от других возможных равновесных состояний того же вещества. Если, например, в закрытом сосуде находится вода, то эта система является двухфазной: жидкая фаза — вода; газообразная фаза — смесь воздуха с водяными парами. Если в воду бросить кусочки льда, то эта система станет трехфазной, в которой лед является твердой фазой. Часто понятие «фаза» употребляется в смысле агрегатного состояния, однако надо учитывать, что оно шире, чем понятие «агрегатное состояние». В пределах одного агрегатного состояния вещество может находиться в нескольких фазах, отличающихся по своим свойствам, составу и строению (лед, например, встречается в пяти различных модификациях — фазах). Переход вещества из одной фазы в другую — фазовый переход — всегда связан с качественными изменениями свойств вещества. Примером фазового перехода могут служить изменения агрегатного состояния вещества или переходы, связанные с изменениями в составе, строении и свойствах вещества (например, переход кристаллического вещества из одной модификации в другую).
Различают фазовые переходы двух родов. Фазовый переход I рода (например, плавление, кристаллизация и т. д.) сопровождается поглощением или выделением теплоты, называемой теплотой фазового перехода. Фазовые переходы I рода характеризуются постоянством температуры, изменениями энтропии и объема. Объяснение этому можно дать следующим образом. Например, при плавлении телу нужно сообщить некоторое количество теплоты, чтобы вызвать разрушение кристаллической решетки. Подводимая при плавлении теплота идет не на нагрев тела, а на разрыв межатомных связей, поэтому плавление протекает при постоянной температуре. В подобных переходах — из более упорядоченного кристаллического состояния в менее упорядоченное жидкое состояние — степень беспорядка увеличивается, т. е., согласно второму началу термодинамики, этот процесс связан с возрастанием энтропии системы. Если переход происходит в обратном направлении (кристаллизация), то система теплоту выделяет.
Фазовые переходы, не связанные с поглощением или выделением теплоты и изменением объема, называются фазовыми переходами II рода. Эти переходы характеризуются постоянством объема и энтропии, но скачкообразным изменением теплоемкости. Общая трактовка фазовых переходов II рода предложена академиком Л. Д. Ландау (1908—1968). Согласно этой трактовке, фазовые переходы II рода связаны с изменением симметрии: выше точки перехода система, как правило, обладает более высокой симметрией, чем ниже точки перехода. Примерами фазовых переходов II рода являются: переход ферромагнитных веществ (железа, никеля) при определенных давлении в температуре в парамагнитное состояние; переход металлов и некоторых сплавов при температуре, близкой к 0 К, в сверхпроводящее состояние, характеризуемое скачкообразным уменьшением электрического сопротивления до нуля; превращение обыкновенного жидкого гелия (гелия I) при Т=2,9 К в другую жидкую модификацию (гелий II), обладающую свойствами сверхтекучести.
