Применение первого закона термодинамики к изопроцессам
Напомним, что в изопроцессе остаётся неизменным значение некоторой величины, характеризующей состояние газа — температуры, объёма или давления. Для каждого вида изопроцессов запись первого закона термодинамики упрощается.
1. Изотермический процесс, T = const.
Внутренняя энергия идеального газа зависит только от его температуры. Если температура газа не меняется, то не меняется и внутренняя энергия: ∆U = 0. Тогда формула (11) даёт:
Q = A.
Всё подведённое к газу тепло идёт на совершение газом работы.
2. Изохорный процесс, V = const.
Если объём газа остаётся постоянным, то поршень не перемещается, и потому работа газа равна нулю: A = 0. Тогда первый закон термодинамики даёт:
Q = ∆U.
Всё тепло, переданное газу, идёт на изменение его внутренней энергии.
3. Изобарный процесс, p = const.
Подведённое к газу тепло идёт как на изменение внутренней энергии, так и на совершение работы (для которой справедлива формула (9)). Имеем:
Q = ∆U + p∆V.
Адиабатный процесс
Процесс называется адиабатным, если он идёт без теплообмена с окружающими телами.
Адиабатный процесс совершается газом, находящимся в теплоизолированном сосуде. Такой сосуд препятствует всем видам теплопередачи: теплопроводности, конвекции, излучению. Пример теплоизолированного сосуда — термос.
Приблизительно адиабатным будет всякий процесс, протекающий достаточно быстро: в течение процесса теплообмен просто не успевает произойти.
При адиабатном процессе Q = 0. Из первого закона термодинамики получаем: A + ∆U = 0, или A = −∆U.
В процессе адиабатного расширения газ совершает положительную работу, поэтому ∆U <0 (работа совершается за счёт убыли внутренней энергии). Следовательно, газ охлаждается. Если заставить газ совершить достаточно большую работу, охладить его можно весьма сильно. Именно на этом основаны методы сжижения газов.
Наоборот, в процессе адиабатного сжатия будет A <0, поэтому ∆U >0: газ нагревается. Адиабатное нагревание воздуха используется в дизельных двигателях для воспламенения топлива.
Кривая, изображающая ход адиабатного процесса, называется адиабатой. Интересно сравнить ход адиабаты и изотермы на pV -диаграмме (рис. 30).
| p |
| изотерма |
| адиабата |
V
Рис. 30. Сравнительный ход изотермы и адиабаты
В обоих процессах давление убывает с увеличением объёма, но в адиабатном процессе убывание идёт быстрее. Почему?
При изотермическом расширении давление падает потому, что уменьшается концентрация частиц газа, в результате чего удары частиц по стенкам сосуда становятся реже. Однако интенсивность этих ударов остаётся прежней: ведь температура газа не меняется — значит, не меняется и средняя кинетическая энергия его частиц.
А при адиабатном расширении, наряду с уменьшением концентрации частиц, падает также и температура газа. Удары частиц становятся не только более редкими, но и более слабыми. Вот почему адиабата убывает быстрее изотермы.
Тепловые машины
Коротко говоря, тепловые машины преобразуют теплоту в работу или, наоборот, работу в теплоту.
Тепловые машины бывают двух видов — в зависимости от направления протекающих в них процессов.
1. Тепловые двигатели преобразуют теплоту, поступающую от внешнего источника, в механическую работу.
Автомобильный двигатель внутреннего сгорания — это пример теплового двигателя. В нём происходит преобразование тепла, выделяющегося при сгорании топлива, в механическую энергию автомобиля.
2. Холодильные машины передают тепло от менее нагретого тела к более нагретому за счёт механической работы внешнего источника.
Бытовой холодильник, который стоит у вас в квартире, служит примером холодильной машины. В нём тепло отводится от холодильной камеры и передаётся в окружающее пространство.
Рассмотрим эти виды тепловых машин более подробно.
Тепловые двигатели
Мы знаем, что совершение над телом работы есть один из способов изменения его внутренней энергии: совершённая работа как бы растворяется в теле, переходя в энергию беспорядочного движения и взаимодействия его частиц.
| Нагреватель |
| Холодильник |
| Рабочеетело |
| двигателя |
| A |
| Q |
| Q |
Принципиальную схему теплового двигателя можно изобразить следующим образом (рис. 31). Давайте разбираться, что означают элементы данной схемы.
Рабочее тело двигателя — это газ. Он расширяется, двигает поршень и совершает тем самым полезную механическую работу.
Но чтобы заставить газ расширяться, преодолевая внешние силы, нужно нагреть его до температуры, которая существенно выше температуры окружающей среды. Для этого газ приводится в контакт с нагревателем — сгорающим топливом.
В процессе сгорания топлива выделяется значительная энергия, часть которой идёт на нагревание газа. Газ получает от нагревателя количество теплоты Q1. Именно за счёт этого тепла двигатель совершает полезную работу A.
Это всё понятно. Что такое холодильник и зачем он
Рис. 31. Тепловой двигатель нужен?
При однократном расширении газа мы можем использовать поступающее тепло максимально эффективно и целиком превратить его в работу. Для этого надо расширять газ изотермически: первый закон термодинамики, как мы знаем, даёт нам в этом случае A = Q1.
Но однократное расширение никому не нужно. Двигатель должен работать циклически, обеспечивая периодическую повторяемость движений поршня. Следовательно, по окончании расширения газ нужно сжимать, возвращая его в исходное состояние.
В процессе расширения газ совершает некоторую положительную работу A1. В процессе сжатия над газом совершается положительная работа A2 (а сам газ совершает отрицательную работу −A2). В итоге полезная работа газа за цикл: A = A1 − A2.
Разумеется, должно быть A >0, или A2 < A1 (иначе никакого смысла в двигателе нет). Сжимая газ, мы должны совершить меньшую работу, чем совершил газ при расширении.
Как этого достичь? Ответ: сжимать газ под меньшими давлениями, чем были в ходе расширения. Иными словами, на pV -диаграмме процесс сжатия должен идти ниже процесса расширения, т.е. цикл должен проходиться по часовой стрелке (рис. 32).
| V |
| p |
| a |
| b |
| V |
| V |
| A |
Рис. 32. Цикл теплового двигателя
Например, в цикле на рисунке работа газа при расширении равна площади криволинейной трапеции V11a2V2. Аналогично, работа газа при сжатии равна площади криволинейной трапеции V11b2V2 со знаком минус. В результате работа A газа за цикл оказывается положительной и равной площади цикла 1a2b1.
Хорошо, но как заставить газ возвращаться в исходное состояние по более низкой кривой, то есть через состояния с меньшими давлениями? Вспомним, что при данном объёме давление газа тем меньше, чем ниже температура. Стало быть, при сжатии газ должен проходить состояния с меньшими температурами.
Вот именно для этого и нужен холодильник: чтобы охлаждать газ в процессе сжатия. Холодильником может служить атмосфера (для двигателей внутреннего сгорания) или охлаждающая проточная вода (для паровых турбин).
При охлаждении газ отдаёт холодильнику некоторое количество теплоты Q2. Суммарное количество теплоты, полученное газом за цикл, оказывается равным Q1−Q2. Согласно первому закону термодинамики:
Q1 − Q2 = A + ∆U,
где ∆U — изменение внутренней энергии газа за цикл. Оно равно нулю: ∆U = 0, так как газ вернулся в исходное состояние (а внутренняя энергия, как мы помним, является функцией состояния). В итоге работа газа за цикл получается равна:
A = Q1 − Q2. (12)
Как видите, A < Q1: не удаётся полностью превратить в работу поступающее от нагревателя тепло. Часть теплоты приходится отдавать холодильнику — для обеспечения цикличности процесса.
Показателем эффективности превращения энергии сгорающего топлива в механическую работу служит коэффициент полезного действия теплового двигателя.
КПД теплового двигателя — это отношение механической работы A к количеству теплоты Q1, поступившему от нагревателя:
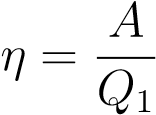 .
.
С учётом соотношения (12) имеем также
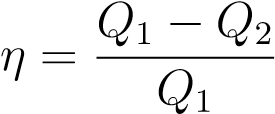 . (13)
. (13)
КПД теплового двигателя, как видим, всегда меньше единицы. Например, КПД паровых турбин приблизительно 25%, а КПД двигателей внутреннего сгорания около 40%.
Холодильные машины
Житейский опыт и физические эксперименты говорят нам о том, что в процессе теплообмена теплота передаётся от более нагретого тела к менее нагретому, но не наоборот. Никогда не наблюдаются процессы, в которых за счёт теплообмена энергия самопроизвольно переходит от холодного тела к горячему, в результате чего холодное тело ещё больше остывало бы, а горячее тело — ещё больше нагревалось.
| Нагреватель |
| Холодильник |
| Рабочеетело |
| холодильной |
| машины |
| Q |
| Q |
По сравнению с тепловым двигателем процессы в холодильной машине имеют противоположное направление (рис. 33).
Рабочее тело холодильной машины называют также
хладагентом. Мы для простоты будем считать его газом,0
A который поглощает теплоту при расширении и отдаёт при сжатии[21].
Холодильник в холодильной машине — это тело, от которого отводится теплота. Холодильник передаёт рабочему телу (газу) количество теплоты Q2, в результате чего газ расширяется.
В ходе сжатия газ отдаёт теплоту Q1 более нагретому телу — нагревателю. Чтобы такая теплопередача осуществлялась, надо сжимать газ при более высоких температурах, чем были при расширении. Это возможно лишь за счёт работы A0, совершаемой внешним источником (на- Рис. 33. Холодильная машина пример, электродвигателем)[22]. Поэтому количество тепло-
ты, передаваемое нагревателю, оказывается больше количества теплоты, забираемого от холодильника, как раз на величину A0:
Q1 = Q2 + A0.
Таким образом, на pV -диаграмме рабочий цикл холодильной машины идёт против часовой стрелки. Площадь цикла — это работа A0, совершаемая внешним источником (рис. 34).
| V |
| p |
| b |
| a |
| V |
| V |
| A |
Рис. 34. Цикл холодильной машины
Основное назначение холодильной машины — охлаждение некоторого резервуара (например, морозильной камеры). В таком случае данный резервуар играет роль холодильника, а нагревателем служит окружающая среда — в неё рассеивается отводимое от резервуара тепло.
Показателем эффективности работы холодильной машины является холодильный коэффициент, равный отношению отведённого от холодильника тепла к работе внешнего источника:
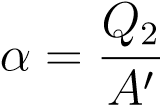 .
.
Холодильный коэффициент может быть и больше единицы. В реальных холодильниках он принимает значения приблизительно от 1 до 3.
Имеется ещё одно интересное применение: холодильная машина может работать как тепловой насос. Тогда её назначение — нагревание некоторого резервуара (например, обогрев помещения) за счёт тепла, отводимого от окружающей среды. В данном случае этот резервуар будет нагревателем, а окружающая среда — холодильником.
Показателем эффективности работы теплового насоса служит отопительный коэффициент, равный отношению количества теплоты, переданного обогреваемому резервуару, к работе внешнего источника:
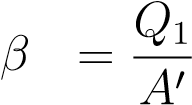 .
.
Значения отопительного коэффициента реальных тепловых насосов находятся обычно в диапазоне от 3 до 5.
Тепловая машина Карно
Важными характеристиками тепловой машины являются наибольшее и наименьшее значения температуры рабочего тела в ходе цикла. Эти значения называются соответственно температурой нагревателя и температурой холодильника.
Мы видели, что КПД теплового двигателя строго меньше единицы. Возникает естественный вопрос: каков наибольший возможный КПД теплового двигателя с фиксированными значениями температуры нагревателя T1 и температуры холодильника T2?
Пусть, например, максимальная температура рабочего тела двигателя равна 1000 K, а минимальная — 300 K. Каков теоретический предел КПД такого двигателя?
Ответ на поставленный вопрос дал французский физик и инженер Сади Карно в 1824 году. Он придумал и исследовал замечательную тепловую машину с идеальным газом в качестве рабочего тела. Эта машина работает по циклу Карно, состоящему из двух изотерм и двух адиабат.
Рассмотрим прямой цикл машины Карно, идущий по часовой стрелке (рис. 35). В этом случае машина функционирует как тепловой двигатель.
| V |
| p |
| T |
| T |
Рис. 35. Цикл Карно
Изотерма 1 → 2. На участке 1 → 2 газ приводится в тепловой контакт с нагревателем температуры T1 и расширяется изотермически. От нагревателя поступает количество теплоты Q1 и целиком превращается в работу на этом участке: A12 = Q1.
Адиабата 2 → 3. В целях последующего сжатия нужно перевести газ в зону более низких температур. Для этого газ теплоизолируется, а затем расширяется адиабатно на учатке 2 → 3. При расширении газ совершает положительную работу A23, и за счёт этого уменьшается его внутренняя энергия: ∆U23 = −A23.
Изотерма 3 → 4. Теплоизоляция снимается, газ приводится в тепловой контакт с холодильником температуры T2. Происходит изотермическое сжатие. Газ отдаёт холодильнику количество теплоты Q2 и совершает отрицательную работу A34 = −Q2.
Адиабата 4 → 1. Этот участок необходим для возврата газа в исходное состояние. В ходе адиабатного сжатия газ совершает отрицательную работу A41, а изменение внутренней энергии положительно: ∆U41 = −A41. Газ нагревается до исходной температуры T1.
Карно нашёл КПД этого цикла (вычисления, к сожалению, выходят за рамки школьной программы):
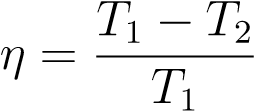 . (14)
. (14)
Кроме того, он доказал, что КПД цикла Карно является максимально возможным для всех тепловых двигателей с температурой нагревателя T1 и температурой холодильника T2. Так, в приведённом выше примере (T1 = 1000 K, T2 = 300 K) имеем:
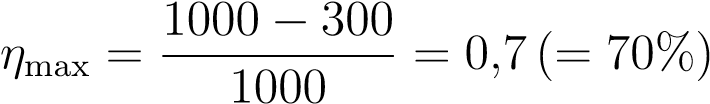 .
.
В чём смысл использования именно изотерм и адиабат, а не каких-то других процессов? Оказывается, изотермические и адиабатные процессы делают машину Карно обратимой. Её можно запустить по обратному циклу (против часовой стрелки) между теми же нагревателем и холодильником, не привлекая другие устройства. В таком случае машина Карно будет функционировать как холодильная машина.
Возможность запуска машины Карно в обоих направлениях играет очень большую роль в термодинамике. Например, данный факт служит звеном доказательства максимальности КПД цикла Карно. Мы ещё вернёмся к этому в следующей статье, посвящённой второму закону термодинамики.
