Вопрос. Теория атома водорода по Бору. Постулаты Бора. Спектр атома водорода по Бору. Недостатки теории Бора.
| Модель атома водорода по Бору | ||
На электрон со стороны ядра действует кулоновская сила, сообщая ему центростремительное ускорение. Поэтому 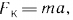 | ||
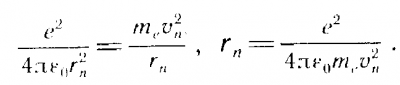 | ||
Из правила квантования: 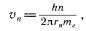 Подставляя уравнение для скорости электрона на орбите в предыдущее, получим: Подставляя уравнение для скорости электрона на орбите в предыдущее, получим: 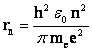 , где n=1,2,3... , где n=1,2,3... | 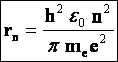 | |
Если п=1, а r1 =0,5-10-10 м, то r2=r1.n2=4r1, r3=9r1 и т.д. Т.о. 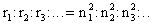 или rn~n2. или rn~n2. | 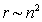 | |
Полная энергия атома равна: Е = Ek + Eп 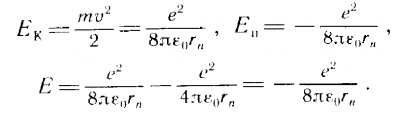 | ||
Подставляя выражение для радиуса стационарной орбиты, получим: 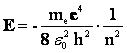 Знак "-" говорит о том, что между электроном и ядром действуют силы притяжения. Знак "-" говорит о том, что между электроном и ядром действуют силы притяжения. | 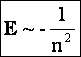 | |
Переход электрона с более высокой орбиты k на орбиту п сопровождается излучением фотона с частотой: 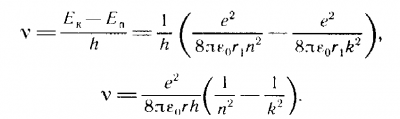 Таким образом, мы пришли к формуле Бальмера, где Таким образом, мы пришли к формуле Бальмера, где 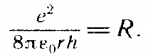 - постоянная Ридберга. - постоянная Ридберга. | 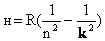 | |
| Трудности теории Бора Правило квантования Бора применимо не всегда, представление об определенных орбитах, по которым движется электрон в атоме Бора, оказалось условным. Теория Бора неприменима для многоэлектронных атомов и не объясняет ряд спектральных закономерностей. | 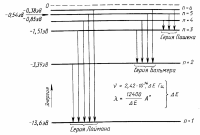 | |
| В 1917 г. А. Эйнштейн предсказал возможность перехода атома с высшего энергетического состояния в низшее под влиянием внешнего воздействия. Такое излучение называется вынужденным излучением и лежит в основе работы лазеров. | ||
| Постулаты Бора | ||
| 1. Атомная система может находиться только в особых стационарных квантовых состояниях, каждому из которых соответствует определенная энергия Еn . В стационарном состоянии атом не излучает. | ||
2. При переходе атома из стационарного состояния с большей энергией Ek в стационарное состояние с меньшей энергией En излучается квант энергии: 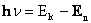 | 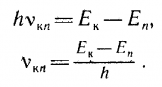 | |
3. К этим постулатам следует добавить правило квантования орбит: в стационарном состоянии атома электрон, двигаясь по круговой орбите, должен иметь дискретные, квантованные значения момента импульса 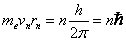 где rn - радиус n-ой орбиты; vn—скорость электрона на этой орбите; me— масса электрона, п—целое число - номер орбиты или главное квантовое число. где rn - радиус n-ой орбиты; vn—скорость электрона на этой орбите; me— масса электрона, п—целое число - номер орбиты или главное квантовое число. | 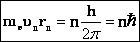 | |
| Спектральные закономерности | 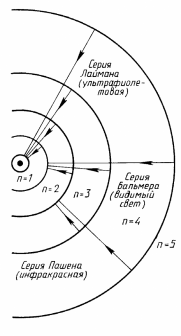 | |
В середине XVIII в. Г. Кирхгоф обнаружил: свечение газов дает четко выраженные дискретные линии. Швейцарский преподаватель И. Бальмер эмпирически вывел формулу для спектра водорода (1885): 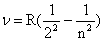 , где п—любое целое число >2, т. е. п=3, 4, 5 и т.д. , где п—любое целое число >2, т. е. п=3, 4, 5 и т.д. | ||
| Величина R носит название "постоянная Ридберга" | ||
Для инфракрасной области спектра аналогичную формулу вывел Ф. Пашен: 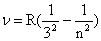 , где п—любое целое число >3, т. е. п=, 4, 5 и т.д. , где п—любое целое число >3, т. е. п=, 4, 5 и т.д. | ||
А для ультрафиолетовой - Т. Лайман 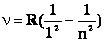 , где п—любое целое число >1, т. е. п=2,3, 4, 5 и т.д. , где п—любое целое число >1, т. е. п=2,3, 4, 5 и т.д. | ||
| Значения длин волн спектральных линий, вычисленных по этим формулам, совпадали с исключительной точностью со значениями длин волн этих линий, измеренных экспериментально. В конце XIX в. ученые обнаружили фундаментальную закономерность в микромире, которую в то время объяснить не смогли. Только через 30 лет Н. Бор дал физическую интерпретацию этой формулы. Он предположил, что два члена в формуле Бальмера представляют собой полные энергии разрешенных орбит электрона в атоме водорода. | ||
Преобразовав формулу Бальмера (умножив обе части на h), получим: 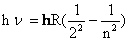 | 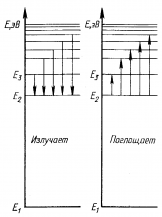 | |
Учитывая, что согласно гипотезе Планка энергия кванта Δ 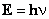 , получим: , получим: 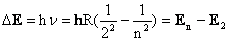 | ||
| Свои постулаты Н. Бор применил для построения теории атома водорода. | ||
26 Вопрос. Экспериментальное подтверждение постулатов Бора (опыты Франка и Герца).
| Опыт Франка и Герца | |
| Существование дискретных энергетических уровней атома подтверждается опытом Франка и Герца. Немецкие ученые Джеймс Франк и Густав Герц за экспериментальные исследования дискретности энергетических уровней получили Нобелевскую премию в 1925 г. В опытах использовалась трубка (рис. 6.9), заполненная парами ртути при давлении р ≈ 1 мм рт. ст. и три электрода: катод, сетка и анод. Электроны ускорялись разностью потенциалов U между катодом и сеткой. Эту разность потенциалов можно было изменять с помощью потенциометра П. Между сеткой и анодом тормозящее поле 0,5 В (метод задерживающих потенциалов). Определялась зависимость тока через гальванометр Г от разности потенциалов между катодом и сеткой U. В эксперименте была получена зависимость, изображенная на рис. 6.10. ЗдесьU = 4,86 В – соответствует первому потенциалу возбуждения Согласно боровской теории, каждый из атомов ртути может получить лишь вполне определенную энергию, переходя в одно из возбужденных состояний. Поэтому если в атомах действительно существуют стационарные состояния, то электроны, сталкиваясь с атомами ртути, должны терять энергию дискретно, определенными порциями, равными разности энергии соответствующих стационарных состояний атома. Из опыта следует, что при увеличении ускоряющего потенциала вплоть до 4,86 В анодный ток возрастает монотонно, его значение проходит через максимум (4,86 В), затем резко уменьшается и возрастает вновь. Дальнейшие максимумы наблюдаются при и . Ближайшим к основному, невозбужденному состоянию атома ртути является возбужденное состояние, отстоящее по шкале энергий на 4,86 В. Пока разность потенциалов между катодом и сеткой меньше 4,86 В, электроны, встречая на своем пути атомы ртути, испытывают с ними только упругие соударения. При = 4,86 эВ энергия электрона становится достаточной, чтобы вызвать неупругий удар, при котором электрон отдает атому ртути всю кинетическую энергию, возбуждая переход одного из электронов атома из нормального состояния в возбужденное. Электроны, потерявшие свою кинетическую энергию, уже не смогут преодолеть тормозящий потенциал и достигнуть анода. Этим и объясняется резкое падение анодного тока при = 4,86 эВ. При значениях энергии, кратных 4,86, электроны могут испытывать с атомами ртути 2, 3, … неупругих соударения. При этом они полностью теряют свою энергию и не достигают анода, т.е. наблюдается резкое падение анодного тока. Таким образом, опыт показал, что электроны передают свою энергию атомам ртути порциями, причем 4,86 эВ – наименьшая возможная порция, которая может быть поглощена атомом ртути в основном энергетическом состоянии. Следовательно, идея Бора о существовании в атомах стационарных состояний блестяще выдержала проверку экспериментом. Атомы ртути, получившие при соударении с электронами энергию , переходят в возбужденное состояние и должны вернуться в основное, излучая при этом, согласно второму постулату Бора, квант света с частотой . По известному значению можно вычислить длину волны светового кванта: . Таким образом, если теория верна, то атомы ртути, бомбардируемые электронами с энергией 4,86 эВ, должны являться источником ультрафиолетового излучения с , что действительно обнаружилось в опытах. Таким образом, опыты Франка и Герца экспериментально подтвердили не только первый, но и второй постулат Бора и сделали большой вклад в развитие атомной физики. |
