Распределение растворённого вещества между
Двумя несмешивающимися растворителями
Рассмотрим систему, состоящую из двух несмешивающихся жидкостей (фаза I и фаза II), находящихся в контакте друг с другом и третьего вещества растворимого и в одной, и в другой жидкости.
Третье вещество определённым образом распределяется между обеими фазами, и к моменту наступления равновесия устанавливаются определенные концентрации этого вещества в фазе I – cI, а в фазе II – cII.
Момент наступления равновесия характеризуется равенством химического потенциала третьего компонента в обеих фазах:
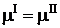
Подставляя выражения, описывающие зависимость химического потенциала от активности компонентов получим:
m0I + RT ln a I = m0II + RT ln aII
или:
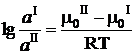
Поскольку все величины, стоящие в правой части уравнения являются постоянными (при постоянной температуре), левая часть уравнения также является постоянной и может быть обозначена ln k:
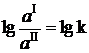
или:
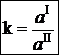
Полученное выражение получило название закон распределения, а k – константа или коэффициент распределения.
Значение коэффициента распределения зависит от природы обеих жидкостей, от природы растворенного вещества и от температуры и не зависит от концентрации растворенного вещества.
Если k>1, то это свидетельствует о преимущественной растворимости третьего вещества в растворителе I, если k<1, то соответственно в растворителе II.
Для разбавленных растворов вместо активностей можно использовать значения концентраций, тогда закон распределения принимает вид:
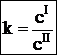
В приведенном виде закон распределения выполняется только в том случае, если в обеих фазах частицы растворенного вещества находятся в одинаковом состоянии. Однако в реальных системах могут происходить процессы диссоциации (распад на две, или большее количество частей) и ассоциации (объединение двух, или большего количества частиц). Эти процессы вносят существенные отклонения в закон распределения.
При необходимости учёта отклонений, вызванных процессами диссоциации и ассоциации используется уравнение Нернста - Шилова
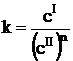 , (1)
, (1)
где n – постоянная (для данной системы) величина, учитывающая отклонения от закона распределения.
Если прологарифмировать уравнение Нернста – Шилова, то получим следующее соотношение:
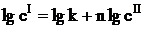 (2)
(2)
Таким образом, зависимость lg cI = f(lg cII) должна носить линейный характер, а тангенс угла наклона этой зависимости равен величине n.
Экстракция
Распределение растворенного вещества между двумя фазами используется для извлечения веществ из жидких и твердых растворов методом экстракции.
Экстракцией называется метод извлечения вещества из раствора, основанный на его преимущественной растворимости в другом растворителе – экстрагенте.
В качестве экстрагента выбирается растворитель, практически не смешивающийся с растворителем, в котором растворено экстрагируемое вещество, и хорошо растворяющий это вещество.
Высокая растворимость экстрагируемого вещества в экстрагенте позволяет использовать для экстракции гораздо меньшее количество экстрагента по сравнению с исходным раствором. Результатом экстракции является получение намного более концентрированного, по сравнению с исходным раствором, раствора экстрагируемого вещества в экстрагенте – экстракта.
Если исходный раствор содержит несколько растворённых веществ, из которых интерес представляет только одно, то, подбирая состав экстрагента, можно добиться извлечения из раствора только интересующего вещества.
Таким образом, экстракция является одним из наиболее универсальных и эффективных методов выделения, концентрирования и очистки веществ.
Экстракция производится путём перемешивания исходного раствора и экстрагента в течение времени, необходимого для установления в системе равновесия. После отстаивания жидкости разделяются.
Экстрагируемое вещество выделяется из концентрированного раствора в экстрагенте методом перегонки, либо другими методами. В некоторых случаях раствор экстрагируемого вещества используется в качестве готового продукта.
В пищевой и фармацевтической промышленности метод экстракции часто применяется для извлечения растворимых веществ из твёрдого материала растительного или животного происхождения. Так, например, одним из промышленных способов получения подсолнечного масла является его экстракция из семечек подсолнечника при помощи бензина, методом экстракции извлекается желатин из костей животных, экстракцией являются процессы заварки чая и кофе и др.
Применение различных растворителей позволяет извлекать из одного и того же сырья различные вещества. Так, например, водные и спиртовые экстракты лекарственных растений содержат наборы различных веществ и производят соответственно различное терапевтическое воздействие.
Скорость экстракции из твёрдых материалов определяется скоростью проникновения растворителя в твёрдую фазу (набухания) и скоростью диффузии экстрагируемого вещества из твёрдой фазы в жидкую. С целью повышения скоростей этих процессов, твёрдые материалы обычно предварительно измельчают и обрабатывают горячим экстрагентом или его парами с последующей их конденсацией. В некоторых случаях экстракция из твёрдых материалов требует достаточно длительного времени, например при приготовлении различного рода отваров.
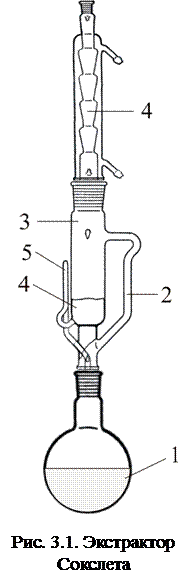 В лабораторной практике для проведения экстракции из твёрдых веществ используется экстрактор Сокслета (Рис. 3.1.). Экстрагент, помещённый в перегонную колбу 1, нагревается до кипения, его пары по трубке 2 поступают в экстракционный сосуд 3 и далее в обратный холодильник 4. В холодильнике происходит конденсация паров экстрагента, конденсат стекает в экстракционный сосуд и омывает твёрдое вещество 5, из которого производится экстракция (твёрдое вещество обычно помещают в бумажный или тканевой мешочек). Когда уровень экстракта достигает изгиба переливной трубки 5, раствор по сифону сбрасывается в перегонную колбу и процесс экстракции повторяется. Поскольку при кипении экстракта происходит испарение только экстрагента, в перегонной колбе происходит накопление экстрагируемого вещества.
В лабораторной практике для проведения экстракции из твёрдых веществ используется экстрактор Сокслета (Рис. 3.1.). Экстрагент, помещённый в перегонную колбу 1, нагревается до кипения, его пары по трубке 2 поступают в экстракционный сосуд 3 и далее в обратный холодильник 4. В холодильнике происходит конденсация паров экстрагента, конденсат стекает в экстракционный сосуд и омывает твёрдое вещество 5, из которого производится экстракция (твёрдое вещество обычно помещают в бумажный или тканевой мешочек). Когда уровень экстракта достигает изгиба переливной трубки 5, раствор по сифону сбрасывается в перегонную колбу и процесс экстракции повторяется. Поскольку при кипении экстракта происходит испарение только экстрагента, в перегонной колбе происходит накопление экстрагируемого вещества.
Метод экстракции находит также применение в аналитической химии.
Масса вещества, экстрагируемого путём однократной экстракции равно:
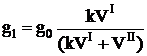
где g0 – исходная масса экстрагируемого вещества; VI – объём экстрагента;VII – объем раствора, из которого производится экстракция; k – коэффициент распределения.
Если экстракция проводится m раз одним и тем же объёмом экстрагента, то масса экстрагированного вещества может быть определена по формуле:
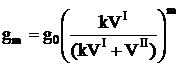
Титриметрический метод
Титриметрический метод является классическим методом химического анализа. Он используется для определения концентрации веществ в растворах.
Титруемым веществом называется вещество концентрацию которого необходимо определить.
Титриметрический метод основан на реакции взаимодействия титруемого вещества с титрантом.
Титрантомназывается вещество, способное вступать в реакцию с титруемым веществом.
Кислотно-основное титрование основано на реакции взаимодействия кислоты со щелочью:
H+ + OH– = H2O
При титровании раствора кислоты, титрантом служит раствор щелочи.
Прибавление раствора титранта производится до достижения точки эквивалентности.
Точкой эквивалентности называется момент, когда число молей (точнее число эквивалентов) титранта равняется числу молей титруемого вещества.
Обычно наступление точки эквивалентности не сопровождается видимыми изменениями. Возможность визуального фиксирования этой точки достигается путём добавки в титруемый раствор индикатора.
Индикаторомназывается вещество, изменяющее окраску в точке эквивалентности. При кислотно-основном титровании в качестве индикатора обычно используется фенолфталеин (при титровании кислоты щелочью) и метиловый оранжевый (при титровании щелочи кислотой).
Процесс титрования состоит из следующих стадий:
 1. Приготовление раствора титранта – вещества, взаимодействующего с веществом, содержащимся в исследуемом растворе. Концентрация раствора титранта равна c(2). Обычно раствор титранта готовится весовым способом: Рассчитанная и взятая на весах навеска вещества, помещается в мерную колбу определённого объёма и заливается при перемешивании дистиллированной водой. Объём раствора доводится до метки на мерной колбе. Растворы титранта готовятся также из фиксаналов – запаянных ампул, содержащих необходимую навеску вещества.
1. Приготовление раствора титранта – вещества, взаимодействующего с веществом, содержащимся в исследуемом растворе. Концентрация раствора титранта равна c(2). Обычно раствор титранта готовится весовым способом: Рассчитанная и взятая на весах навеска вещества, помещается в мерную колбу определённого объёма и заливается при перемешивании дистиллированной водой. Объём раствора доводится до метки на мерной колбе. Растворы титранта готовятся также из фиксаналов – запаянных ампул, содержащих необходимую навеску вещества.
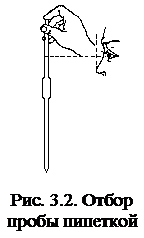
2. Отбор пробы исследуемого раствора с неизвестной концентрацией титруемого вещества – c(1) осуществляется при помощи мерной посуды (обычно пипетки). Объем пробы исследуемого раствора равен V(1).
