Расчет равновесного состава продуктов
Химической реакции
Зная величины констант равновесия при данных условиях и используя стехиометрические соотношения реакции (закон сохранения массы), рассчитывают равновесный состав продуктов по следующей схеме.
1. Пишут уравнение реакции.
2. Пишут под формулами уравнения начальные концентрации исходных веществ (в моль/л). Если начальные концентрации продуктов реакции не оговариваются в условии задачи, они обычно принимаются равными нулю.
А + b В « c С + D
Начальное
состояние [А]0 [В]0 [С]0 0
Число молей
по уравнению 1 b c 1
Изменение
концентраций x b x c x x
Равновесное
состояние [А]0 - x [В]0 – bx [С]0 + c x x
3. Принимают, что в ходе реакции до состояния равновесия прореагировало x моль/л какого-либо вещества. Обычно за x принимают изменение концентрации того реагента, стехиометрический коэффициент при котором в уравнении реакции наименьший, чтобы избежать дробных коэффициентов при неизвестном x. Например, прореагировало x моль/л вещества А.
4. По уравнению реакции определяют изменение концентраций других веществ.
5. Определяют равновесные концентрации веществ. При протекании реакции в прямом направлении до состояния равновесия происходит уменьшение концентраций исходных веществ и увеличение концентраций продуктов реакции.
6. Пишут выражение закона действующих масс. Подставляют в него найденные значения равновесных концентраций.
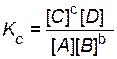 ,
,
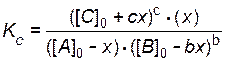 .
.
7. Решают уравнение с одним неизвестным. При этом учитывают, что отрицательный корень не имеет физического смысла, и убыль концентрации исходного вещества не может быть больше величины самой концентрации (начальная концентрация исходного вещества не может быть меньше его остаточной равновесной концентрации).
8. Находят равновесные концентрации.
[А] = [А]0- x;
[B] = [B]0 - b x;
[C] = [С]0 + cx;
[D] = x.
Приведенная схема расчета может быть применена также для определения исходных (начальных) молярных концентраций, если известны равновесные концентрации реагентов.
Смещение химического равновесия.
Принцип Ле Шателье
Истинное химическое равновесие является динамическим и подвижным: изменение внешних условий (температуры, давления, концентраций реагирующих веществ) ведет к смещению равновесия в сторону прямой или обратной реакции. Характер влияния внешних факторов на равновесные системы выражает принцип Ле Шателье.
Если на систему, находящуюся в состоянии равновесия, оказать внешнее воздействие, то смещение равновесия происходит в сторону той реакции (прямой или обратной), которая ослабляет эффект внешнего воздействия.
Изменение концентраций
Равновесное состояние в системе
H2 (г) + I2 (г) ®2 HI (г)
характеризуется (для одной и той же температуры) константой равновесия
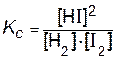 .
.
Если, например, в систему добавить водород, т.е. увеличить его концентрацию, то скорость прямой реакции увеличится (в соответствии с законом действующих масс)
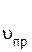 =
= 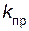 [H2] [I 2],
[H2] [I 2], 
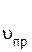 >
> 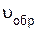 ,
,
равновесие сместится вправо. Концентрация йодоводорода будет увеличиваться, а концентрация водорода и йода будет уменьшаться. Процесс будет протекать до тех пор, пока не установится новое равновесие. Новые равновесные концентрации всех компонентов будут другими, но соотношение между ними, определяемое константой равновесия, останется постоянным.
Если в систему ввести дополнительное количество йодоводорода, то скорость обратной реакции увеличится
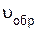 =
= 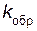 [HI] 2 ,
[HI] 2 , 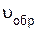 >
> 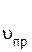 ,
,
равновесие сместится влево.
Удаление из системы продуктов (или продукта) реакции ведет к смещению равновесия в сторону прямой реакции, а уменьшение концентрации исходных (или исходного) веществ приводит к сдвигу равновесия в направлении обратной реакции.
Изменение давления
Повышение давления (уменьшение общего объема) вызывает смещение равновесия в направлении уменьшения общего количества молей газообразных веществ, т.е. в направлении, приводящем к понижению давления.
При уменьшении давления (увеличении общего объема) равновесие смещается в сторону увеличения количества молей газообразных веществ, т.е. в направлении, приводящем к возрастанию давления.
Рассмотрим, в каком направлении сместится равновесие в системе
CO (г) + Cl2 (г) « COCl2 (г),
если при неизменной температуре увеличить давление путем уменьшения объема газовой смеси?
В реакцию вступают 2 моля, а образуется 1 моль газообразных веществ. Прямая реакция при постоянном объеме сопровождается уменьшением давления. Если увеличить общее давление в системе, то согласно принципу Ле Шателье равновесие сместится в сторону прямой реакции.
Это можно доказать расчетами. Скорость прямой реакции равна

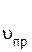 =
= 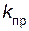 [СО][Сl2],
[СО][Сl2],
скорость обратной реакции равна
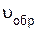 =
= 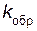 [COCl2].
[COCl2].
При повышении давления объем системы уменьшился, например, в 3 раза. Тогда концентрации всех реагентов увеличатся в 3 раза. При этом скорость прямой реакции увеличивается в 9 раз:
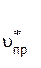 =
= 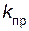 (3 [CO]) × (3 [Cl2]) =
(3 [CO]) × (3 [Cl2]) = 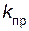 × 32 [CO][Cl2] = 9
× 32 [CO][Cl2] = 9 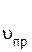 .
.
Скорость обратной реакции увеличивается только в 3 раза:
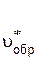 =
= 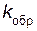 (3[СОCl2]) = 3
(3[СОCl2]) = 3 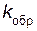 [СОCl2] = 3
[СОCl2] = 3 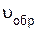 .
.
Таким образом, равновесие этой реакции будет смещаться в сторону накопления СОCl2 в системе до тех пор, пока не установится вновь состояние химического равновесия.
Для реакций, протекающих без изменения числа молей газообразных веществ, изменение давления (или общего объема) не влияет на химическое равновесие и равновесный состав продуктов.
Для реакции
H2 (г) + I2 (г) «2 HI (г)
количество молей газообразных веществ слева и справа от знака равновесия равно. При изменении давления скорости прямой и обратной реакций изменяются одинаково, а их отношение будет оставаться неизменным. В этом случае изменение давления не влияет на положение равновесия.
Рассмотрим влияние разбавления реагирующей смеси инертным газом на химическое равновесие.
1. Если разбавление ведется при постоянных давлении и температуре (изобарно-изотермический процесс), объем системы при накачивании инертного газа увеличивается (он пропорционален количеству вещества n газов, 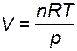 . Следовательно, молярные концентрации
. Следовательно, молярные концентрации 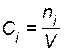 и парциальные давления
и парциальные давления 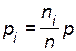 исходных веществ и продуктов реакции уменьшаются (
исходных веществ и продуктов реакции уменьшаются ( 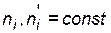 ;
; 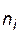 – число молей i - го исходного вещества,
– число молей i - го исходного вещества, 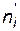 – число молей i - го продукта реакции). Создается эффект уменьшения общего давления, ведущий к смещению равновесия в соответствующем направлении.
– число молей i - го продукта реакции). Создается эффект уменьшения общего давления, ведущий к смещению равновесия в соответствующем направлении.
2. Если разбавление осуществляется при постоянных объеме и температуре (изохорно-изотермический процесс), то при накачивании инертного газа, например, в автоклав, общее давление возрастает пропорционально увеличению количества вещества газов в системе 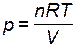 . При
. При 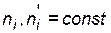 молярные концентрации
молярные концентрации 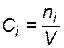 и парциальные давления
и парциальные давления 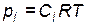
 исходных веществ и продуктов сохраняются постоянными. В этом случае разбавление инертным газом не влияет на химическое равновесие.
исходных веществ и продуктов сохраняются постоянными. В этом случае разбавление инертным газом не влияет на химическое равновесие.
Влияние температуры
Зависимость константы равновесия от температуры 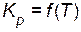 выражается уравнением
выражается уравнением
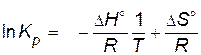 , или , или 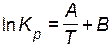 , , | (4.4) |
где 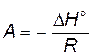 ;
; 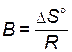 .
.
Выражение (4.4) представляет собой уравнение прямой в координатах 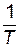 —
— 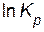 , тангенс угла наклона которой к оси абсцисс
, тангенс угла наклона которой к оси абсцисс 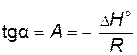 , а отрезок, отсекаемый на оси ординат,
, а отрезок, отсекаемый на оси ординат, 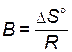 (рис. 11).
(рис. 11).
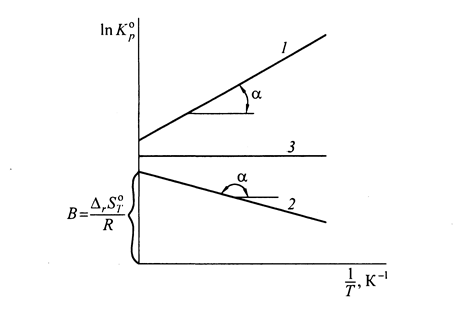
Рис. 11. Зависимость логарифма константы равновесия от обратной
абсолютной температуры для разных типов реакции:
1 – экзотермическая ( 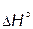 < 0); 2 – эндотермическая (
< 0); 2 – эндотермическая ( 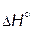 > 0);
> 0);
3 – реакция с нулевым тепловым эффектом ( 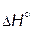 = 0)
= 0)
Для экзотермической реакции ( 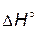 < 0,
< 0, 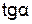 > 0) угол наклона прямой к оси абсцисс положителен, для эндотермических процессов (
> 0) угол наклона прямой к оси абсцисс положителен, для эндотермических процессов ( 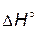 > 0,
> 0, 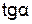 < 0) отрицателен, для реакций с нулевым тепловым эффектом (
< 0) отрицателен, для реакций с нулевым тепловым эффектом ( 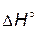 = 0,
= 0, 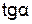 = 0) равен 0 (рис. 11, прямые 1, 2, 3 соответственно).
= 0) равен 0 (рис. 11, прямые 1, 2, 3 соответственно). 

1. Для экзотермических процессов 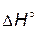 < 0 при увеличениии температуры значения
< 0 при увеличениии температуры значения 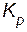 уменьшаются, что соответствует смещению равновесия в сторону обратной (эндотермической) реакции.
уменьшаются, что соответствует смещению равновесия в сторону обратной (эндотермической) реакции.
Например, для реакции синтеза аммиака из азота и водорода
N2(г) + 3H2 (г) 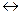 2NH3(г),
2NH3(г),
которая является экзотермической ( 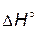 < 0), первое слагаемое в уравнении (4.4) будет положительным. С повышением температуры его абсолютная величина будет уменьшаться. Это приведет к уменьшению
< 0), первое слагаемое в уравнении (4.4) будет положительным. С повышением температуры его абсолютная величина будет уменьшаться. Это приведет к уменьшению 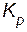 независимо от знака
независимо от знака 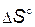 .
.
Уменьшение 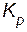 означает, что в выражении константы равновесия числитель (концентрации продуктов реакции) уменьшается, а знаменатель (концентрации исходных веществ) увеличивается.
означает, что в выражении константы равновесия числитель (концентрации продуктов реакции) уменьшается, а знаменатель (концентрации исходных веществ) увеличивается.
Равновесие смещается в сторону обратного эндотермического процесса разложения аммиака.
2. Для эндотермических процессов 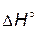 > 0 при увеличении температуры значения
> 0 при увеличении температуры значения 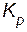 увеличиваются, что соответствует смещению равновесия в сторону прямой (экзотермической) реакции.
увеличиваются, что соответствует смещению равновесия в сторону прямой (экзотермической) реакции.
Например, в реакции
N2O4 (г) « 2 NO2 (г), 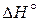 = 57,4 кДж.
= 57,4 кДж.
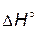 > 0, т.е. прямая реакция - эндотермическая. Следовательно, первое слагаемое в уравнении (4.4) отрицательно. При увеличении температуры его абсолютная величина уменьшается и независимо от знака
> 0, т.е. прямая реакция - эндотермическая. Следовательно, первое слагаемое в уравнении (4.4) отрицательно. При увеличении температуры его абсолютная величина уменьшается и независимо от знака 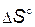 константа увеличивается.
константа увеличивается.
Увеличение 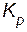 означает, что в выражении константы равновесия числитель (концентрации продуктов реакции) увеличивается, а знаменатель (концентрации исходных веществ) уменьшается. Равновесие смещается в сторону прямой реакции.
означает, что в выражении константы равновесия числитель (концентрации продуктов реакции) увеличивается, а знаменатель (концентрации исходных веществ) уменьшается. Равновесие смещается в сторону прямой реакции.
Зная знак 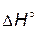 , можно сказать, в каком направлении будет изменяться константа равновесия при изменении температуры.
, можно сказать, в каком направлении будет изменяться константа равновесия при изменении температуры.
Повышение температуры приводит к смещению равновесия в направлении реакции, сопровождающейся поглощением теплоты и охлаждением системы, т.е. в сторону эндотермической реакции.
При понижении температуры равновесие смещается в сторону экзотермической реакции.
Цепные реакции
Цепные реакции – особый класс сложных многостадийных реакций, в которых появление промежуточной активной частицы (атома, содержащего неспаренный электрон, свободного радикала, иона) вызывает цепь превращений исходных веществ в продукты реакции.
К цепным реакциям относятся горение топлива, взрывы, окисление, хлорирование и бромирование соединений, реакции в атмосфере, полимеризация, крекинг нефтепродуктов, ядерные цепные реакции.
В сложном цепном процессе можно выделить следующие стадии:
1) инициирование (зарождение цепи), при котором образуются активные частицы - переносчики цепи;
2) рост цепи (продолжение цепи), активные частицы вступают в химическое взаимодействие с исходными веществами, в результате чего образуются новые активные частицы;
3) обрыв цепи – гибель активных частиц.
Зарождение цепи может происходить в результате диссоциации молекул под действием тепла, излучения или с помощью инициаторов – веществ, которые легко распадаются на свободные радикалы.
Свободным радикалом называется нестойкая частица, образующаяся из молекулы при разрыве одной или нескольких химических связей и обладающая одним или несколькими неспаренными электронами, которые обусловливают высокую химическую активность радикалов (H· , Cl·, Н3С· и др.).
Обрыв цепи может произойти в результате рекомбинации (образования ковалентной связи путем обобществления двух неспаренных электронов, принадлежащих разным частицам), взаимодействия активных частиц со стенками реакционного сосуда (для отвода избыточной энергии) или их взаимодействия со специальными веществами (замедлителями или ингибиторами).
Энергии активации отдельных стадий с участием активных частиц обычно во много раз меньше, чем энергии активации обычных молекулярных реакций, что способствует протеканию цепных реакций с большой скоростью.
