Процесс массообмена между фазами
Общие сведения
Различают два основных вида процессов массопередачи:
1) массообмен между жидкостью и газом (паром) или между двумя несмешивающимися жидкостями;
2)  массообмен между твердым телом и жидкостью, газом или паром (стр. 581).
массообмен между твердым телом и жидкостью, газом или паром (стр. 581).
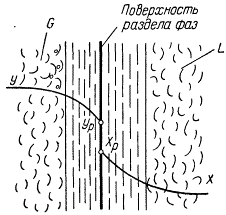
 Процесс переноса вещества из одной фазы в другую в первом случае можно представить следующим образом (рис. 1-3). Пусть концентрация распределяемого вещества в фазе G выше равновесной и вещество переходит из фазы G в фазу L. Распределяемое вещество в фазе G переносится к поверхности раздела фаз, а в фазе L переносится от этой поверхности. Перенос вещества в обеих фазах осуществляется путем молекулярной диффузии (т. е. диффузии молекул через слой носителя) и путем конвективной диффузии (т. е. движущимися частицами носителя и распределяемого вещества).
Процесс переноса вещества из одной фазы в другую в первом случае можно представить следующим образом (рис. 1-3). Пусть концентрация распределяемого вещества в фазе G выше равновесной и вещество переходит из фазы G в фазу L. Распределяемое вещество в фазе G переносится к поверхности раздела фаз, а в фазе L переносится от этой поверхности. Перенос вещества в обеих фазах осуществляется путем молекулярной диффузии (т. е. диффузии молекул через слой носителя) и путем конвективной диффузии (т. е. движущимися частицами носителя и распределяемого вещества).
В каждой фазе различают две области: ядро (основная масса) и пограничный слой, образующийся у поверхности раздела фаз. Перенос распределяемого вещества в ядре фазы, где обычно происходит интенсивное перемешивание, осуществляется преимущественно путем конвективной диффузии. Вследствие интенсивного перемешивания в ядре концентрация распределяемого вещества в каждом сечении системы почти постоянна.
Пограничный слой является областью резкого изменения концентрации распределяемого вещества. Перенос вещества в пограничном слое осуществляется путем конвективной и молекулярной диффузии, причем по мере приближения к поверхности раздела фаз происходит затухание конвективных потоков и возрастает роль молекулярной диффузии.
Концентрация распределяемого вещества в фазе G уменьшается от величины Y в ядре потока до величины Yр на границе раздела фаз. В фазе L концентрация распределяемого вещества уменьшается от величины Хр на границе раздела фаз до величины X в ядре потока. При установившемся процессе на границе раздела фаз наблюдается равновесие, т. е. концентрации Yр и Хр являются равновесными.
Молекулярная диффузия
При молекулярной диффузии, согласно закону Фика, количество диффундирующего через слой вещества пропорционально поверхности слоя F м2, изменению концентрации по толщине слоя Δсл. кг/м3, времени τ сек и обратно пропорционально толщине слоя δ м. Таким образом
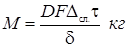 (1-23)
(1-23)
где D — коэффициент пропорциональности, называемый коэффициентом диффузии.
Уравнение (1-23) называется уравнением диффузии. Оно аналогично уравнению теплопроводности: разности температур соответствует разность концентраций Δсл., коэффициенту теплопроводности — коэффициент диффузии D.
Из уравнения (1-23) определяем размерность коэффициента диффузии:
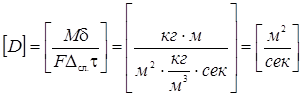
Коэффициент диффузии выражают также в м2/ч. Для пересчета величины коэффициента диффузии из м2/ч в м2/сек надо разделить данный коэффициент на 3600:
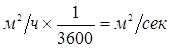
Коэффициент диффузии зависит от свойств диффундирующего компонента и среды, в которой происходит диффузия, а также от температуры и давления.
В справочных таблицах обычно приводятся коэффициенты диффузии D0 в газах при температуре Т0 = 273° К и абсолютном давлении Р0 = 1 ат. При других абсолютных температурах Т и других абсолютных давлениях Р этот коэффициент определяется по формуле
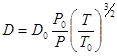 (1-24)
(1-24)
из которой видно, что коэффициент диффузии в газах обратно пропорционален давлению и прямо пропорционален абсолютной температуре в степени 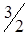 .
.
Для определения коэффициента диффузии газа А в газе В (или, что то же, газа В в газе А) при абсолютной температуре Т и абсолютном давлении Р ат можно пользоваться следующей зависимостью:
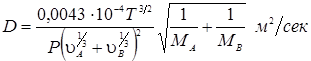 (1-25)
(1-25)
где υA и υB — молекулярные объемы газов А и В;
MA и МB — молекулярные массы газов А и В.
Молекулярные объемы определяются как сумма атомных объемов υ элементов, входящих в состав соединений. Значения υ приведены ниже:
| υ | |
| Водород……………………………………………………………………… | 3,7 |
| Кислород | |
| в метиловом эфире и сложных эфирах……………………………… | 9,1 |
| в высших эфирах……………………………………………………… | |
| в кислотах……………………………………………………………… | |
| в прочих соединениях………………………………………………… | 7,4 |
| Азот | |
| в первичных аминах………………………………………………….. | 10,5 |
| во вторичных аминах…………………………………………………. | |
| в прочих соединениях………………………………………………… | 15,6 |
| Углерод……………………………………………………………………….. | 14,8 |
| Сера…………………………………………………………………………… | 25,6 |
| Хлор…………………………………………………………………………... | 24,6 |
| Бром…………………………………………………………………………... | |
| Воздух………………………………………………………………………… | 29,9 |
| Бензольное кольцо (вычитать)……………………………………………… | |
| Нафталиновое кольцо (вычитать)…………………………………………... | |
| Водород (H2)……………………………………………………………….… | 14,3 |
Коэффициенты диффузии в жидкостях значительно меньше, чем в газах. Для приближенного определения коэффициентов диффузии в жидкостях при 20° С можно пользоваться формулой
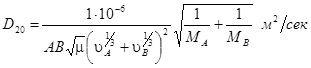 (1-26)
(1-26)
где μ — вязкость растворителя, спз;
А и В — поправочные коэффициенты для диффундирующего вещества и растворителя.
Поправочные коэффициенты характеризуют отклонение свойств вещества от свойств неассоциированных веществ, для которых этот коэффициент равен единице. Для газов поправочный коэффициент А = 1. Для воды В = 4,7, для метилового и этилового спирта В = 2, для ацетона В = 1,15.
Коэффициент диффузии в жидкости при данной температуре t находят по соотношению
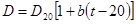 (1-27)
(1-27)
причем температурный коэффициент b определяют по формуле
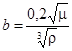
где μ — вязкость растворителя при 20° С, спз;
ρ — плотность растворителя, кг/м3.
Пример 1-7. Определить коэффициент диффузии паров бензола в воздухе при 40° С (313° К) и абсолютном давлении 1 ат.
Решение. Молекулярный объем для бензола (C6H6)
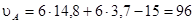
Молекулярный объем для воздуха υВ = 29,9; молекулярные массы компонентов: МA = 78 (для бензола), МВ = 29 (для воздуха). Подставляя все известные величины в формулу (1-25), получим:
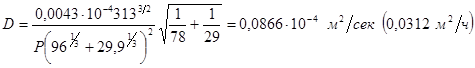
Пример 1-8. Определить коэффициент диффузии двуокиси углерода в воздухе при 25° С и абсолютном давлении Р = 20 ат
Решение. Коэффициент диффузии СО2 в воздухе при Р0 = 1 ат и T0 = 273° К равен D0 = 0,138·10-4 м2/сек (0,0497 м2/ч). По формуле (16-24)
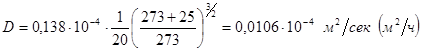
Пример 1-9. Определить коэффициент диффузии аммиака в воде при температуре 50° С.
Решение. Сначала определяем коэффициент диффузии при 20° С, подставляя в формулу (1-26) значения A = 1, В = 4,7, μ = 1 спз, υА = 15,6 + 3·3,7 = = 26,7 (для NH3); υB = 2·3,7 + 7,4 = 14,8 (для воды), MA = 17 (для NH3), Mв = 18 (для воды):
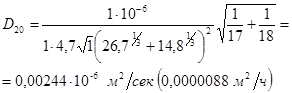
По формуле (1-27) при t = 50° С:
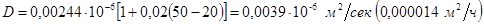
где 0,02 – температурный коэффициент b при μ = 1 спз и ρ = 1000 кг/м3.
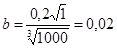
Конвективная диффузия
При конвективной диффузии количество вещества, переносимого в единицу времени из фазы, отдающей вещество, к поверхности раздела фаз (или от поверхности раздела фаз в фазу, воспринимающую это вещество), пропорционально поверхности F и разности концентраций Δчаст.распределяемого вещества в фазе и у поверхности раздела:
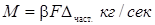 (1-28)
(1-28)
Разность концентраций Δчаст. является частной движущей силой процесса, коэффициент пропорциональности β называется коэффициентом массоотдачи.
Подобно тому как уравнения (1-17) и (1-23) аналогичны уравнениям теплопередачи и теплопроводности, уравнение (1-28) аналогично уравнению конвективного теплообмена: коэффициент массоотдачи является аналогом коэффициента теплоотдачи и учитывает перенос вещества путем молекулярной и конвективной диффузии.
В зависимости от единиц, принятых для выражения Δчаст.,коэффициент массоотдачи β имеет такие же размерности, как и коэффициент массопередачи К.
Коэффициент массоотдачи зависит от гидродинамических, физических и геометрических факторов и определяется экспериментальным путем с обработкой данных при помощи теории подобия.
Приложение теории подобия к процессам массопередачи показало, что эти процессы определяются кинематическим критерием Re и диффузионными критериями Nu' и Pr', являющимися аналогами тепловых критериев Nu и Pr. Значения диффузионных критериев приведены в табл. 1.1.
Таблица 1.1
| Критерий | Формула | Физический смысл критерия |
| Диффузионный критерий Нуссельта | 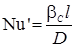 (1-29) (1-29) | Характеризует процесс массопередачи у поверхности раздела фаз |
| Диффузионный критерий Прандтля | 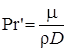 (1-30) (1-30) | Характеризует физические свойства среды |
Критерии подобия являются безразмерными, поэтому при вычислениях входящие в формулу критерия величины должны быть взяты в одинаковой системе единиц. При пользовании системой СИ все величины, входящие в формулы (1-29) и (1-30), берутся в следующих единицах:
βC — коэффициент массоотдачи, м/сек;
D — коэффициент диффузии, м2/сек;
μ — вязкость, н·сек/м2;
ρ — плотность, кг/м3;
l — определяющий геометрический размер, м.
При пользовании системой МКГСС величину μ берут в кгс·сек/м2, ρ — в кгс·сек2/м4. При этом за единицу времени для βC и D обычно принимают ч, тогда формула (1-30) принимает следующий вид:
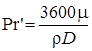
Критерии Re и Pr’ являются определяющими, критерий Nu’ — определяемым. Зависимость между критериями выражается в общем виде уравнением
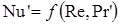 (16-31)
(16-31)
По найденному значению Nu’ вычисляют коэффициент массоотдачи при помощи формулы (1-29), из которой следует:
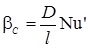 (16-32)
(16-32)
Пересчет βC в другие размерности коэффициента β производится аналогично пересчету коэффициента массопередачи по формулам (1-19) — (1-22).
Конкретные зависимости критерия Nu’ от Re и Pr’ будут приведены при рассмотрении отдельных процессов.
Подобие процессов массопередачи
Условия подобия процессов массопередачи можно вывести аналогично условиям теплового подобия. Обозначив через 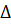 ' изменение концентрации по толщине пограничного слоя и через
' изменение концентрации по толщине пограничного слоя и через 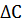 изменение концентрации по длине (высоте) аппарата, можно написать условие подобия для двух аппаратов (1 и 2) в следующем виде:
изменение концентрации по длине (высоте) аппарата, можно написать условие подобия для двух аппаратов (1 и 2) в следующем виде:
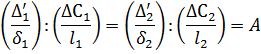
Здесь  представляет собой градиент концентрации по толщине пограничного слоя,
представляет собой градиент концентрации по толщине пограничного слоя, 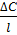 – градиент концентрации по длине (высоте) аппарата.
– градиент концентрации по длине (высоте) аппарата.
Объем фазы, проходящий через аппарат, в единицу времени, равен 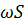 (
( 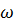 - скорость фазы, S- площадь сечения аппарата).Если концентрация фазы изменилась по длине (высоте) аппарата на
- скорость фазы, S- площадь сечения аппарата).Если концентрация фазы изменилась по длине (высоте) аппарата на 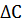 , то количество вещества, перешедшего в эту фазу, будет
, то количество вещества, перешедшего в эту фазу, будет 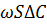 .Такое же количество вещества будет передается путем диффузии через пограничный слой и, согласно уравнению диффузии, составляет:
.Такое же количество вещества будет передается путем диффузии через пограничный слой и, согласно уравнению диффузии, составляет: 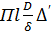 , где П- периметр пограничного слоя.Таким образом
, где П- периметр пограничного слоя.Таким образом
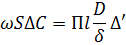
Заменяя  эквивалентным диаметром dэкв., получим:
эквивалентным диаметром dэкв., получим:
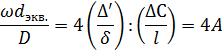
Таким образом, условием подобия процессов массопередачи является равенство отношения А или, что то же, равенство диффузионного критерия Пекле:
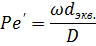
Диффузионный критерий Пекле Ре' характеризует отношение поперечного градиента концентрации (по толщине пограничного слоя) к продольному градиенту (по длине или высоте аппарата).
При практических расчетах критерий Пекле заменяют диффузионным критерием Прандтля:
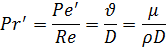
где 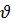 — кинематическая вязкость фазы.
— кинематическая вязкость фазы.
Условием подобия процессов массопередачи в двух аппаратах является равенство критериев Ре, а также критериев Рr'.
Количество вещества, передаваемого через пограничный слой, было определено как 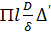 . Это же количество вещества, согласно уравнению мас-
. Это же количество вещества, согласно уравнению мас-
соотдачи (1-28), равно 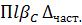 , где
, где 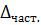 - движущая сила массоотдачи (разность концентраций у поверхности раздела фаз и в ядре фазы). Отсюда
- движущая сила массоотдачи (разность концентраций у поверхности раздела фаз и в ядре фазы). Отсюда
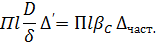
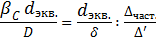
Правая часть этого уравнения для подобных систем одинакова. Следовательно, для них одинакова и левая часть, т. е. одинаков диффузионный критерий Нуссельта:
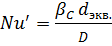
Связь коэффициента массопередачи и
коэффициентов массоотдачи
Рассмотрим переход вещества из фазы G в фазу L (см. рис. 1-3). Уравнение конвективного массообмена для фазы G:
Для фазы L: 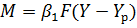 (1-33)
(1-33)
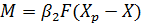 (1-34)
(1-34)
где 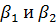 —коэффициенты массоотдачи для фаз G и L;
—коэффициенты массоотдачи для фаз G и L;
F— поверхность соприкосновения фаз.
Пусть линия равновесия представляет собой прямую с тангенсом угла наклона, равным k, т. е.
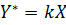
тогда на границе раздела фаз
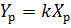
Таким образом, концентрации в фазе L можно выразить через концентрации в фазе G:
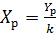 и
и 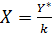
где Y* — концентрация в фазе G, равновесная с концентрацией X в ядре
фазы L.
Подставляя значения Хр и X в уравнение (1-34), получим:
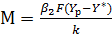 (1-35)
(1-35)
Определим из уравнений (1-33) и (1-35) движущую силу процесса:
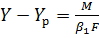 ;
; 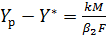
Складывая почленно эти уравнения, получим:
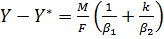 (1-36)
(1-36)
Уравнение массопередачи для рассматриваемого случая имеет следующий вид:
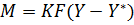
или 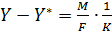 (1-37)
(1-37)
Приравнивая правые части уравнений (1-36) и (1-37), находим зависимость между коэффициентом массопередачи К и коэффициентами массоотдачи 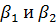 :
:
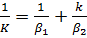 (1-38)
(1-38)
Уравнение (1-38) аналогично уравнению, устанавливающему связь между коэффициентом теплопередачи k и коэффициентами теплоотдачи 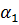 и
и 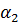 .
.
В уравнении (1-38) член 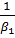 выражает сопротивление переходу вещества в фазе G, член
выражает сопротивление переходу вещества в фазе G, член 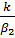 - сопротивление в фазе L.
- сопротивление в фазе L.
Если коэффициент 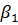 велик, то член
велик, то член 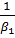 мал и, как видно из уравнения (1-38),
мал и, как видно из уравнения (1-38), 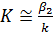 . В этом случае сопротивлением в фазе G можно пренебречь.
. В этом случае сопротивлением в фазе G можно пренебречь.
При большом коэффициенте 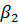 член
член 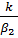 мал и, как видно из
мал и, как видно из
уравнения (1-38), 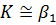 .В этом случае сопротивлением в фазе L можно
.В этом случае сопротивлением в фазе L можно
пренебречь.
Уравнение (1-38) выведено при условии линейной зависимости между равновесными концентрациями Y* и X. В случае отсутствия такой зависимости линия равновесия не будет прямой и в качестве k надо брать тангенс угла наклона касательной к линии равновесия в данной точке. При этом величины k и К будут изменяться по длине аппарата. При расчетах берут среднее значение k или же разделяют аппарат по длине на несколько участков, считая к постоянным в пределах каждого участка.
Массообмен с участием твердой фазы
В твердой фазе конвекция отсутствует и перенос вещества характеризуется уравнением массопроводности, аналогичным уравнению молекулярной диффузии:
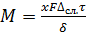 (1-39)
(1-39)
где х — коэффициент пропорциональности, имеющий размерность коэффициента диффузии и называемый коэффициентом массопроводности.
Если распределяемое вещество переносится из твердой фазы в омывающую ее жидкую, газовую или паровую фазу, то в пределах твердой фазы вещество перемещается вследствие массопроводности к границе раздела фаз и далее переносится в омывающую фазу путем конвективной диффузии.
Перемещение вещества вследствие массопроводности яв ляется неустановившимся процессом. В начальный момент концентрация вещества (Y1) одинакова во всем объеме твердого тела. В момент времени т средняя концентрация (Y) ниже начальной, причем распределение концентрации в твердом теле неравномерно — в центре концентрация больше, у границы раздела фаз — меньше. При 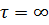 концентрация выравнивается и стремится к равновесной (Y*).
концентрация выравнивается и стремится к равновесной (Y*).
