Закон Бугера - Ламберта - Бэра
Поглощение света проявляется в ослаблении светового потока после прохождения через исследуемый объект, и оно тем больше, чем выше концентрация вещества. Согласно закона Бугера – Ламбера – Бэра, интенсивность света, прошедшего через слой поглощающего вещества толщины l, равна:
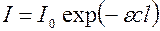 [1]
[1]
где Io - интенсивность падающего света,
c - концентрация поглощающего вещества ( в моль/л)
ε- молярный коэффициент поглощения (в л/моль*см)
В случае монохроматического света закон может быть выражен:
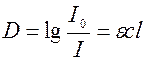 [2]
[2]
где D - называется оптической плотностью вещества.
где D - оптическая плотность; I0 и I - интенсивность падающего и вышедшего из образца пучка света соответственно; T - пропускание образца; С - концентрация поглощающего вещества, выраженная в моль/л; l - толщина образца, см; e - молярный коэффициент экстинкции, М-1×см-1.
Для определения концентрации вещества в растворе можно использовать следующие подходы.
1). Если заранее известно значение коэффициента молярной экстинкции при данной длине волны монохроматического света el (лучше всего в одном из главных максимумов поглощения) то, зная толщину поглощающего слоя кюветы (длину оптического пути l), которая обычно указывается на ее боковой стенке, можно рассчитать концентрацию исследуемого вещества по формуле:
С = D / e × l
Для многих веществ el хорошо известны и представляют собой табличные значения. Однако при использовании заранее известного значения el необходимо стараться точно воспроизвести условия, при которых оно было определено.
2). Если есть возможность приготовить стандартный раствор вещества с известной концентрацией (Сст) (взяв точную навеску), то можно определить концентрацию вещества в исследуемом растворе (Сх), не зная el.
3). Графический метод, основанный на построении калибровочного графика в координатах D и C. Для построения калибровочного графика измеряют поглощение серии растворов данного вещества с известной концентрацией. Получаемый график обычно представляет собой прямую линию, тангенс угла наклона ( tga ) которой равен el × l (при l = 1 см tga = el). Измерив D исследуемого раствора, можно по калибровочному графику определить концентрацию вещества.
4). С помощью абсорбционного анализа можно одновременно определять концентрацию нескольких веществ в растворе при условии, что спектры их поглощения различаются по форме. Если компоненты смеси не взаимодействуют между собой, то измеряемая оптическая плотность будет представлять сумму оптических плотностей компонентов (поскольку D есть величина аддитивная).
Закон Бугера-Ламберта-Бера выполняется не всегда. Зависимость D от С может по разным причинам отклоняться от линейной. Количественное определение вещества по результатам измерения спектров поглощения можно проводить в том случае, если выполняются следующие требования:
1) измеряющий световой пучок является монохроматическим;
2) поглощающие молекулы распределены по всему объему образца равномерно;
3) поглощающие молекулы в пределах исследуемых концентраций не изменяют характера взаимодействия друг с другом и молекулами среды (e = соnst для данной длины волны);
4) выходящий световой поток ослабляется только за счет поглощения фотонов (светорассеяние, отражение, люминесценция и другие явления не влияют на регистрируемый световой поток);
5) интенсивность измеряющего светового пучка и время жизни поглощающих молекул в возбужденном состоянии таковы, что концентрация невозбужденных (способных поглощать свет) молекул не изменяется в ходе измерения;
6) измеряющий световой пучок не вызывает фотохимических превращений поглощающих молекул.
В случае отклонений от закона Бугера-Ламберта-Бера нужно строить градуировочные графики, связывающие наблюдаемые величины оптической плотности и известные концентрации, и путём графической интероляции находить концентрации исследуемых растворов.
При количественном спектрофотометрическом анализе главная задача исследователя – измерить концентрации, а значит, и оптические плотности растворов с большей возможной точностью. Ошибка измерения оптической плотности в сильной мере зависит от самой величины измеряемой оптической плотности
