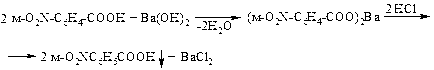Химические методы разделения смеси веществ и их очистки
Нередко разделение смеси веществ производят методами, основанными на различии в химических свойствах: по кислотно-основному характеру, по способности одного из соединений образовывать кристаллическое производное, которое вновь может быть превращено в исходное соединение и т.д. Если для разделения смеси можно применить химический метод, то его предпочитают, так как он позволяет быстрее и лучше разделить смесь.
Применяя химические методы разделения, необходимо помнить, что соединения, молекулы которых образованы только ковалентными связями, как правило, лучше растворяются в органических растворителях, причем мало полярные вещества растворяются в неполярных растворителях, полярные – в полярных.
Соединения, в молекулах которых имеются ионные связи, хорошо растворимы в воде. Например, органические кислоты и основания (амины) в большинстве своем плохо растворимы в воде, но хорошо в органических растворителях, а их соли, состоящие из катиона и аниона, хорошо растворяются в воде. Этим свойством пользуются при химических методах разделения, если смесь состоит: 1) из нейтрального вещества и кислоты; 2) из нейтрального вещества и основания (амина); 3) из кислоты и основания. При этом кислоты и амины действием щелочи или минеральной кислоты соответственно переводят в соль – ионное соединение, растворимое в воде, а нейтральное соединение в воде не растворимо. Его отделяют, а кислоту или амин из водного раствора выделяют в свободном виде, действуя сильной кислотой или щелочью соответственно. Рассмотрим насколько примеров.
9.1. Разделение смеси бромистого бутила и бутилового спирта
Бромистый бутил – соединение нейтральное; бутиловый спирт имеет амфотерный характер, т.е. проявляет свойства очень слабой кислоты и слабого основания. Поэтому смесь встряхивают в делительной воронке с концентрированной серной кислотой, с которой спирт дает соль оксония, а затем алкилсерную кислоту:
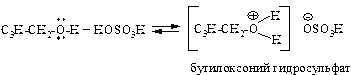
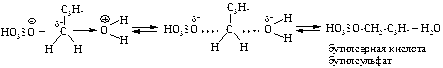
Бутилсульфат растворим в серной кислоте, а бромистый бутил нерастворим и после отстаивания остается в виде органического слоя, который отделяют. Если раствор бутилсульфата в серной кислоте разбавить водой, то приведенное выше равновесие сместится в сторону исходных продуктов: бутанола и раствора серной кислоты. При этом бутанол также выделится в виде органического слоя, который отделяют.
9.2. Разделение смеси нейтрального соединения и кислоты (например, фенетола и фенола)
Фенол слабо растворим в воде, а фенетол практически не растворим в воде. Фенетол – нейтральное соединение, а фенол является слабой кислотой. Для их разделения эфирный раствор смеси встряхивают в делительной воронке с 10%-ным раствором щелочи, в результате чего фенол превращается в фенолят-ионное соединение и переходит в водный раствор:
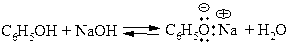
Эфирный раствор фенетола отделяют от водного слоя, промывают от щелочи водой, высушивают, отгоняют эфир и очищают фенетол перегонкой.
Из водного раствора фенол выделяют подкислением разбавленной серной или соляной кислотой:
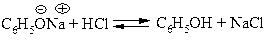
Так как фенол немного растворим в воде, его извлекают эфиром, эфирный экстракт высушивают, отгоняют, а фенол также перегоняют.
Таким же образом отделяют галогенарены от фенолов.
9.3. Разделение смеси нейтрального соединения и основания (например, нитробензола и анилина)
Для разделения смесь встряхивают в делительной воронке с 10%-ной соляной кислотой, при этом амин, образуя соль - ионное соединение, переходит в водный раствор:

Нитросоединение в воде не растворимо, остается в виде органического слоя, его отделяют, промывают водой от кислоты, затем раствором соды, высушивают и перегоняют.
Амин выделяют из водного раствора его соли подщелачиванием 30%-ным раствором NaOH. Выделившийся органический слой отделяют, водный слой два раза экстрагируют эфиром, соединяют с амином, промывают водой, высушивают твердой щелочью, эфир отгоняют, амин очищают перегонкой.
9.4.Разделение смеси кислоты или основания с нейтральным веществом с помощью перегонки с паром
Нередко реакционная смесь, кроме веществ кислотного, основного и нейтрального характера, содержит еще смолистые вещества и много неорганических солей. Тогда продукты реакции не удается разделить с помощью экстракции в делительной воронке. В этом случае применяют перегонку с паром из кислой или из щелочной среды.
Известно, что с паром перегоняются вещества, молекулы которых образованы ковалентными связями; ионные соединения, растворимые в воде, с паром не перегоняются. Если реакционная смесь содержит основание и нейтральное соединение (например, анилин и нитробензол), то к смеси перед перегонкой с паром прибавляют минеральную кислоту до сильно-кислой реакции (рН 2-3). При этом амин превращается в соль - ионное соединение, которое с паром не летит. Нитробензол отгоняют с паром, отделяют от воды, высушивают и перегоняют.
К кислому раствору, из которого отогнан нитробензол, прибавляют 40%-ный раствор щелочи до рН 8 и отгоняют с паром анилин.
Аналогично разделяют галогенарены, амины и фенолы.
9.5.Выделение и очистка веществ через их кристаллические производные
Другой принцип, на котором основываются химические методы разделения, заключается в том, что одно из соединений, составляющих смесь, переводят в кристаллическое производное, которое отделяют и из которого затем легко регенерируется исходное соединение. Такие кристаллические производные образуют альдегиды, амины, кислоты.
1. Альдегиды с NaHSO3 образуют кристаллическое бисульфитное производное, которое после отделения от жидких веществ фильтрованием переводят действием кислоты в альдегид:
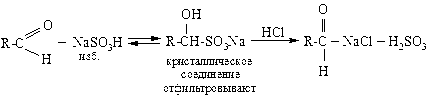
2. Амины первичные и вторичные с ангидридами и хлорангидридами кислот образуют кристаллические алкилированные амиды кислот (или ацильные производные аминов), гидролизируемые водой в присутствии кислоты или щелочи в исходные соединения:
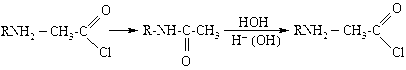
Кристаллы N - алкиламида отфильтровывают, а затем гидролизуют.
3. Альдегиды с первичными аминами образуют основания Шиффа – алкилиденамины, которые часто представляют собой кристаллические вещества:
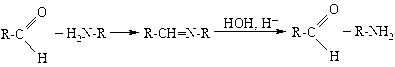
Эту реакцию можно использовать для выделения из смеси как альдегидов, так и аминов.
4. Некоторые кислоты с гидроксидами щелочно-земельных металлов образуют соли, плохо растворимые в воде. Твердую соль отфильтровывают, а затем действием минеральной кислоты при нагревании выделяют органическую кислоту.