Что такое идеально-газовая температура?
Недостатком шкал измерения температур, является то, что для разных термометрических веществ показания термометров совпадают только в выбранных реперных точках (для шкалы по Цельсию – при 0 и 100˚). Во всех остальных точках показания термометров будут разные. Эта неоднозначность устраняется, если в качестве термометрического вещества использовать достаточно разреженные газы, которые по своим свойствам близки к идеальному газу.
Идеальная газовая шкала температур (шкала Кельвина) – шкала, установленная на основании уравнения Клапейрона–Менделеева. В качестве термометрического тела берется идеальный газ, а в качестве температурного параметра – произведение давления на объем. Шкала, по которой отсчет температуры ведется от абсолютного нуля (Т = –273,16 °С), называется идеально-газовой абсолютной шкалой.
Идеально-газовая температура – это температура, отсчитываемая по газовому термометру, наполненному сильно разреженным газом.
Что такое постоянная Больцмана? Как связаны давление и концентрация идеального газа?
Постоянная Больцмана (k) — физическая постоянная, определяющая связь между средней энергией теплового движения молекулы и абсолютной температурой. (между энергией и температурой.)
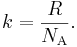
k = 1,38 x 10–23 Дж/К.
Уравнение состояния идеального газа - формула, устанавливающая зависимость между давлением, молярным объёмом и абсолютной температурой идеального газа
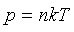
Какой вид имеет основное уравнение молекулярно-кинетической теории идеального газа?
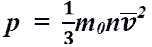 основное уравнение МКТ идеального газа. Выведено в предположении, что давление газа есть результат ударов его молекул о стенки сосуда. (масса одной молекулы, концентрация, средняя скорость молекул)
основное уравнение МКТ идеального газа. Выведено в предположении, что давление газа есть результат ударов его молекул о стенки сосуда. (масса одной молекулы, концентрация, средняя скорость молекул)
Это же уравнение в другой записи:
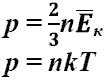
Что такое парциальное давление? Сформулируйте закон Дальтона.
Парциальное давление — давление отдельно взятого компонента газовой смеси.
Закон Дальтона — общее давление смеси газов равно сумме парциальных давлений каждого газа в отдельности.
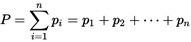
Какой вид имеет термическое уравнение состояния для смеси идеальных газов?
Из закона Дальтона:
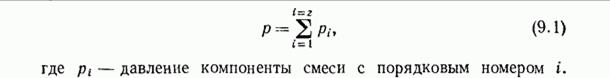

Напишите уравнение изобарного процесса для идеального газа. Закон Гей-Люссака.
Относительное изменение объёма данной массы газа при неизменном давлении P пропорционально изменению температуры
 где V0 – объем газа при температуре 0 °С. Коэффициент α равен (1/273,15) К–1. Его называют температурным коэффициентом объемного расширения газов.
где V0 – объем газа при температуре 0 °С. Коэффициент α равен (1/273,15) К–1. Его называют температурным коэффициентом объемного расширения газов.
Напишите уравнение изохорного процесса для идеального газа. Закон Шарля.
Описывает соотношение давления и температуры для идеального газа при постоянном объёме. P/T = const
Уравнение изохорного процесса может быть записано в виде:
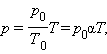 где p0 – давление газа при T = T0 = 273,15 К (т. е. при температуре 0 °С). Коэффициент α, равный (1/273,15) К–1, называют температурным коэффициентом давления.
где p0 – давление газа при T = T0 = 273,15 К (т. е. при температуре 0 °С). Коэффициент α, равный (1/273,15) К–1, называют температурным коэффициентом давления.
