Теоретические основы массопередачи.
В массообмене участвуют 3 вещества:
1.Распределяющее-фаза. Фу (y-пар, газ)
2.Распределяющая - фаза Фх (х-жидкость, тв.тело)
3. Распределяющее вещество М – вещество, которое переходит из одной фазы в другую.
Особенности массообменных процессов.
1.Процесс происходит при непосредственном контакте фаз.
2.Процесс обратимый.
3.В процессе ректификации фазы Фх и Фу обмениваются компонентами, а во всех остальных массообменных процессах фазы Фх и Фу являются инертными носителями.
Способы выражения состава фаз.
1. Фх - жидкая или твердая фаза
2. Фу - паровая или газовая фаза
3.А, В, С,….N- компоненты системы
4.gа, gв, gс,…gN – массы компонентов фазы Фх, кг
5.gа, gв, gс,…gN- массы компонентов фазы Фу, кг
6. Ма, Мв, Мс,…МN-молекулярные массы компонентов
7. Ра, Рв, Рс,… РN-упругости паров чистых компонентов
8. Ра, Рв, Рс,…РN-парциальные давления компонентов
9. Робщ- общее давление
Диффундирующее в пределах фазы вещество перемещается от точки с большей концентрацией к точке с меньшей концентрацией, и в расчетах движущую силу процессов массопереноса выражают приближенно через разность концентраций, подобно тому, как в процессах теплопереноса её выражают разностью температур.
Обычно количественный состав фаз выражают:
1.а – массовые проценты- % мас, в Фх
в– массовые проценты- % мас, в Фу
а i = 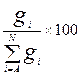
 в i=
в i= 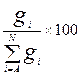

2.Массовые доли: кг/кг
 = а i /100 - в фазе Фх
= а i /100 - в фазе Фх  = в i/100 - в фазе Фу
= в i/100 - в фазе Фу
3.Мольные доли: кмоль/кмоль
xi = 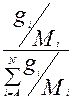 yi =
yi = 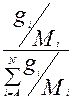
4.Относительные мольные доли :
X- 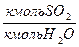 - в Фх Y-
- в Фх Y- 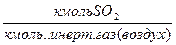 -в Фу
-в Фу
5.Относительные массовые доли:
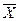 -
- 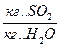 - в Фх
- в Фх 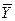 -
- 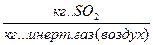 -в Фу
-в Фу
6.Объемная мольная концентрация:
Сх- 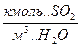 Сy -
Сy - 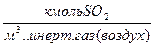
7.Объемная массовая концентрация
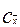 -
- 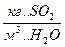 - в Фх
- в Фх 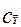 -
- 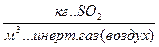
8.Состав газовых смесей часто выражают через парциальные давления компонентов.
Равновесие между фазами.
Процесс перехода вещества из одной фазы в другую (например, из газовой в жидкость) происходит до установления динамического равновесия.
Скорость перехода вещества из газа в жидкость прямо пропорциональна его концентрации:
w=my y
Скорость обратного процесса:
w=mx x
При достижении динамического равновесия скорости выравниваются:
my y=mx x
Уравнение равновесия:
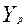 =
= 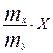 =myx X
=myx X
yp= y* - равновесная концентрация
myx - константа фазового равновесия ( коэффициент распределения)
Графическое изображение линий равновесия
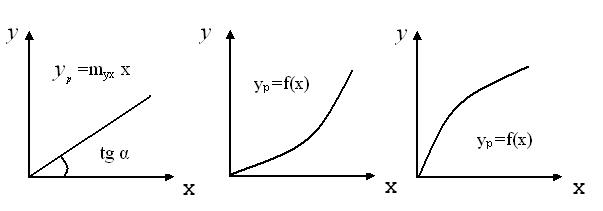
Идеальный случай Реальный Реальный
mx x =tg α Абсорбция Ректификация,
абсорбция экстракция
Если концентрации фаз выражены в одной и той же размерности, то «m» величина безразмерная, если нет, то будет иметь соответствующую размерность
Уравнение равновесия необходимо для определения направления протекания процесса и движущей силы.
Материальный баланс
Разберем на процессе абсорбции.
Пример: Пусть идет поглощение SO2 из воздуха водой. Рассмотрим схему движения потоков в противоточном аппарате.
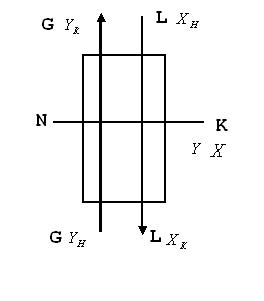
В аппарат поступают фазы G и L.
Расход фазы G является постоянным – это количество газовой инертной фазы (воздух), кмоль/с. L- жидкостная фаза (вода), расход постоянный, кмоль/с.
YН, YК, XН, XК –концентрация SO2 в газе и жидкости на входе и выходе из аппарата.
Дано: G, YН, YК, XН=0, XК
Определить: расход жидкости L и количество абсорбированного вещества M.
Запишем уравнение материального баланса по поглощаемому веществу для сечения N-K, в котором текущие концентрации составляют Y и X.
-GdY= LdX=dM
-GdY- баланс по поглощаемому компоненту, знак (-) означает, что концентрация вещества в газовой фазе уменьшается.
Какая получается размерность:
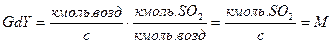
Запишите: интегрируем всегда по ходу газа, по ходу жидкости
- 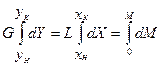 и получим:
и получим:
M=G (YН - YК) =L (XК - XН )
Из этого уравнения получим соотношения между массовыми потоками распределяющих фаз
G= L 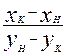 L= G
L= G 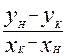
Удельный расход абсорбента найдем из соотношения:
l =L/G = 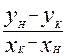
Уравнение рабочей линии
1ый случай- противоток.
Запишем уравнение материального баланса по поглощаемому компоненту по ходу газа до произвольно выбранного сечения N-K.
-GdY= LdX проинтегрируем:
- 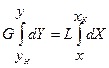 и получим:
и получим:
G (YН - Y) =L (XК – X )
Решим это уравнение относительно Y:
Y= YН –L/G(XК – X ) = YН – l (XК – X )
Это уравнение рабочей линии для противотока, отображающее изменение рабочих концентраций в произвольном сечении аппарата N-K.
Уравнение рабочей линии имеет вид:
Y= Ax +B
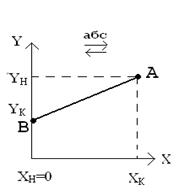 Графическое изображение рабочей линии.
Графическое изображение рабочей линии.
Как видно из уравнения рабочей линии, на диаграмме в координатах X-Y, рабочая линия представляет собой прямую с наклоном к оси абсцисс под углом , тангенс которого равен l .
т.А с координатами YН ,XК . т.В (XН,YК)
2ой случай – прямоток:

Запишем уравнение материального баланса по поглощаемому компоненту от входа до сечения N-K
-GdY= LdX
- 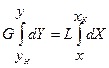
G (YН - Y) =L (XК – X )
Y = YН – l (XК – X )
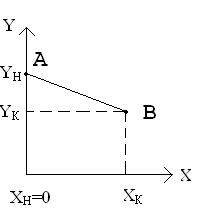
т.А (YН, XН) т.В (YК, XК)
Точки, лежащие на рабочей линии, отражают рабочие концентрации, лежащие на равновесной линии - равновесные концентрации.
