Распределение электронов в атоме по состояниям
 Если частицы имеют одинаковые квантовые числа, то их вол- новая функция симметрична относи- тельно перестановки частиц. Отсюда следует, что два одинаковых фермиона, входящих в одну систему, не могут на- ходиться в одинаковых состояниях, так как для
Если частицы имеют одинаковые квантовые числа, то их вол- новая функция симметрична относи- тельно перестановки частиц. Отсюда следует, что два одинаковых фермиона, входящих в одну систему, не могут на- ходиться в одинаковых состояниях, так как для 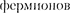 волновая функция должна быть антисимметричной. Обоб- щая опытные данные, В. Паули сформу- лировал принцип, согласно которому системы фермионов встречаются в природетолько состояниях, описыва- емых антисимметричными волновыми функциями
волновая функция должна быть антисимметричной. Обоб- щая опытные данные, В. Паули сформу- лировал принцип, согласно которому системы фермионов встречаются в природетолько состояниях, описыва- емых антисимметричными волновыми функциями 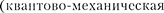 формулировка принципа Паули).
формулировка принципа Паули).


 Из этого положения вытекает более простая формулировка принципа Пау- ли, которая и была введена им в кван- товую теорию (1925) еще до утвержде- ния квантовой механики: в системе оди- наковых
Из этого положения вытекает более простая формулировка принципа Пау- ли, которая и была введена им в кван- товую теорию (1925) еще до утвержде- ния квантовой механики: в системе оди- наковых 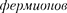 любые два из нихне могутодновременнонаходиться одном томжесостоянии. Отметим, что чис- ло однотипных бозонов, находящихся в одном и том же состоянии, лими-
любые два из нихне могутодновременнонаходиться одном томжесостоянии. Отметим, что чис- ло однотипных бозонов, находящихся в одном и том же состоянии, лими-
тируется.
Напомним, что состояние электро- на в атоме однозначно определяется набором четырех квантовых чисел:
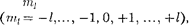 главного п
главного п 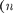 = 1, 2, 3,...), орбитального
= 1, 2, 3,...), орбитального 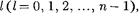 магнитного
магнитного
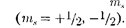 магнитного спинового
магнитного спинового
 Распределение электронов в атоме подчиняется принципу Паули, кото- рый может быть использован в его про- стейшей формулировке: в одном и том атоме неможет быть более одного
Распределение электронов в атоме подчиняется принципу Паули, кото- рый может быть использован в его про- стейшей формулировке: в одном и том атоме неможет быть более одного
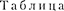

| Главное квантовое число п | |||||||||||||||
| Символ оболочки | К | L | м | N | О | ||||||||||
| Максимальное число электронов в оболочке | |||||||||||||||
Орбитальное квантовое 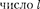 | |||||||||||||||
Символ 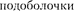 | 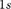 | 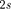 | 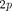 | 3 s | 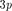 | 3d | 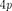 | Ad | 4/ | 5s | 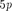 | 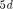 | 5/ | 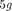 | |
Максимальное число электронов в 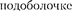 |  |  |  |  |
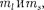 электронасодинаковымнаборомчеты- рех квантовых чисел п,
электронасодинаковымнаборомчеты- рех квантовых чисел п, 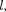 т.е.
т.е.
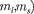
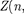 /, = 0 или
/, = 0 или 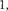
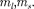 где
где 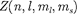 — число электронов, находящихся в квантовом состоянии, описываемом набором четырех кванто- вых чисел: п, /,
— число электронов, находящихся в квантовом состоянии, описываемом набором четырех кванто- вых чисел: п, /,
Таким образом, принцип Паули ут- верждает, что два электрона, связанные в одном и том же атоме, различаются значениями по крайней мере одного квантового числа.
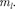

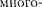
 Согласно формуле (223.8), данному п соответствует п2различных состояний, отличающихся значениями / и Кван- товое число может принимать лишь два значения Поэтому макси- мальное число электронов, находящих- ся в состояниях, определяемых данным главным квантовым числом, равно
Согласно формуле (223.8), данному п соответствует п2различных состояний, отличающихся значениями / и Кван- товое число может принимать лишь два значения Поэтому макси- мальное число электронов, находящих- ся в состояниях, определяемых данным главным квантовым числом, равно
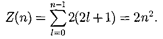 |
Совокупность электронов в электронном атоме, имеющих одно и то же главное квантовое число п, называ- ют электронной оболочкой. В каждой из оболочек электроны распределяют- ся по соответствующим данному Поскольку орбитальное квантовое число принимает значения
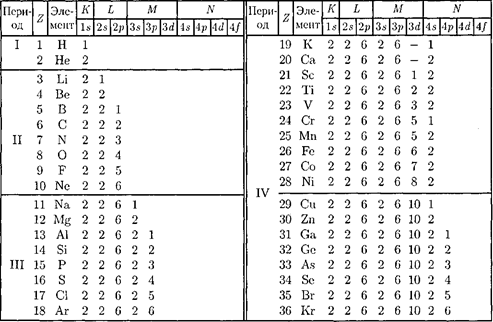
от 0 до п — 1, число 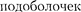 равно порядковому номеру п оболочки. Коли- чество электронов в гюдоболочке опре- деляется магнитным и магнитным спи- новым квантовыми числами: макси- мальное число электронов в подоболоч- ке с данным /равно 2(2/ + 1). Обозна- чения оболочек, а также распределение электронов по оболочкам и подоболоч- кам
равно порядковому номеру п оболочки. Коли- чество электронов в гюдоболочке опре- деляется магнитным и магнитным спи- новым квантовыми числами: макси- мальное число электронов в подоболоч- ке с данным /равно 2(2/ + 1). Обозна- чения оболочек, а также распределение электронов по оболочкам и подоболоч- кам 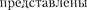 в табл.
в табл. 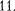
§ 228. Периодическая система элементов Менделеева
Принцип Паули лежит в основе си- стематики заполнения электронных со- стояний в атомах и позволяет объяс- нить Периодическую систему эле- ментов Д.И.Менделеева (1869) — фундаментальный закон природы, яв- ляющийся основой современной хи- мии, атомной и ядерной физики.
Д.И.Менделеев ввел понятие по- рядкового номера Z химического эле- мента, равного числу протонов в ядре и соответственно равного общему числу электронов в электронной оболочке атома. Расположив химические элемен- ты по мере возрастания порядковых но- меров, он получил периодичность в из- менении химических свойств элемен- тов. Однако для известных в то время
64 химических элементов некоторые клетки таблицы оказались незаполнен- ными, так как соответствующие им эле- менты (например, Ga, Se, Ge) тогда еще не были известны. Д.  Менделеев, та- ким образом, не только правильно рас- положил известные элементы, но и предсказал существование новых, еще не открытых элементов и их основные свойства. Кроме того, ему удалось уточ- нить атомные веса некоторых элемен- тов. Например, атомные веса
Менделеев, та- ким образом, не только правильно рас- положил известные элементы, но и предсказал существование новых, еще не открытых элементов и их основные свойства. Кроме того, ему удалось уточ- нить атомные веса некоторых элемен- тов. Например, атомные веса 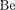 и U, вычисленные на основе таблицы Мен- делеева, оказались правильными, а по- лученные ранее экспериментально — ошибочными.
и U, вычисленные на основе таблицы Мен- делеева, оказались правильными, а по- лученные ранее экспериментально — ошибочными.
Так как химические и некоторые физические свойства элементов опреде- ляются внешними (валентными) элек- тронами в атомах, то периодичность свойств химических элементов должна быть связана с определенной периодич- ностью в расположении электронов в
атомах. Поэтому для объяснения табли- цы будем считать, что каждый последу- ющий элемент образован из предыду- щего 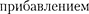 к ядру одного про- тона и соответственно прибавлением одного электрона в электронной обо- лочке атома. Взаимодействием электро- нов пренебрегаем, внося, где это необ- ходимо, соответствующие поправки. Рассмотрим атомы химических элемен- тов, находящиеся в основном состоя- нии.
к ядру одного про- тона и соответственно прибавлением одного электрона в электронной обо- лочке атома. Взаимодействием электро- нов пренебрегаем, внося, где это необ- ходимо, соответствующие поправки. Рассмотрим атомы химических элемен- тов, находящиеся в основном состоя- нии.
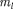
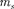 Единственный электрон атома водо- рода находится в состоянии
Единственный электрон атома водо- рода находится в состоянии 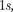 харак- теризуемом квантовыми числами п — 1,
харак- теризуемом квантовыми числами п — 1, 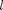 = 0, — О и —
= 0, — О и — 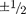 (ориентация его спина произвольна). Оба электро- на атома Не находятся в состоянии
(ориентация его спина произвольна). Оба электро- на атома Не находятся в состоянии 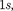 но с антипараллелыюй ориентацией спина. Электронная конфигурация для атома Не записывается как
но с антипараллелыюй ориентацией спина. Электронная конфигурация для атома Не записывается как 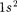 (два
(два
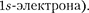 На атоме Не заканчива-
На атоме Не заканчива-
ется заполнение 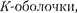 что соот-
что соот-
 |
 12
12ветствует завершению I периода Пери- одической системы элементов Менде- леева (табл. 12).
Третий электрон атома Li (Z= 3), со- гласно принципу Паули, уже не может разместиться в целиком заполненной
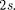
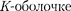 и занимает наинизшее энер- гетическое состояние с в = 2
и занимает наинизшее энер- гетическое состояние с в = 2 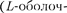 ка), т. е.
ка), т. е. 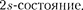 Электронная кон- фигурация для атома Li:
Электронная кон- фигурация для атома Li: 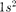 2 s. Атомом Li начинается II период Периодической системы элементов. Четвертым элект- роном Be (Z = 4) заканчивается запол- нение подоболочки У следующих шести элементов от В (Z = 5) до Ne
2 s. Атомом Li начинается II период Периодической системы элементов. Четвертым элект- роном Be (Z = 4) заканчивается запол- нение подоболочки У следующих шести элементов от В (Z = 5) до Ne
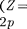
 10) идет заполнение подоболочки (табл. 12). II период Периодической системы заканчивается — инер- тным газом, для которого
10) идет заполнение подоболочки (табл. 12). II период Периодической системы заканчивается — инер- тным газом, для которого 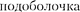
2р целиком заполнена.
Одиннадцатый электрон Na (Z= 11) размещается в М-оболочке (п = 3), за- нимая наинизшее состояние 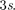 Элект- ронная конфигурация имеет вид
Элект- ронная конфигурация имеет вид
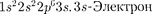
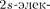 (каки
(каки
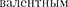

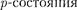 трон Li) является электро- ном, поэтому оптические свойства Na подобны свойствам Li. С Z = 12 идет последовательное заполнение М-обо- лочки. А
трон Li) является электро- ном, поэтому оптические свойства Na подобны свойствам Li. С Z = 12 идет последовательное заполнение М-обо- лочки. А 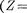 18) оказывается подоб- ным Не и Ne: в его наружной оболочке все s- и заполнены.
18) оказывается подоб- ным Не и Ne: в его наружной оболочке все s- и заполнены. 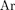 яв- ляется химически инертным и завер- шает III период Периодической сис- темы.
яв- ляется химически инертным и завер- шает III период Периодической сис- темы.
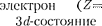
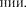 Девятнадцатый К 19) должен был бы занять в М- оболочке. Однако и в оптическом, и в химическом отношениях атом К схож с атомами Li и Na, которые имеют вне- шний
Девятнадцатый К 19) должен был бы занять в М- оболочке. Однако и в оптическом, и в химическом отношениях атом К схож с атомами Li и Na, которые имеют вне- шний 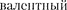 электрон в s-состоя- Поэтому 19-й валентный электрон
электрон в s-состоя- Поэтому 19-й валентный электрон
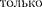 К должен также находиться в s-состоя- нии, но это может быть s-состоя- ние новой оболочки (TV-оболочки), т. е. заполнение TV-оболочки для К начина-
К должен также находиться в s-состоя- нии, но это может быть s-состоя- ние новой оболочки (TV-оболочки), т. е. заполнение TV-оболочки для К начина-
ется при незаполненной М-оболочке. Это означает, что в результате взаимо- действия электронов состояние п = 4,

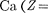 / = 0 имеет меньшую энергию, чем со- стояние п = 3,
/ = 0 имеет меньшую энергию, чем со- стояние п = 3, 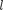 2. Спектроскопичес- кие и химические свойства 20) показывают, что его 20-й электрон также находится в 45-состоянии TV-оболочки.
2. Спектроскопичес- кие и химические свойства 20) показывают, что его 20-й электрон также находится в 45-состоянии TV-оболочки.
В последующих элементах происхо- дит заполнение М-оболочки [от Sc
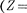
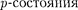 21) до Zn (Z= 30)]. Далее TV-обо- лочка заполняется до
21) до Zn (Z= 30)]. Далее TV-обо- лочка заполняется до 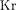 (Z = 36), у которого опять-таки, как и в случае Ne и
(Z = 36), у которого опять-таки, как и в случае Ne и 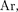 s- и наружной обо- лочки заполнены целиком. Криптоном заканчивается IV период Периодиче- ской системы. Подобные рассуждения применимы и к остальным элементам таблицы Менделеева, однако эти дан- ные можно найти в справочниках. От- метим лишь, что и начальные элемен- ты последующих периодов Rb, Cs, Fr яв- ляются щелочными металлами, а их последний электрон находится в s-co-
s- и наружной обо- лочки заполнены целиком. Криптоном заканчивается IV период Периодиче- ской системы. Подобные рассуждения применимы и к остальным элементам таблицы Менделеева, однако эти дан- ные можно найти в справочниках. От- метим лишь, что и начальные элемен- ты последующих периодов Rb, Cs, Fr яв- ляются щелочными металлами, а их последний электрон находится в s-co-
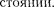
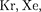
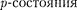 Кроме того, атомы инертных газов
Кроме того, атомы инертных газов 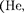 Ne,
Ne, 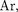 Rn) занимают в таблице особое положение — в каж- дом из них 5- и наружной оболочки целиком заполнены и ими за- вершаются очередные периоды Перио- дической системы.
Rn) занимают в таблице особое положение — в каж- дом из них 5- и наружной оболочки целиком заполнены и ими за- вершаются очередные периоды Перио- дической системы.
 Каждую из двух групп элементов — лантаниды [от лантана
Каждую из двух групп элементов — лантаниды [от лантана 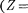 57) до лю- теция (Z = 71)] и актиниды [от акти- ния (Z= 89) до лоуренсия
57) до лю- теция (Z = 71)] и актиниды [от акти- ния (Z= 89) до лоуренсия 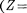 103)] — приходится помещать в одну клетку таблицы, так как химические свойства элементов в пределах этих групп очень близки. Это объясняется тем, что для лантанидов заполнение подоболочки 4/, которая может содержать 14 электро- нов, начинается лишь после того, как целиком заполнятся подоболочки 5s, Ър 6 s. Поэтому для этих элементов вне- шняя Р-оболочка (6s2) оказывается одинаковой. Аналогично, одинаковой
103)] — приходится помещать в одну клетку таблицы, так как химические свойства элементов в пределах этих групп очень близки. Это объясняется тем, что для лантанидов заполнение подоболочки 4/, которая может содержать 14 электро- нов, начинается лишь после того, как целиком заполнятся подоболочки 5s, Ър 6 s. Поэтому для этих элементов вне- шняя Р-оболочка (6s2) оказывается одинаковой. Аналогично, одинаковой
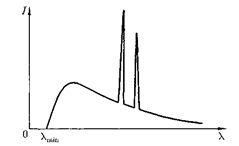 для актинидов является
для актинидов является 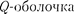
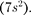
 Таким образом, открытая Менделе- евым периодичность в химических свойствах элементов
Таким образом, открытая Менделе- евым периодичность в химических свойствах элементов 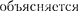 по- вторяемостью в структуре внешних оболочек у атомов родственных эле- ментов. Так, инертные газы имеют оди- наковые внешние оболочки из 8 элект- ронов (заполненные s-
по- вторяемостью в структуре внешних оболочек у атомов родственных эле- ментов. Так, инертные газы имеют оди- наковые внешние оболочки из 8 элект- ронов (заполненные s- 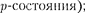 во внешней оболочке щелочных метал- лов (Li, Na, К, Rb, Cs, Fr) имеется лишь один 5-электрои; во внешней
во внешней оболочке щелочных метал- лов (Li, Na, К, Rb, Cs, Fr) имеется лишь один 5-электрои; во внешней 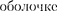 щелочно-земельных металлов (Be, Mg,
щелочно-земельных металлов (Be, Mg,
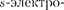
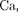 Sr,
Sr, 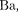 Ra) имеется два
Ra) имеется два
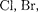
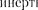 на; галоиды (F, I, At) имеют вне- шние оболочки, в которых недостает одного электрона до оболочки ю- го газа, и т.д.
на; галоиды (F, I, At) имеют вне- шние оболочки, в которых недостает одного электрона до оболочки ю- го газа, и т.д.
§229.Рентгеновскиеспектры
 Большую роль в выяснении строе- ния атома, а именно
Большую роль в выяснении строе- ния атома, а именно
электронов по оболочкам, сыграло из- лучение, открытое в 1895 г. немецким физиком В. Рентгеном (1845 — 1923) и названное рентгеновским.
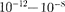 Самым распространенным источни- ком рентгеновского излучения являет- ся рентгеновская трубка, в которой сильно ускоренные электрическим по- лем электроны бомбардируют анод (ме- таллическая мишень из тяжелых метал- лов, например W или Pt), испытывая на нем резкое торможение. При этом возникает рентгеновское излучение, представляющее собой электромагнит- ное излучение с длиной волны пример- но м. Волновая природа рен- тгеновского излучения доказана опыта- ми по его дифракции (см. §
Самым распространенным источни- ком рентгеновского излучения являет- ся рентгеновская трубка, в которой сильно ускоренные электрическим по- лем электроны бомбардируют анод (ме- таллическая мишень из тяжелых метал- лов, например W или Pt), испытывая на нем резкое торможение. При этом возникает рентгеновское излучение, представляющее собой электромагнит- ное излучение с длиной волны пример- но м. Волновая природа рен- тгеновского излучения доказана опыта- ми по его дифракции (см. § 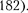
Исследование спектрального соста- ва рентгеновского излучения показыва- ет, что его спектр имеет сложную струк-
 309
309
 туру (рис. 309) и зависит как от энер- гии электронов, так и от материала ано- да. Спектр представляет собой наложе- ние сплошного спектра, ограниченного со стороны коротких длин волн неко- торой границей
туру (рис. 309) и зависит как от энер- гии электронов, так и от материала ано- да. Спектр представляет собой наложе- ние сплошного спектра, ограниченного со стороны коротких длин волн неко- торой границей 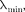 называемой гра- ницей сплошного спектра, линейча- того спектра — совокупности отдель- ных линий, появляющихся на фоне сплошного спектра.
называемой гра- ницей сплошного спектра, линейча- того спектра — совокупности отдель- ных линий, появляющихся на фоне сплошного спектра.
 Исследования показали, что харак- тер сплошного спектра не зависит от материала анода, а определяется толь- ко
Исследования показали, что харак- тер сплошного спектра не зависит от материала анода, а определяется толь- ко 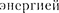 бомбардирующих анод электронов. Детальное исследование свойств этого излучения показало, что оно испускается бомбардирующими анод электронами в результате их тор- можения при взаимодействии с атома- ми мишени. Сплошной рентгеновский спектр поэтому называют тормозным спектром. Этот вывод находится в со- с классической теорией излуче-
бомбардирующих анод электронов. Детальное исследование свойств этого излучения показало, что оно испускается бомбардирующими анод электронами в результате их тор- можения при взаимодействии с атома- ми мишени. Сплошной рентгеновский спектр поэтому называют тормозным спектром. Этот вывод находится в со- с классической теорией излуче-
ния, так как при торможении движу- щихся зарядов должно действительно возникать излучение со сплошным спектром.
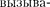 Из классической теории, однако, не вытекает существование коротковол- новой границы сплошного спектра. Из опытов следует, что чем больше кине- тическая энергия электронов,
Из классической теории, однако, не вытекает существование коротковол- новой границы сплошного спектра. Из опытов следует, что чем больше кине- тическая энергия электронов,
ющих тормозное рентгеновское излуче- ние, тем меньше 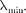 Это обстоятель- ство, а также наличие самой границы
Это обстоятель- ство, а также наличие самой границы
объясняются квантовой теорией. Оче- видно, что предельная энергия кванта соответствует такому случаю торможе- ния, при котором вся кинетическая энергия электрона переходит в энергию кванта, т. е.
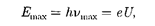
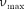 где —частота, соответствующая границе сплошного спектра; U —раз- ность потенциалов, засчет которой электрону сообщается энергия
где —частота, соответствующая границе сплошного спектра; U —раз- ность потенциалов, засчет которой электрону сообщается энергия 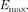
Отсюда граничная длина волны
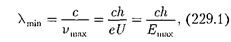
что полностью соответствует экспери- ментальным данным. Измеряя границу рентгеновского сплошного спектра, по формуле (229.1) можно определить эк- спериментальное значение постоянной Планка h, которое наиболее точно со- впадает с современными данными.
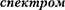 При достаточно большой энергии бомбардирующих анод электронов на фоне сплошного спектра появляются отдельные резкие линии — линейчатый спектр, определяемый материалом ано- да и называемый характеристичес- ким рентгеновским (излу- чением).
При достаточно большой энергии бомбардирующих анод электронов на фоне сплошного спектра появляются отдельные резкие линии — линейчатый спектр, определяемый материалом ано- да и называемый характеристичес- ким рентгеновским (излу- чением).
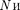

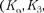 По сравнению с оптическими спек- трами характеристические рентгено- вские спектры элементов совершенно однотипны и состоят из нескольких се- рий, обозначаемых К, L, M, О. Каж- дая серия, в свою очередь, содержит небольшой набор отдельных линий, обозначаемых в порядке убывания дли- ны волны индексами а, (3, ...
По сравнению с оптическими спек- трами характеристические рентгено- вские спектры элементов совершенно однотипны и состоят из нескольких се- рий, обозначаемых К, L, M, О. Каж- дая серия, в свою очередь, содержит небольшой набор отдельных линий, обозначаемых в порядке убывания дли- ны волны индексами а, (3, ...
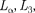
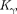 ...,
..., 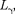 ...).
...).
При переходе от легких элементов к тяжелым структура характеристическо- го спектра не изменяется, лишь весь спектр смещается в сторону коротких волн. Особенность этих спектров зак-
лючается в том, что атомы каждого хи- мического элемента, независимо от того, ли они в свободном стоянии или входят в химическое со- единение, обладают определенным, присущим только данному элементу линейчатым спектром характеристи- ческого излучения. Так, если анод со- стоит из нескольких элементов, то и ха- рактеристическое рентгеновское излу- чение представляет собой наложение спектров этих элементов.
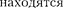
 Рассмотрение структуры и особен- ностей характеристических рентгено- вских спектров приводит к выводу, что их возникновение связано с процесса- ми, происходящими во внутренних, за- строенных электронных оболочках атомов, которые имеют сходное строе- ние.
Рассмотрение структуры и особен- ностей характеристических рентгено- вских спектров приводит к выводу, что их возникновение связано с процесса- ми, происходящими во внутренних, за- строенных электронных оболочках атомов, которые имеют сходное строе- ние.
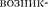 Разберем механизм возникновения рентгеновских серий, который схемати- чески показан на рис. 310. Предполо- жим, что под влиянием внешнего элек- трона или высокоэнергетического фо- тона вырывается один из двух электро- нов
Разберем механизм возникновения рентгеновских серий, который схемати- чески показан на рис. 310. Предполо- жим, что под влиянием внешнего элек- трона или высокоэнергетического фо- тона вырывается один из двух электро- нов 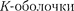 атома. Тогда на его ме- сто может перейти электрон с более уда- ленных от ядра оболочек L,M,N,... . Та- кие переходы сопровождаются испуска- нием рентгеновских квантов и
атома. Тогда на его ме- сто может перейти электрон с более уда- ленных от ядра оболочек L,M,N,... . Та- кие переходы сопровождаются испуска- нием рентгеновских квантов и
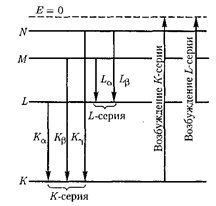 |
Рис.310
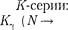 новениемспектральныхлиний
новениемспектральныхлиний

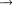
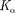 (L К),
(L К), 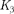 (М К), К)
(М К), К)
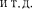
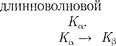 Самой
Самой 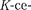
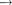 рии является линия Частоты линий возрастают в ряду
рии является линия Частоты линий возрастают в ряду 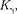 по- скольку энергия, высвобождаемая при переходе электрона на
по- скольку энергия, высвобождаемая при переходе электрона на 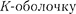 с более удаленных оболочек, увеличива- ется.
с более удаленных оболочек, увеличива- ется.
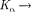
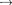 Наоборот, интенсивности линий в ряду
Наоборот, интенсивности линий в ряду 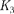
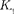 убывают, так как вероятность переходов электронов с
убывают, так как вероятность переходов электронов с
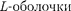 на
на 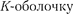 больше, чем с более удаленных оболочек М и N.
больше, чем с более удаленных оболочек М и N. 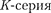 сопровождается обязательно другими сериями, так как при испуска- нии ее линий появляются вакансии в оболочках L, М, ..., которые будут за- полняться электронами, находящими- ся на более высоких уровнях.
сопровождается обязательно другими сериями, так как при испуска- нии ее линий появляются вакансии в оболочках L, М, ..., которые будут за- полняться электронами, находящими- ся на более высоких уровнях.
Аналогично возникают и другие се- рии, наблюдаемые, впрочем, только для тяжелых элементов. Рассмотренные линии характеристического излучения могут иметь тонкую структуру, по- скольку уровни, определяемые глав- ным квантовым числом, расщепляют- ся согласно значениям орбитального и магнитного квантовых чисел.
Исследуя рентгеновские спектры элементов, английскийфизик Г. Мозли (1887-1915) установил в 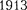 г. соот- ношение, называемое законом Мозли:
г. соот- ношение, называемое законом Мозли:
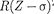 = 1(229.2)
= 1(229.2)
 где v — частота, соответствующая дан- ной линии характеристического рент- геновского излучения; R — постоянная Ридберга; — постоянная экранирова- ния; т = 1, 2, 3,...
где v — частота, соответствующая дан- ной линии характеристического рент- геновского излучения; R — постоянная Ридберга; — постоянная экранирова- ния; т = 1, 2, 3,... 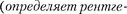

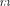 новскую серию), п принимает целочис- ленные значения, начиная с + 1 (оп- ределяет отдельную линию соответ- ствующей серии).
новскую серию), п принимает целочис- ленные значения, начиная с + 1 (оп- ределяет отдельную линию соответ- ствующей серии).
Закон Мозли (229.2) подобен обоб- щенной формуле Бальмера (209.3) для атома водорода.
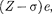 Смысл постоянной экранирования заключается в том, что на электрон, со- вершающий переход, соответствующий некоторой линии, действует не весь за- ряд ядра
Смысл постоянной экранирования заключается в том, что на электрон, со- вершающий переход, соответствующий некоторой линии, действует не весь за- ряд ядра 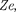 а заряд ослаблен- ный экранирующим действием других электронов. Например, для
а заряд ослаблен- ный экранирующим действием других электронов. Например, для 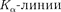 а = 1, и закон Мозли запишется в виде
а = 1, и закон Мозли запишется в виде
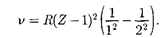
§ 230. Молекулы: химические связи, понятие об энергетических уровнях
 Молекула — наименьшая частица вещества, состоящая из одинаковых или различных атомов, соединенных между собой химическими связями, и являющаяся носителем его основных химических и физических свойств. Хи- мические связи обусловлены взаимо- действием внешних, валентных элект- ронов атомов. Наиболее часто в моле- кулах встречается два типа связи: ион- ная (см. § 71).
Молекула — наименьшая частица вещества, состоящая из одинаковых или различных атомов, соединенных между собой химическими связями, и являющаяся носителем его основных химических и физических свойств. Хи- мические связи обусловлены взаимо- действием внешних, валентных элект- ронов атомов. Наиболее часто в моле- кулах встречается два типа связи: ион- ная (см. § 71).
Ионная связь (например, в молеку- лах 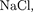
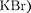 осуществляется элект- ростатическим взаимодействием ато- мов при переходе электрона одного атома к другому, т.е. при образовании положительного и отрицательного
осуществляется элект- ростатическим взаимодействием ато- мов при переходе электрона одного атома к другому, т.е. при образовании положительного и отрицательного
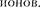
Ковалентная связь (например, в молекулах 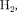
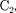 СО) осуществляется при обобществлении валентных элект- ронов двумя соседними атомами (спи- ны валентных электронов должны быть антипараллельны).
СО) осуществляется при обобществлении валентных элект- ронов двумя соседними атомами (спи- ны валентных электронов должны быть антипараллельны).
Ковалентная связь объясняется на основе принципа неразличимости тож-
 Явственных частиц (см. § 226), напри- мер электронов в молекуле водорода. Неразличимость частиц приводит к специфическому взаимодействию меж- ду ними, называемому обменным вза- имодействием. Это чисто квантовый эффект, не имеющий классического объяснения, его можно себе предста- вить так, что электрон каждого из ато- мов молекулы водорода проводит неко- торое время у ядра другого атома и, сле- довательно, осуществляется связь обо- их атомов, образующих молекулу. При сближении двух водородных атомов до расстояний порядка боровского радиу- са возникает их взаимное притяжение и образуется устойчивая молекула во- дорода.
Явственных частиц (см. § 226), напри- мер электронов в молекуле водорода. Неразличимость частиц приводит к специфическому взаимодействию меж- ду ними, называемому обменным вза- имодействием. Это чисто квантовый эффект, не имеющий классического объяснения, его можно себе предста- вить так, что электрон каждого из ато- мов молекулы водорода проводит неко- торое время у ядра другого атома и, сле- довательно, осуществляется связь обо- их атомов, образующих молекулу. При сближении двух водородных атомов до расстояний порядка боровского радиу- са возникает их взаимное притяжение и образуется устойчивая молекула во- дорода.
Молекула является квантовой сис- темой; она описывается уравнением Шредингера, учитывающим движение электронов в молекуле, колебания ато- мов молекулы, вращение молекулы. Решение этого уравнения — очень слож- ная задача, которая обычно разбивает- ся на две: для электронов и ядер.
Энергия изолированной молекулы
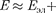

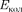
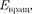 (230.1)
(230.1)
где 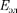 — энергия движения электронов относительно ядер;
— энергия движения электронов относительно ядер; 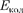 — энергия ко- лебаний ядер (в результате которых периодически изменяется относитель- ное положение ядер);
— энергия ко- лебаний ядер (в результате которых периодически изменяется относитель- ное положение ядер); 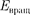 — энергия вращения ядер (в результате которых периодически изменяется ориентация молекулы в пространстве).
— энергия вращения ядер (в результате которых периодически изменяется ориентация молекулы в пространстве).
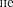 В формуле (230.1) не учтены энер- гия поступательного движения центра масс молекулы и энергия ядер атомов в молекуле. Первая из них не квантует- ся, поэтому ее изменения не могут при- вести к возникновению молекулярно- го спектра, а вторую можно не учиты- вать, если рассматривать сверхтон- кую структуру спектральных линий.
В формуле (230.1) не учтены энер- гия поступательного движения центра масс молекулы и энергия ядер атомов в молекуле. Первая из них не квантует- ся, поэтому ее изменения не могут при- вести к возникновению молекулярно- го спектра, а вторую можно не учиты- вать, если рассматривать сверхтон- кую структуру спектральных линий.
Отношения =
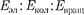

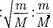
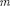 где — масса электрона; М— величина, имеющая порядок массы ядер атомов
где — масса электрона; М— величина, имеющая порядок массы ядер атомов
 в молекуле, —
в молекуле, — 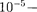
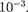 Поэтому
Поэтому
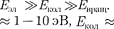
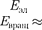
 Доказано, что
Доказано, что
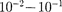 эВ,
эВ,
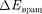 Каждая из входящих в выражение (230.1) энергий квантуется (ей соответ- ствует набор дискретных уровней энер- гии) и определяется квантовыми чис- лами. При переходе из одного энерге- тического состояния в другое поглоща- ется или испускается энергия
Каждая из входящих в выражение (230.1) энергий квантуется (ей соответ- ствует набор дискретных уровней энер- гии) и определяется квантовыми чис- лами. При переходе из одного энерге- тического состояния в другое поглоща- ется или испускается энергия 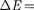 hv. При таких переходах одновременно из- меняются энергия движения электро- нов,энергии колебанийи вращенияядер. Из теории и эксперимента следует, что расстояние между вращательными уровнями энергии гораздо мень-
hv. При таких переходах одновременно из- меняются энергия движения электро- нов,энергии колебанийи вращенияядер. Из теории и эксперимента следует, что расстояние между вращательными уровнями энергии гораздо мень-
 |
Электронные уровни
 432
432
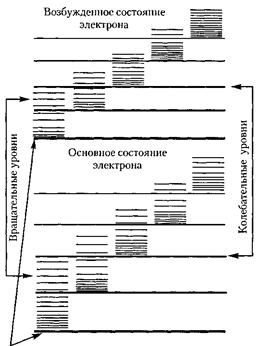
 ше расстояния между колебательными уровнями
ше расстояния между колебательными уровнями 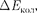 которое, в свою оче- редь, меньше расстояния между элект- ронными уровнями
которое, в свою оче- редь, меньше расстояния между элект- ронными уровнями 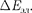 На рис.
На рис. 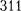 схематически представлены
схематически представлены
энергии двухатомной молекулы (для примера рассмотрены только два элек- тронных уровня — показаны жирными
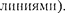
Как будет показано в § 231, структу- ра энергетических уровней молекул определяет их спектр излучения, возни- кающий при квантовых переходах меж- ду соответствующими энергетическими уровнями.
§ 231. Молекулярные спектры. Комбинационное рассеяние света
 Строение молекул и свойства их энергетических уровней проявляются в молекулярных спектрах — спектрах излучения (поглощения), возникаю- щих при квантовых переходах между уровнями энергии молекул. Спектр из- лучения определяется струк- турой ее энергетических уровней и со- ответствующими правилами отбора (например, изменение квантовых чи- сел, соответствующих как колебатель- ному, так и вращательному движению, должно быть равно ±1).
Строение молекул и свойства их энергетических уровней проявляются в молекулярных спектрах — спектрах излучения (поглощения), возникаю- щих при квантовых переходах между уровнями энергии молекул. Спектр из- лучения определяется струк- турой ее энергетических уровней и со- ответствующими правилами отбора (например, изменение квантовых чи- сел, соответствующих как колебатель- ному, так и вращательному движению, должно быть равно ±1).
 Итак, при разных типах переходов между уровнями возникают различные типы молекулярных спектров. Частоты спектральных линий, испускаемых мо- лекулами, могут соответствовать пере- ходам с одного электронного уровня на другой (электронные спектры) или с одного колебательного (вращательно- го) уровня на другой [колебательные (вращательные) спектры]. Кроме того, возможны и переходы с одними значениями пауровни, име- ющие другие значения всех трех ком-
Итак, при разных типах переходов между уровнями возникают различные типы молекулярных спектров. Частоты спектральных линий, испускаемых мо- лекулами, могут соответствовать пере- ходам с одного электронного уровня на другой (электронные спектры) или с одного колебательного (вращательно- го) уровня на другой [колебательные (вращательные) спектры]. Кроме того, возможны и переходы с одними значениями пауровни, име- ющие другие значения всех трех ком-
понентов, в результате чего возникают электронно-колебательные ко- лебательно-вращательные спек- тры. Поэтому спектр молекул доволь- но 
 Типичные молекулярные спект- ры — полосатые, представляют собой совокупность более или менее узких по- лос в ультрафиолетовой, видимой и ин- фракрасной областях. Применяя спек- тральные приборы высокой разрешаю- щей способности, можно видеть, что полосы представляют собой настолько тесно расположенные линии, что они с трудом разрешаются.
Типичные молекулярные спект- ры — полосатые, представляют собой совокупность более или менее узких по- лос в ультрафиолетовой, видимой и ин- фракрасной областях. Применяя спек- тральные приборы высокой разрешаю- щей способности, можно видеть, что полосы представляют собой настолько тесно расположенные линии, что они с трудом разрешаются.
Структура молекулярных спектров различна для разных молекул и с уве- личением числа атомов в молекуле ус- ложняется (наблюдаются лишь сплош- ные широкие полосы). Колебательны- ми и вращательными спектрами обла- дают только многоатомные молекулы, а двухатомные их не имеют. Это объяс- няется тем, что двухатомные молекулы не имеют дипольиых моментов (при ко- лебательных и вращательных перехо- дах отсутствует изменение диполыюго момента, что является необходимым условием отличия от нуля вероятнос- ти перехода).
В 1928 г. академики Г.  (1890-1957) и Л.И.Мандельштам, а также индийские физики
(1890-1957) и Л.И.Мандельштам, а также индийские физики 
 (р. 1911) од-
(р. 1911) од-
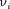 новременно открыли явление комби- национного рассеяния света. Если на вещество (газ, жидкость, прозрачный кристалл) падает строго монохромати- ческий свет, то в спектре рассеянного света помимо несмещенной спектраль- ной линии обнаруживаются новые ли- нии, частоты которых представляют собой суммы или разности частоты v падающего света и частот собствен- ных колебаний (или вращений) моле- кул рассеивающей среды.
новременно открыли явление комби- национного рассеяния света. Если на вещество (газ, жидкость, прозрачный кристалл) падает строго монохромати- ческий свет, то в спектре рассеянного света помимо несмещенной спектраль- ной линии обнаруживаются новые ли- нии, частоты которых представляют собой суммы или разности частоты v падающего света и частот собствен- ных колебаний (или вращений) моле- кул рассеивающей среды.
 Линии в спектре комбинационного рассеяния с частотами у — меньши- ми частоты v падающего света, называ- ются стоксовыми (или красными) спутниками, линии с частотами v + большими v, — антистоксовыми(или фиолетовыми) спутниками.
Линии в спектре комбинационного рассеяния с частотами у — меньши- ми частоты v падающего света, называ- ются стоксовыми (или красными) спутниками, линии с частотами v + большими v, — антистоксовыми(или фиолетовыми) спутниками.
 Анализ спектров комбинационного рассеяния приводит к вы- водам: 1) линии спутников располага- ются симметрично по обе стороны от несмещенной линии; 2) частоты не за- висят от частоты падающего на веще- ство света, а определяются только рас- сеивающим веществом, т.е. характери- зуют его состав структуру; 3) число спутников определяется рассеивающим веществом; 4) интенсивность антисток- совых спутников меньше интенсивно- сти стоксовых и с повышением темпе- ратуры рассеивающего вещества увели- чивается, в то время как интенсивность стоксовых спутников практически от температуры не зависит.
Анализ спектров комбинационного рассеяния приводит к вы- водам: 1) линии спутников располага- ются симметрично по обе стороны от несмещенной линии; 2) частоты не за- висят от частоты падающего на веще- ство света, а определяются только рас- сеивающим веществом, т.е. характери- зуют его состав структуру; 3) число спутников определяется рассеивающим веществом; 4) интенсивность антисток- совых спутников меньше интенсивно- сти стоксовых и с повышением темпе- ратуры рассеивающего вещества увели- чивается, в то время как интенсивность стоксовых спутников практически от температуры не зависит.
 Объяснение закономерностей ком- бинационного рассеяния света дает квантовая теория. Согласно этой тео- рии, рассеяние света есть процесс, в ко- тором один фотон поглощается и один фотон испускается молекулой. Если энергии фотонов одинаковы, то в рас- сеянном свете наблюдается несмещен- ная линия. Однако возможны процес- сы рассеяния, при которых энергии по- глощенного и испущенного фотонов неодинаковы. Различие энергии фото- нов связано с переходом молекулы из нормального состояния в возбужденное (испущенный фотон будет иметь мень- шую частоту — возникает стоксов спут- ник), либо из возбужденного
Объяснение закономерностей ком- бинационного рассеяния света дает квантовая теория. Согласно этой тео- рии, рассеяние света есть процесс, в ко- тором один фотон поглощается и один фотон испускается молекулой. Если энергии фотонов одинаковы, то в рас- сеянном свете наблюдается несмещен- ная линия. Однако возможны процес- сы рассеяния, при которых энергии по- глощенного и испущенного фотонов неодинаковы. Различие энергии фото- нов связано с переходом молекулы из нормального состояния в возбужденное (испущенный фотон будет иметь мень- шую частоту — возникает стоксов спут- ник), либо из возбужденного
в нормальное (испущенный фотон бу- дет иметь большую частоту — возника- ет антистоксов спутник).
Рассеяние света сопровождается пе- реходами молекулы между различны-
ми колебательными или вращательны- ми уровнями, в результате чего и воз- никает ряд симметрично расположен- ных спутников. Число спутников, та- ким образом, определяется энергети- ческим спектром молекул, т. е. зависит только от природы рассеивающего ве- щества. Так как число возбужденных молекул гораздо меньше, чем число не- возбужденных, то интенсивность анти- стоксовых спутников меньше, чем сто- ксовых. С повышением температуры число возбужденных молекул растет, в результате чего возрастает и интенсив- ность антистоксовых спутников.
Молекулярные спектры (в том чис- ле и спектры комбинационного рассея- ния света) применяются для исследо- вания строения и свойств молекул, ис- пользуются в молекулярном спектраль- ном анализе, лазерной спектроскопии, квантовой электронике и т. д.
§ 232. Поглощение. Спонтанное и вынужденное излучения
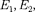
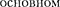

 Как отмечалось выше, атомы могут находиться лишь в квантовых состоя- ниях с дискретными значениями энер- гии
Как отмечалось выше, атомы могут находиться лишь в квантовых состоя- ниях с дискретными значениями энер- гии 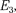 ... . Ради простоты рас- смотрим только два из этих состояний
... . Ради простоты рас- смотрим только два из этих состояний 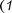 и 2) с энергиями
и 2) с энергиями 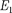 и
и 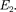 Если атом находится в 1,
Если атом находится в 1,
под действием внешнего излучения может осуществиться вынужденный переход в возбужденное состояние 2 (рис. 312, а), приводящий к поглоще- нию излучения. Вероятность подобных переходов пропорциональна плотности излучения, вызывающего
