В чем состоит гипотеза де Бройля. Чему равна длина волны де Бройля.
В 1923 году выпускник Сорбонны французский физик принц Луи де Бройль высказал предположение (гипотезу) о том, что корпускулярно – волновой дуализм присущ не только свету, но и частицам вещества. Он рассуждал следующим образом. Кванты света с длиной волны 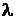 имеют импульс
имеют импульс 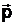 , величина которого определяется по формуле:
, величина которого определяется по формуле:
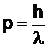 .
.
Любой частице вещества, имеющей импульс 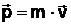 , можно поставить в соответствие волну, длина волны которой определяется соотношением:
, можно поставить в соответствие волну, длина волны которой определяется соотношением:
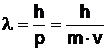 .
.
Соотношение де Бройля недолго оставалось гипотезой. Де Бройль предсказывал, что волны вещества можно будет обнаружить при изучении дифракции пучка частиц вещества на кристаллической структуре естественных кристаллов.
Оценим порядок длин волн, соответствующих нескольким частицам вещества.
1. электрон, движущийся со скоростью 1000000 м/с=106 м/с
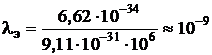 м;
м;
2. пылинка массой 1 мг=10-6 кг, движущаяся с скоростью 1 м/с
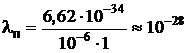 м.
м.
Структур, соизмеримых с длиной волны пылинки нет, а для наблюдения дифракции быстрых электронов вполне подходит кристаллической структуре естественных кристаллов.
32. Что доказывает теорема Нетер
Среди всех интегралов движения особое значение имеют аддитивные или асимптотически аддитивные интегралы движения, для которых существует специальное название – законы сохранения. Если рассмотреть две системы, находящиеся очень далеко друг от друга, то физически очевидно, что процессы в одной системе совсем никак не должны влиять на движение другой. Поскольку, с другой стороны ничто не мешает нам рассматривать две такие системы как две части, I и II, единой общей системы, то мы приходим к условию асимптотической аддитивности, который заключается в следующем: если некоторая система (I + II) разделяется на две подсистемы таким образом, что минимум расстояния между материальными точками разных подсистем 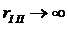 , то ее функция Лагранжа распадается на сумму функций Лагранжа обеих подсистем:
, то ее функция Лагранжа распадается на сумму функций Лагранжа обеих подсистем:
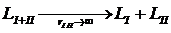 . (1)
. (1)
Законы сохранения имеют глубокое происхождение, связанное с инвариантностью описания механической системы относительно некоторой группы преобразований времени и координат. Существует теорема Нётер, утверждающая, что для системы дифференциальных уравнений, которые могут быть получены как уравнения Эйлера из некоторого вариационного принципа, из инвариантности вариационного функционала относительно однопараметрической непрерывной группы преобразований следует существование одного закона сохранения. Если группа содержит l параметров, то из инвариантности функционала будет следовать существование l законов сохранения.
Наличие входящих в требуемую теоремой Нётер группу преобразований симметрии зависит от природы физической системы. Для рассматриваемых замкнутых систем действие должно быть инвариантным относительно семипараметрической группы преобразований – зависящего от одного сдвига по времени, зависящих от трех параметров пространственных сдвигов и зависящих от трех параметров вращения пространства. В соответствии с этим у всякой замкнутой системы должны существовать 7 сохраняющихся величин, отвечающих указанным преобразованиям. Если система такова, что она допускает еще и другие преобразования симметрии, то сохраняющихся величин может оказаться больше.
Другими словами, из инвариантности действия получаем то следствие, что, величина остается постоянной во времени. Это и есть точное утверждение теоремы Нётер.
33. Место и роль химии в системе «природа-человек»
Химия испытывает на себе влияние физики, пожалуй сильнее, чем любая другая наука. На заре своего развития она играла важную роль в становлении физики. Эти науки взаимодействовали очень сильно, они были практически неразделимы. Теория атомного строения вещества получила основательное подтверждение именно в химических опытах. Под теорией неорганической химии подвел черту Д.И.Менделеев (1834-1907), создав свою периодическую систему химических элементов. Эта система выявила немало удивительных связей между различными элементами. Она предсказала существование многих тогда еще неизвестных химических элементов. Однако, объяснение системы Менделеева возможно только с опорой на теорию строения атома, т.е. на физическую теорию. В настоящее время в неорганической химии остались два раздела: физическая химия и квантовая химия. Сами названия этих разделов говорят о тесной связи с физикой.
Другая ветвь химии - органическая химия, химия веществ, связанных с жизненными процессами. Одно время предполагали, что органические вещества столь сложны, что их нельзя синтезировать. Однако, развитие физики и неорганической химии изменило ситуацию. В настоящее время научились синтезировать сложные органические соединения, необходимые в жизненных процессах. Главной задачей органической химии является анализ и синтез веществ, образующихся в биологических системах, живых организмах. Отсюда вытекает тесная связь химии и физики с другим разделом естествознания, с биологией.
34. Структура химии как науки практической деятельности человека
В начале XIX в. ученые начинают использовать понятие «молекулы». Молекула — это устойчивая совокупность атомов, способная к самостоятельному существованию. Научная революция в химии связана с именем другого русского ученого Д.И. Менделеева, который в 1869 г. предложил периодическую систему химических элементов. Периодическая система, оформленная в виде таблицы, упорядочивала все многообразие известных к тому времени химических элементов и позволяла предсказывать новые. Д.И. Менделеев расположил все элементы в соответствии с возрастанием их атомного веса и показал, что таким образом складывается четкая система. Периодическая система Д.И. Менделеева стала той объединяющей концепцией, которая позволила не только систематизировать, но и объяснить весь накопленный к концу XIX в. эмпирический материал, и стала прочной основой ее временной теоретической химии.
Развитие химии в XX в. шло по линии возрастания дифференцированное внутри комплекса химического знания. Этот процесс привел к разделению на неорганическую и органическую химию и созданию аналитической и физической химии: возникновению целого ряда междисциплинарных исследований, которые со временем обрели самостоятельный научный статус (космохимия, геохимия, агрохимия, биохимия и др.).
35. Законы химии
Закон Авогадро: Одинаковые объемы различных газов при одинаковых условиях (температуре или давлении) содержат одинаковое количество молекул. Таким образом, Авогадро указал, что противоречие между законом объемных отношений Гей-Люссака и учением Дальтона легко устраняется, если ввести представление о молекуле и атоме как о различных формах материи. Закон Гей-Люссака есть закон о числе молекул, а не атомов, находящихся в объеме газа. Из закона Авогадро вытекает важное следствие: при одинаковых условиях 1 моль газа занимает одинаковый объем.Этот объем легко вычислить, если известна масса 1л газа.
По закону Авогадро массы m1 и m2 л каждого из двух разных газов равняются произведению молярной массы М1 и М2 на число 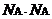 - постоянная (число) Авогадро: число частиц (атомов, молекул или ионов) в моле вещества.
- постоянная (число) Авогадро: число частиц (атомов, молекул или ионов) в моле вещества.
Отношение массы определенного объема одного газа к массе такого же другого газа, взятого при тех же условиях (объем, температура, давление), называется полностью первого газа по второму
