III. Исходный уровень знаний
Тема 2: ПРЕДВАРИТЕЛЬНОЕ ИССЛЕДОВАНИЕ. АНАЛИТИЧЕСКИЙ СКРИНИНГ
I. Мотивация цели
Судебно-химическая экспертиза складывается из предварительного и подтверждающего исследований. Цель предварительного исследования - выявить наличие или отсутствие лекарственных средств в органических экстрактах с использованием скрининговых методов.
Овладение теоретическими основами и практическими навыками проведения аналитического скрининга необходимы провизору для последующей специализации в области судебно-химической экспертизы и клинической токсикологии.
II. Цель самоподготовки
Используя учебный и учебно-методический материал по токсикологической химии, атакже знания и умения по базисным дисциплинам, изучить методы предварительного разделения иобнаружения лекарственных средств.
III. Исходный уровень знаний
Студенты должны знать:
• физико-химические методы, используемые для разделения иобнаружения химических соединений, - хроматография в тонких слоях сорбента.
Студенты должны уметь:
• выполнять хроматографирование в тонких слоях сорбента;
• выполнять обработку хроматограммы цветореагентами и идентифицировать исследуемые соединения;
• рассчитывать абсолютную (Rf) и относительную (Rs) хроматографическую подвижность исследуемых соединений.
IV. План изучения темы
На занятии рассмотреть:
• способы предварительного обнаружения групп лекарственных соединений, экстрагируемых из кислой среды;
• условия ТСХ-скрининга лекарственных соединений кислотного и основного характера, способы обнаружения лекарственных средств на хроматограмме.
V. Рекомендуемая литература
1. Швайкова М.Д.. Токсикологическая химия. - М.: Медицина, 1975. - С. 142-241.
2, Еремин С.К., Изотов Б.Н., Веселовская Н.В. Анализ наркотических средств: Руководство по химико-токсикологическому анализу наркотических и других одурманивающих средств / Под ред. Б.Н. Изотова. - М.: Мысль, 1993. - 250 с.
3. Крамаренко В.Ф, Токсикологическая химия. - Киев: Выща школа, 1989. - С 20-22, 204-295,
4. Крамаренко В.Ф. Химико-токсикологический анализ. - Киев: Выща школа,
1982.-0.9-27,121-197.
5. Белова А.В. Руководство к практическим занятиям по токсикологической химии. - М.: Медицина, 1976. - С. 56-60.
6. Конспект лекций.
VI. Блок информации
Аналитический скрининг
Это научно обоснованная система поиска неизвестного вещества, когда в процессе последовательных операций поэтапно «отсеиваются» отдельные группы веществ и индивидуальные соединения.
Слово «скрининг» в переводе с английского означает «отсеивание».
Аналитический скрининг эффективен при диагностике комбинированных отравлений, а также при ненаправленном анализе.
Требованияк скрининговым методам:
• универсальность;
• специфичность для определенной группы веществ;
• высокая чувствительность (10"8 -10 "!Ог в пробе);
• экспрессность и простота исполнения;
в возможность выполнения серийных анализов;
• возможность стандартизации и совершенствования методов за счет
использования новых материалов, оборудования, расширения списка анализируемых соединений.
Общий скринингпозволяет проводить групповую идентификацию при исследовании веществ, отличающихся по химическому строению и относящихся к различным фармакологическим группам.
Частный скринингнаправлен на обнаружение веществ внутри группы и идентификацию ее отдельных представителей.
К скрининговым методам относятся:
• хроматографические,
• спектральные,
• иммунохимические.
ТСХ- скрининг
В ТСХ-скрининге используют системы растворителей:
• для алкалоидов опия частная система — этилацетат — метанол - 25% раствор гидроксида аммония (17:2:1);
• для веществ из группы наркотических и одурманивающих средств, а также в экспресс-анализе острых интоксикаций - толуол - ацетон - этанол - 25% раствор гидроксида аммония (45:45:7,5:2,5).
Детектирование (проявление) соединений проводят последовательно. Для фракции А:
• 5% раствор сульфата ртути в концентрированной серной кислоте – барбитураты (белые зоны);
• 0,01% раствор дифенилкарбазона (ДФК) в хлороформе — барбитураты (сине- фиолетовые зоны);
• 10% раствор хлорида железа (III) - производные пиразолона-5 (синие зоны, антипирин - красно-оранжевая зона);
• реактив Драгендорфа - вещества, содержащие третичный азот (оранжевые зоны).
• для барбитуратов частная система — хлороформ — н-бутанол — 25% раствор
• для веществ кислотного, нейтрального и слабо основного характера, содержащихся в «кислом» извлечении (фракция А), - хлороформ-ацетон (9:1);
• для веществ основного характера, содержащихся в «щелочном» извлечении (фракция Б), - диоксан - хлороформ - ацетон - 25% раствор гидроксида аммония (47,5:45:5:2,5);
| гидроксида аммония | (70:40:5); | ||||
| Хроматографическая подвижность I соединений фракции Б в общей системе растворителей на пластинах Silufol | |||||
| Название лекарственного средства | R | Rs | |||
| Пахикарпин | 0,12 | 0,23 | |||
| Атропин | 0,15 | 0,29 | |||
| Эфедрин | 0,18 | 0,35 | |||
| Хинин | 0,25 | 0,49 | |||
| стрихнин | 0.25 | 0,49 | |||
| Этапиразин | 0.51 | 1,00 | | |||
| Антипирин | 0,54 | 1,06 | |||
| Кофеин | 0,56 | 1,10 | |||
| Хлозепид | 0,63 | 1.25 | |||
| Дипразин | 0,66 | 1,30 | |||
| Производные ПАБК | 0,70 | 1,37 | |||
| Тиоридазин | 0,72 | 1,41 | |||
| Аминазин | 0,75 | 1,47 | |||
| Нитразепам | 0,77 | 1,51 | |||
| Амидопирин | 0.83 | 1,63 | |||
| Тизерцин | 0,87 | 1,71 | |||
| Диазепам | 0,95 | 1,87 | |||
Для фракции Б:
- 10% раствор хлорида железа (III) — производные пиразолона-5 (синие зоны, антипирин — красно-оранжевая зона), производные фенотиазина (аминазин, дипразин - розовые, тизерцин - фиолетовая, тиоридазин - зелено-голубая зоны);
- хлорная кислота концентрированная, содержащая 5% раствор нитрита натрия (97:3) — производные фенотиазина (аминазин, дипразин - розовые, тизерцин - фиолетовая, тиоридазин - зелено-голубая зоны);
- 10% раствор серной кислоты - хинин (голубая флуоресценция в УФ-свете)
- реактив Драгендорфа - вещества, содержащие третичный азот (оранжевые зоны).
ВЭТСХ - высокоэффективная тонкослойная хроматография. Высокая эффективность метода достигается за счет применения высокодисперсного сорбента, а высокая чувствительность и экспрессность — более тонкого слоя сорбента.
ГЖХ- газо-жидкостная хроматография. Достоверность определения повышается за счет хроматографирования на колонках, обладающих различной полярностью. Комитет по судебной токсикологии предлагает использовать ко лонки с неподвижными жидкими фазами SE-3O, OV-17, OV- 225. Детектор ионизации пламени.
ВЭЖХ - высокоэффективная жидкостная хроматография. ВЭЖХ или жидкостная хроматография высокого давления является вариантом колоночной жидкостной хроматографии, где элюент подается на колонку под большим давлением, что ускоряет проведение анализа. В качестве детекторов могут быть использованы: спектрофотометрический с переменной (190-700 нм) или фиксированной (254 нм) длинной волны, рефрактометрический, флуори-метрический, ионизации пламени, масс-спектрометрический, электрохимический и т.д. Идентификацию веществ проводят по параметрам удерживания и спектрам поглощения.
Иммунохимические методы
В основе методов лежит специфическая реакция «антиген-антитело», где антигеном является определяемое вещество, чужеродное для организма. Специфическим реагентом является антитело, которое вырабатывается как реакция на внедрение чужеродного вещества. При взаимодействии антигена-яда со специфичным к нему реактивом-антителом образуется комплекс, который выпадает в осадок. Количественно оценить результаты реакции позволяют введение специальных меток. В зависимости от природы метки и способа детектирования выделяют:
• радиоиммунный анализ,
• иммуноферментный (иммуноэнзимный) анализ,
• поляризационный флюороиммунный анализ,
• люминесцентный иммуноанализ.
Иммуноэнзимный метод получил наибольшее распространение. В качестве метки для антигенов используют ферменты - различные оксидазы, способные количественно окислять специальное химическое вещество - хромо-генный субстрат - с образование окрашенных продуктов.
Иммунохимические методы анализа обладают высокой чувствительностью, специфичностью, экспрессностью, простотой исполнения. Реакции проводятся непосредственно в биологических жидкостях и позволяют одновременно диагностировать большое число проб.
VII. Вопросы для самоконтроля
1. Какие этапы включает в себя предварительное исследование? В чём
цель предварительного исследования?
2. Какие химические реакции используются для предварительного обнаружения производных барбитуровой кислоты, пиразолона-5, фенотиазина?
3. Укажите особенности оформления пластинки в ТСХ-скрининге лекарственных и наркотических средств.
4. Объясните цель нанесения на пластинку двух стандартов и двух, порций экстракта в соответствующие зоны пластинки.
Какие стандарты-метчики используются при хроматографическом скрининге экстракта из кислой среды, из щелочной среды?
6. подвижных фаз, используемых в ТСХ-скринкнге.
7. Какие реактивы, и в какой последовательности применяют для обнаружения средств кислотного характера, обнаружения средств основного характера?
8. Что представляет собой реактив Драгендорфа? В чём суть и цель модификации реактива Драгендорфа?
9. Объясните термин «аналитический скрининг».
10.Какие требования предъявляются к скрининговым методам?
VIII. Задания, обязательные для выполнения
| ТСХ-скрининг экстракта из щелочной среды |
Заполнить таблицы: ТСХ-скрининг экстракта из кислой среды
IX. План работы на занятии
Работа на занятии состоит из этапов:
• обсуждение основных этапов исследования лекарственных соединений;
• рассмотрение условий ТСХ-скрининга лекарственных соединений кислотного и основного характера;
• рассмотрение методов обнаружения лекарственных средств на хрома то грамме;
• проведение ТСХ-исследования лекарственных средств изучаемых групп.
X. Лабораторная работа
Проводят хроматографическое исследование хлороформных экстрактов на наличие лекарственных средств. В качестве подвижных фаз используют общие системы для ТСХ-скрининга веществ кислотного и щелочного характера-Условия хроматографирования приведены в блоке информации.
Проводят обработку хроматограмм соответствующими цветореагентами.
Рассчитывают хроматографическую подвижность (Rf) исследуемых лекарственных средств и сравнивают их с табличными значениями.
I. Мотивация цели
Широкое применение лекарственных средств и, в частности, производных барбитуровой кислоты в медицинской практике создает условия для возникновения отравлений в результате их неквалифицированного или немедицинского использования. Овладение техникой и методиками анализа лекарственных соединений является необходимым при освоении химико-токсикологических методов исследования.
II. Цель самоподготовки
Используя учебный и учебно-методический материал по токсикологической химии, а также знания и умения по базисным дисциплинам, изучить методы исследования лекарственных средств кислотного, нейтрального и слабоосновного характера, выделенных из объектов биологического происхождения.
VI. Блок информации
Производные барбитуровой кислоты
Всасывание производных барбитуровой кислоты начинается в желудке, где они находятся в недиссоциированной форме, и заканчивается в кишечнике. Барбитураты, хорошо растворимые в липидах (барбамил, этаминал), всасываются в течение 15-20 мин, а плохо растворимые (барбитал и фенобарбитал) всасываются в течение нескольких часов. Максимальная концентрация в крови наблюдается через 4-8 и 12-18 часов. Наиболее опасны препараты короткого действия, так как токсическая концентрация может возникнуть уже через 30-60 мин. Барбитураты средней продолжительности действия (барбамил, этаминал) связываются с белками крови на 50-60%. Для препаратов длительного действия (фенобарбитал, барбитал) связывание достигает 5-15%.
Следы барбитала и фенобарбитала в моче могут быть обнаружены на протяжении 8-12 дней. Элиминация этаминала заканчивается в течение 3-4 дней.
При отравлении барбитуратами уменьшается диурез, замедляется перистальтика кишечника, снижается секреция желудочного сока, раскрываются сфинктеры. Обычно снижается температура тела.
К смертельному исходу при отравлении приводит тяжелая гипоксия, сопровождающаяся отеком легких, отеком мозга, почечной недостаточностью, гибелью клеток головного мозга.
VIII. Задания, обязательные для выполнения
Составить схему исследования по направлению:
1.Провести судебно-химическое исследование при подозрении на отрав
ление производными барбитуровой кислоты.
2.Провести судебно-химическое исследование при подозрении на отрав
ление производными пиразолона-5.
3.Заполнить таблицу:
| МКС-реакции | производных | барбитуровой | кислоты | ||||
| Производные | Реактивы | ||||||
| барбитуровой | |||||||
| кислоты | Фо | эма кристаллов | |||||
| 1. | 1 1 | ||||||
| 2. | |||||||
| 3. | |||||||
| 4. |
IX. План работы на занятиях
Работа на занятии 1 состоит из этапов:
• обсуждение вопросов токсичности и метаболизма производных барбитуровой кислоты;
• обсуждение методик предварительного и подтверждающего исследова-
ния на производные барбитуровой кислоты химическими методами;
• проведение цветных и МКС реакций на производные барбитуровой ки-
слоты. Работа на занятии 2 состоит из этапов:
• обсуждение методик и проведение определения количественного содержания производных барбитуровой кислоты в изоляте спектрофото-метрическим методом;
• тестовый контроль по вопросам предварительного исследования ве-
ществ кислого характера. Работа на занятии 3 состоит из этапов:
• рассмотрение вопросов токсичности и метаболизма производных пира-золона-5;
• практическая работа по обнаружению производных пиразолона-5;
« тестовый контроль по вопросам предварительного исследования веществ основного характера.
X. Лабораторная работа
Обнаружение производных барбитуровой кислоты Предварительные исследования
1. Реакция с нитратом кобальта.
Бумагу, импрегнированную раствором нитрата кобальта, смачивают исследуемым экстрактом, содержащим производное барбитуровой кислоты, подсушивают, держат над парами аммиака. Бумага окрашивается в розово-фиолетовый цвет.
2. ТСХ-скрининг.
Система растворителей: хлороформ-ацетон (9:1). Способы детекции:
- 5% раствором сульфата ртути;
- раствором 0,01% дифенилкарбазона в хлороформе.
Подтверждающие исследования
1. Мурексидная проба.
В фарфоровую чашку к сухому остатку, полученному после выпаривания хлороформного раствора исследуемого вещества или экстракта при комнатной температуре, прибавляют 3 капли 3% раствора перекиси водорода и 3 капли реактива, содержащего соль Мора и хлорид аммония. Содержимое чашки выпаривают на электроплитке и сухой остаток нагревают до появления белых паров. После охлаждения прибавляют 3 капли б н. раствора гидроксида аммония. При наличии производных барбитуровой и тиобарбитуровой кислот появляется розовая окраска.
Следует обратить внимание, что кофеин даёт подобную реакцию. *
2. Реакция с концентрированной серной кислотой (МКС).
На предметное стекло наносят несколько капель хлороформного раствора исследуемого вещества или экстракта и выпаривают досуха. Сухой остаток растворяют в капле концентрированной серной кислоты, помещенной на предметное стекло. Через 3-5 мин рядом помещают каплю дистиллированной воды и капилляром соединяют их. Через 10-20 мин под микроскопом наблюдают появление кристаллов кислотной формы.
(^ЗуРеакция с хлорцинкйодом (МКС).
На предметное стекло наносят несколько капель хлороформного раствора исследуемого вещества или экстракта и выпаривают досуха. К сухому остатку прибавляют 1 каплю раствора хлорцинкйода. Через 10-15 мин под микроскопом наблюдают форму образовавшихся кристаллов.
2?)Реакпия со смесью хлорида железа и йодида калия (МКС).
На предметное стекло наносят несколько капель хлороформного раствора исследуемого вещества или экстракта и выпаривают досуха. К сухому остатку прибавляют 1 каплю раствора железойоидного реактива (смесь хлорида железа и йодида калия). Через 10-15 мин под микроскопом наблюдают форму образовавшихся кристаллов.
5. Реакция с дииодокупратом калия в растворе йода (МКС).
На предметное стекло наносят несколько капель хлороформного раствора исследуемого вещества или экстракта и выпаривают досуха. К сухому остатку прибавляют 1 каплю дииодокупрата калия в растворе йода. Через 10-15 минут под микроскопом наблюдают форму образовавшихся кристаллов.
6. Поглощение в УФ-области.
Кюветы спектрофотометра заполняют раствором барбитурата (рН=Ю) и буферным раствором (рН=10), снимают спектр поглощения. Максимум поглощения наблюдают в интервале длин волн 235-245 им.
В кюветы спектрофотометра с раствором барбитурата (рН=10) и буферным раствором (рН=10) добавляют по 1-2 капли концентрированной соляной кислоты до рН=2, перемешивают стеклянной палочкой и снимают спектр поглощения, Наблюдают плавное снижение оптической плотности в интервале длин волн 220-260 нм.
В кюветы спектрофотометра с раствором барбитурата (рН=10) и буферным раствором (рН=10) добавляют по 1-2 капли концентрированного (4 н.) раствора натрия гидроксида до рН=13, перемешивают стеклянной палочкой и снимают спектр поглощения. Максимум поглощения наблюдают в интервале длин волн 255-265 нм.
Обнаружение производных пиразолона-5 Предварительные исследования
1. Реакция с хлоридом железа.
На предметное стекло наносят несколько капель хлороформного раствора исследуемого вещества или экстракта и выпаривают досуха, к сухому остатку прибавляют каплю 1% раствора хлорида железа. При наличии амидопирина появляется фиолетовая окраска, исчезающая от избытка реактива; антипирина -оранжево-красная; анальгина— синяя.
2. ТСХ-скрининг.
Система растворителей:
хлороформ-ацетон (9:1), при исследовании экстракта из кислой среды.
Способы детекции:
- 5% раствором хлорида железа,
- реактивом Драгендорфа.
Подтверждающие исследования
1. Реакция с нитратом серебра.
В пробирку или выпарительную чашку вносят 3-5 капель хлороформного раствора исследуемого вещества или экстракта, выпаривают досуха. К сухому остатку прибавляют каплю воды и 1-2 капли реактива и нагревают на водяной бане в течение 3-5 мин. Появляется фиолетовая (амидопирин) или сине-зелёная (анальгин) окраска раствора.
2. Реакция с нитритом натрия.
В пробирку или выпарительную чашку вносят 3-5 капель хлороформного раствора исследуемого вещества или экстракта, выпаривают досуха. К сухому остатку прибавляют каплю воды и каплю 10% раствора нитрита натрия. Появляется фиолетовое окрашивание, быстро исчезающее при добавлении избытка реактива (амидопирин) или устойчивая зелёная окраска (антипирин). Анальгин с 1% раствором нитрита натрия даёт синее окрашивание.
3. Реакция с серной и фуксинсернистой кислотами.
В пробирку или выпарительную чашку вносят 3-5 капель хлороформного раствора исследуемого вещества или экстракта, выпаривают досуха. К сухому остатку прибавляют по капле воды, концентрированной серной и хромотропо-вой кислот. При наличии амидопирина наблюдается красное окрашивание, анальгина - красно-фиолетовое.
4. Лигниновая проба.
Хлороформный раствор исследуемого вещества или экстракт наносят на газетную бумагу в присутствии соляной кислоты. Наблюдают жёлто-оранжевое окрашивание при наличии анальгина.
I. Мотивация цели
Широкое применение лекарственных средств и, в частности, производных фенотиазина, пара-аминобензойной кислоты, 1,4-бензодиазепина, средств из группы алкалоидов в медицинской практике создает условия для возникновения отравлений в результате их неквалифицированного или немедицинского использования. Овладение техникой и методиками анализа лекарственных соединений является необходимым при освоении химико-токсикологических методов исследования.
II. Цель самоподготовки
Используя учебный и учебно-методический материал по токсикологической химии, а также знания и умения по базисным дисциплинам изучить методы исследования лекарственных средств основного характера выделенных из объектов биологического происхождения.
IV. План изучения темы
На занятии 1 рассмотреть:
• вопросы токсичности и метаболизма производных 1,4-бензодиазепина;
• схемы исследования.
На занятии 2 рассмотреть:
вопросы токсичности и метаболизма производных фенотиазина;
• вопросы токсичности и метаболизма производных пара-аминобензойной кислоты;
• схемы исследования.
На занятии 3, рассмотреть:
• вопросы токсичности и метаболизма алкалоидов;
• схемы исследования;
приёмы и методы, используемые в экспресс-анализе наркотических соединений и диагностике наркоманий.
V. Рекомендуемая литература
1. Швайкова М.Д. Токсикологическая химия, - М: Медицина, 1975. - С. 160-236.
2. Еремин С.К., Изотов Б.Н., Веселовская Н.В. Анализ наркотических средств: Руководство по химико-токсикологическому анализу наркотических и других одурманивающих средств / Под ред. Б.Н. Изотова. - М.: Мысль, 1993. - 250 с.
3. Крамаренко В.Ф. Токсикологическая химия. - Киев: Выща школа, 1989. - С. 235-294.
4. Крамаренко В.Ф. Химико-токсикологический анализ. - Киев: Выща школа, 1982. - С. 42-46, 136-196.
5. Белова А.В. Руководство к практическим занятиям по токсикологической химии. - М.: Медицина, 1976. - С. 74-124.
6. Лужников Е.А., Костомарова Л.Г. Острые отравления. - М.: Медицина, 1989.-С. 254, 263-272.
7. Конспект лекций.
VI. Блок информации
Обнаружение кокаина
Для обнаружения кокаина проводят микрокристаллоскопические реакции.
1. Реакция с перманганатом калия (МКС). После удаления хлороформа сухой остаток на предметном стекле растворяют в капле 10%-го раствора соляной кислоты и жидкость испаряют при комнатной температуре. Затем к сухому остатку прибавляют каплю 1%-го раствора перманганата калия. Под микроскопом наблюдают кристаллы розово-фиолетового цвета в виде прямоугольных пластинок и сростков из них.
Реакция с платинохлористоводородной кислотой (МКС). Сухой остаток на предметном стекле после удаления хлороформа растворяют в капле 0,1 н. раствора соляной кислоты и добавляют каплю 10% раствора платинохлористо водородной кислоты. Под микроскопом наблюдают сростки кристаллов в виде перистых депдритов светло-желтого цвета.
Тема 2: ПРЕДВАРИТЕЛЬНОЕ ИССЛЕДОВАНИЕ. АНАЛИТИЧЕСКИЙ СКРИНИНГ
I. Мотивация цели
Судебно-химическая экспертиза складывается из предварительного и подтверждающего исследований. Цель предварительного исследования - выявить наличие или отсутствие лекарственных средств в органических экстрактах с использованием скрининговых методов.
Овладение теоретическими основами и практическими навыками проведения аналитического скрининга необходимы провизору для последующей специализации в области судебно-химической экспертизы и клинической токсикологии.
II. Цель самоподготовки
Используя учебный и учебно-методический материал по токсикологической химии, атакже знания и умения по базисным дисциплинам, изучить методы предварительного разделения иобнаружения лекарственных средств.
III. Исходный уровень знаний
Студенты должны знать:
• физико-химические методы, используемые для разделения иобнаружения химических соединений, - хроматография в тонких слоях сорбента.
Студенты должны уметь:
• выполнять хроматографирование в тонких слоях сорбента;
• выполнять обработку хроматограммы цветореагентами и идентифицировать исследуемые соединения;
• рассчитывать абсолютную (Rf) и относительную (Rs) хроматографическую подвижность исследуемых соединений.
IV. План изучения темы
На занятии рассмотреть:
• способы предварительного обнаружения групп лекарственных соединений, экстрагируемых из кислой среды;
• условия ТСХ-скрининга лекарственных соединений кислотного и основного характера, способы обнаружения лекарственных средств на хроматограмме.
V. Рекомендуемая литература
1. Швайкова М.Д.. Токсикологическая химия. - М.: Медицина, 1975. - С. 142-241.
2, Еремин С.К., Изотов Б.Н., Веселовская Н.В. Анализ наркотических средств: Руководство по химико-токсикологическому анализу наркотических и других одурманивающих средств / Под ред. Б.Н. Изотова. - М.: Мысль, 1993. - 250 с.
3. Крамаренко В.Ф, Токсикологическая химия. - Киев: Выща школа, 1989. - С 20-22, 204-295,
4. Крамаренко В.Ф. Химико-токсикологический анализ. - Киев: Выща школа,
1982.-0.9-27,121-197.
5. Белова А.В. Руководство к практическим занятиям по токсикологической химии. - М.: Медицина, 1976. - С. 56-60.
6. Конспект лекций.
VI. Блок информации
Аналитический скрининг
Это научно обоснованная система поиска неизвестного вещества, когда в процессе последовательных операций поэтапно «отсеиваются» отдельные группы веществ и индивидуальные соединения.
Слово «скрининг» в переводе с английского означает «отсеивание».
Аналитический скрининг эффективен при диагностике комбинированных отравлений, а также при ненаправленном анализе.
Требованияк скрининговым методам:
• универсальность;
• специфичность для определенной группы веществ;
• высокая чувствительность (10"8 -10 "!Ог в пробе);
• экспрессность и простота исполнения;
в возможность выполнения серийных анализов;
• возможность стандартизации и совершенствования методов за счет
использования новых материалов, оборудования, расширения списка анализируемых соединений.

Общий скринингпозволяет проводить групповую идентификацию при исследовании веществ, отличающихся по химическому строению и относящихся к различным фармакологическим группам.
Частный скринингнаправлен на обнаружение веществ внутри группы и идентификацию ее отдельных представителей.
К скрининговым методам относятся:
• хроматографические,
• спектральные,
• иммунохимические.
ТСХ- скрининг
В ТСХ-скрининге используют системы растворителей:
• для алкалоидов опия частная система — этилацетат — метанол - 25% раствор гидроксида аммония (17:2:1);
• для веществ из группы наркотических и одурманивающих средств, а также в экспресс-анализе острых интоксикаций - толуол - ацетон - этанол - 25% раствор гидроксида аммония (45:45:7,5:2,5).
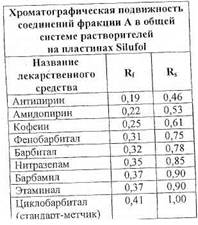
Детектирование (проявление) соединений проводят последовательно. Для фракции А:
• 5% раствор сульфата ртути в концентрированной серной кислоте – барбитураты (белые зоны);
• 0,01% раствор дифенилкарбазона (ДФК) в хлороформе — барбитураты (сине- фиолетовые зоны);
• 10% раствор хлорида железа (III) - производные пиразолона-5 (синие зоны, антипирин - красно-оранжевая зона);
• реактив Драгендорфа - вещества, содержащие третичный азот (оранжевые зоны).
• для барбитуратов частная система — хлороформ — н-бутанол — 25% раствор
• для веществ кислотного, нейтрального и слабо основного характера, содержащихся в «кислом» извлечении (фракция А), - хлороформ-ацетон (9:1);
• для веществ основного характера, содержащихся в «щелочном» извлечении (фракция Б), - диоксан - хлороформ - ацетон - 25% раствор гидроксида аммония (47,5:45:5:2,5);
| гидроксида аммония | (70:40:5); | ||||
| Хроматографическая подвижность I соединений фракции Б в общей системе растворителей на пластинах Silufol | |||||
| Название лекарственного средства | R | Rs | |||
| Пахикарпин | 0,12 | 0,23 | |||
| Атропин | 0,15 | 0,29 | |||
| Эфедрин | 0,18 | 0,35 | |||
| Хинин | 0,25 | 0,49 | |||
| стрихнин | 0.25 | 0,49 | |||
| Этапиразин | 0.51 | 1,00 | | |||
| Антипирин | 0,54 | 1,06 | |||
| Кофеин | 0,56 | 1,10 | |||
| Хлозепид | 0,63 | 1.25 | |||
| Дипразин | 0,66 | 1,30 | |||
| Производные ПАБК | 0,70 | 1,37 | |||
| Тиоридазин | 0,72 | 1,41 | |||
| Аминазин | 0,75 | 1,47 | |||
| Нитразепам | 0,77 | 1,51 | |||
| Амидопирин | 0.83 | 1,63 | |||
| Тизерцин | 0,87 | 1,71 | |||
| Диазепам | 0,95 | 1,87 | |||
Для фракции Б:
- 10% раствор хлорида железа (III) — производные пиразолона-5 (синие зоны, антипирин — красно-оранжевая зона), производные фенотиазина (аминазин, дипразин - розовые, тизерцин - фиолетовая, тиоридазин - зелено-голубая зоны);
- хлорная кислота концентрированная, содержащая 5% раствор нитрита натрия (97:3) — производные фенотиазина (аминазин, дипразин - розовые, тизерцин - фиолетовая, тиоридазин - зелено-голубая зоны);
- 10% раствор серной кислоты - хинин (голубая флуоресценция в УФ-свете)
- реактив Драгендорфа - вещества, содержащие третичный азот (оранжевые зоны).
ВЭТСХ - высокоэффективная тонкослойная хроматография. Высокая эффективность метода достигается за счет применения высокодисперсного сорбента, а высокая чувствительность и экспрессность — более тонкого слоя сорбента.
ГЖХ- газо-жидкостная хроматография. Достоверность определения повышается за счет хроматографирования на колонках, обладающих различной полярностью. Комитет по судебной токсикологии предлагает использовать ко лонки с неподвижными жидкими фазами SE-3O, OV-17, OV- 225. Детектор ионизации пламени.
ВЭЖХ - высокоэффективная жидкостная хроматография. ВЭЖХ или жидкостная хроматография высокого давления является вариантом колоночной жидкостной хроматографии, где элюент подается на колонку под большим давлением, что ускоряет проведение анализа. В качестве детекторов могут быть использованы: спектрофотометрический с переменной (190-700 нм) или фиксированной (254 нм) длинной волны, рефрактометрический, флуори-метрический, ионизации пламени, масс-спектрометрический, электрохимический и т.д. Идентификацию веществ проводят по параметрам удерживания и спектрам поглощения.
Иммунохимические методы
В основе методов лежит специфическая реакция «антиген-антитело», где антигеном является определяемое вещество, чужеродное для организма. Специфическим реагентом является антитело, которое вырабатывается как реакция на внедрение чужеродного вещества. При взаимодействии антигена-яда со специфичным к нему реактивом-антителом образуется комплекс, который выпадает в осадок. Количественно оценить результаты реакции позволяют введение специальных меток. В зависимости от природы метки и способа детектирования выделяют:
• радиоиммунный анализ,
• иммуноферментный (иммуноэнзимный) анализ,
• поляризационный флюороиммунный анализ,
• люминесцентный иммуноанализ.
Иммуноэнзимный метод получил наибольшее распространение. В качестве метки для антигенов используют ферменты - различные оксидазы, способные количественно окислять специальное химическое вещество - хромо-генный субстрат - с образование окрашенных продуктов.
Иммунохимические методы анализа обладают высокой чувствительностью, специфичностью, экспрессностью, простотой исполнения. Реакции проводятся непосредственно в биологических жидкостях и позволяют одновременно диагностировать большое число проб.
VII. Вопросы для самоконтроля
1. Какие этапы включает в себя предварительное исследование? В чём
цель предварительного исследования?
2. Какие химические реакции используются для предварительного обнаружения производных барбитуровой кислоты, пиразолона-5, фенотиазина?
3. Укажите особенности оформления пластинки в ТСХ-скрининге лекарственных и наркотических средств.
4. Объясните цель нанесения на пластинку двух стандартов и двух, порций экстракта в соответствующие зоны пластинки.
Какие стандарты-метчики используются при хроматографическом скрининге экстракта из кислой среды, из щелочной среды?
6. подвижных фаз, используемых в ТСХ-скринкнге.
7. Какие реактивы, и в какой последовательности применяют для обнаружения средств кислотного характера, обнаружения средств основного характера?
8. Что представляет собой реактив Драгендорфа? В чём суть и цель модификации реактива Драгендорфа?
9. Объясните термин «аналитический скрининг».
10.Какие требования предъявляются к скрининговым методам?
VIII. Задания, обязательные для выполнения
| ТСХ-скрининг экстракта из щелочной среды |
Заполнить таблицы: ТСХ-скрининг экстракта из кислой среды
IX. План работы на занятии
Работа на занятии состоит из этапов:
• обсуждение основных этапов исследования лекарственных соединений;
• рассмотрение условий ТСХ-скрининга лекарственных соединений кислотного и основного характера;
• рассмотрение методов обнаружения лекарственных средств на хрома то грамме;
• проведение ТСХ-исследования лекарственных средств изучаемых групп.
X. Лабораторная работа
Проводят хроматографическое исследование хлороформных экстрактов на наличие лекарственных средств. В качестве подвижных фаз используют общие системы для ТСХ-скрининга веществ кислотного и щелочного характера-Условия хроматографирования приведены в блоке информации.
