Спектрофотометрия в УФ-, видимой, ИК-областях спектра в оценке качества ЛС.
Методы анализа антибиотиков
Активность устанавливают диффузионным или турбидиметрическим методами. ГФ XI рекомендует для количественного определения метод диффузии в агар, заключающийся в сравнении действия определенных концентраций испытуемого и стандартного образца антибиотика на тест-микроорганизм.
Поскольку состав агаровой среды и условия выполнения биологического испытания одинаковы, величина зоны диффузии (в которой развитие тест-микроорганизма подавляется антибиотиком) зависит только от химической природы антибиотика и его концентрации.
Единица действия (ЕД) представляет собой меру, которой выражается биологическая активность антибиотиков. За ЕД принимают минимальное количество антибиотика, подавляющего развитие тест-микроорганизма в определенном объеме питательной среды.
К ускоренным микробиологическим методам относят методы, основанные на подавлении изменений рН питательной среды в процессе роста тест-микроорганизмов (уреазный метод).
Сердечные гликозиды - безазотистые соединения растительного происхождения, характеризующиеся кардиотоническим действием. Данные препараты играют исключительно важную роль в терапии больных с острой и хронической сердечной недостаточностью любого генеза. При определении активности лекарственного сырья и многих препаратов сердечных гликозидов используют биологическую стандартизацию. Наиболее часто активность сердечных гликозидов выражают в лягушачьих единицах действия (ЛЕД) и кошачьих единицах действия (КЕД). Одна ЛЕД соответствует минимальной дозе стандартного препарата, в которой он вызывает остановку сердца у большинства подопытных лягушек, кошек, голубей. Так, размельченный порошок листьев наперстянки по активности соответствует такой пропорции: один грамм порошка листьев равен 50-66 ЛЕД или 10-13 КЕД. В процессе хранения активность листьев уменьшается.
Витамины представляют собой группу веществ различной химической структуры, необходимых в малых количествах для нормальной жизнедеятельности организма. Ряд витаминов входят в состав ферментных систем и являются своеобразными биологическими катализаторами химических или фотохимических процессов, происходящих в живой клетке (тиамин, рибофлавин, пиридоксин, пантотеновая кислота и др.).
Для качественной и количественной оценки витаминов в природных источниках используют как биологические, так и физико-химические методы. Принцип оценки биологической активности заключается в том, что животных (крыс, голубей, морских свинок) переводят на диету, содержащую белки, жиры, углеводы, минеральные соли и все витамины, кроме исследуемого. Затем устанавливают, какое количество испытуемого витамина может излечить или предохранить животное от авитаминоза. Параллельно проводят аналогичное испытание со стандартным препаратом.
Биологический метод оценки активности витаминов очень трудоемок, точность его сравнительно невелика. Поэтому для испытания подлинности и количественного определения витаминов обычно используют физические, химические и физико-химические методы.
28. Стабильность и сроки годности ЛС (влияние влаги, CO2, света, кислорода воздуха, примесей).
Под сроком годности лекарственных средств понимают период времени, в течение которого они должны полностью сохранять свою терапевтическую активность, безвредность и по уровню качественных и количественных характеристик соответствовать требованиям ГФ или ФС (ФСП), в соответствии с которыми были выпущены и хранились в условиях, предусмотренных указанными статьями.
По истечении срока годности ЛС не может быть использовано без переконтроля качества и соответствующего изменения установленного срока годности. Существует определенная взаимосвязь между понятием «срок годности», имеющим временной смысл, и понятием «стабильность», обусловливающим качество ЛС (его устойчивость).
Температура – с увеличением увеличивается скорость реакции; с понижением (понижается активность MgSO4, CaCl2, раствора адреналина).
Свет – повышается скорость разложения; кристаллические сухие вещества более устойчивы, чем растворы; изменение цвета при длительном освещении; некоторые вещества сохраняют свою активность (содержащие железо, при этом повышается их стабильность).
Влага – снижает фармакологическую активность; + и – влияет на ЛВ; гигроскопичность.
Окисление — процесс, являющийся одной из причин разложения ЛВ. Некоторые из них (производные фенолов) окисляются, находясь в кристаллическом состоянии. Процесс окисления заметно активизируется при растворении. Особенно легко окисляются ЛВ, проявляющие активные восстановительные свойства (альдегиды, гидразиды, производные фенотиазина и др.).
Система мер, направленных на предохранение ЛВ от окисления, сводится прежде всего к уменьшению влияния атмосферного кислорода или максимальному удалению примесей, катализирующих процесс окисления. Используя окислители, можно смоделировать процесс окисления. Если затем сравнить полученные продукты окисления стандартного образца и продукты разложения ЛВ, то можно сделать заключение о механизме процесса окисления. Это позволяет решать вопрос о путях стабилизации, так как станут известны факторы, влияющие на скорость реакции окисления.
Методы повышения стабильности:
1) физические (твердые вещества – в плотно укупоренной таре; суспензии – в сухом состоянии; инъекции – в ампулах запечатанных);
2) химические (окисление, металлы).
29. Фармакокинетика и биодоступность.
Фармакокинетика – раздел фармакологии о всасывании, распределении, депонировании, метаболизме и выделении ЛВ.
Проведение фармакокинетических исследований возможно только на основе применения современных методов биофармацевтического анализа, позволяющих проследить процесс всасывания и распределения ЛВ в органах и тканях. Они включают выяснение влияния различных биофармацевтических факторов на терапевтическую эффективность ЛВ; изучение их биологической доступности и разработку методов ее определения; создание способов определения ЛВ и их метаболитов в биологических жидкостях.
На фармакокинетику ЛВ оказывают влияние различные факторы: возрастные, генетические, половые, масса тела, питание, беременность, а также различные патологические процессы, например заболевания печени, почек, сердечно-сосудистой системы, желудочно-кишечного тракта, эндокринные, инфекционные и другие заболевания.
Биодоступность – количество неизменного вещества, которое достигло плазмы крови, относительно исходной дозы препарата.
Одним из основных этапов любого исследования биологической доступности ЛС является использование биофармацевтического анализа для определения концентрации ЛВ (метаболита) в биологических жидкостях.
30. Рефрактометрия
Рефрактометрия основана на наличии зависимости величины показателя преломления света от концентрации раствора испытуемого вещества. Показатель преломления зависит также от температуры, длины волны света, концентрации вещества и природы растворителя. Рефрактометрию используют для установления подлинности лекарственных веществ по молярной рефракции. Для количественного определения выбирают интервал линейной зависимости между концентрацией раствора и коэффициентом преломления. В этом интервале концентрацию (х) вычисляют по формуле: х=(n – nO)/F, где n — показатель преломления раствора вещества; nO — показатель преломления растворителя; F — фактор, равный величине прироста показателя преломления при увеличении концентрации вещества на 1% (устанавливается экспериментально).
Рефрактометрические определения выполняют на рефрактометрах, при стабильной температуре (20±0,3ОC) и длине волны линии D спектра натрия (589,3 нм) в диапозоне показателей преломления от 1,3 до 1,7. Прибор юстируют по эталонным жидкостям или воде очищенной, для которой nD20 = 1,3330.
Альдегидная группа
1. + фенилгидразина гидрохлорид в виде солянокислого раствора – образование желтого хлопьевидного остатка фенилгидразона.
2. образование основания Шиффа при взаимодействии с ароматическими аминами.
На третичный атом азота
1. с осадительными (общеалкалоидными) реактивами: Вагнера, Майера, Драгендорфа, раствором пикриновой кислоты, а также с раствором дихромата калия.
На атом фосфора
1. Фосфат-ионы образуют с раствором молибдата аммония желтый осадок фосфор-молибдата.
Количественное определние
Содержание пиридоксальфосфата определяют методом неводного титрования, но без добавления ацетата ртути (II). При этом определении используют растворитель — смесь уксусного ангидрида и муравьиной кислоты, а в качестве индикатора раствор судана III.
Фенольный гидроксил
1. + хлорид железа (III). Растворы (водные, спиртовые или ацетоновые) приобретают зеленое окрашивание.
2. Азосочетание.
3. Обр-ие ауринового красителя
Нитрогруппа
1. После гидрирования нитрогруппы в молекуле нитроксолина до ароматической аминогруппы, выполняют реакцию диазотирования и азосочетания со щелочным раствором β-нафтола. Появляется красно-оранжевое окрашивание.
2. + дифениламин в присутствии концентрированной серной кислоты (синее окрашивание).
3. + гидроксид натрия – образуется ацисоли (красно-оранжевое окрашивание).
Третичный атом азота
1. при нагревании в растворе лимонной кислоты и уксусном ангидриде, то появляется пурпурно-красное окрашивание.
2. с осадительными (общеалкалоидными) реактивами: Вагнера, Майера, Драгендорфа, раствором пикриновой кислоты, а также с раствором дихромата калия (желтый осадок).
Нитроксалин образует окрашенные внутрикомплексные соединения с катионами металлов: магния, кадмия, меди (II), цинка, алюминия.
Количественное определние
Нитроксолин определяют методом неводного титрования, используя в качестве растворителя уксусный ангидрид и титранта — 0,1 М раствор хлорной кислоты. Определение нитроксолина выполняют в присутствии муравьиной кислоты и индикатора малахитового зеленого, а определение хлорхинальдола проводят с индикатором кристаллическим фиолетовым.
Сложноэфирная группа
1. гидроксамовая проба
2. + гидроксид натрия
Фенольный гидроксил
1. + хлорид железа (III) и a,a-дипиридил в смеси этанола и бензола. Появляется красное окрашивание.
2. реакции окисления, сопровождающиеся образованием окрашенных веществ.
1 – при нагревании до 80 C с концентрированной азотной кислотой происходит образование окрашенного в красно-оранжевый цвет.
2 – при добавлении гексацианоферрата (III) калия в щелочной среде образуется окрашенный продукт.
3 – соли церия (IV), железа (III), происходит окисление токоферола до о-, n-токоферилхинона, образование которого обусловливает желтое окрашивание.
Эту химическую реакцию используют для количественного определения токоферола ацетата. Определение основано на кислотном гидролизе (кипячением с обратным холодильником в присутствии серной кислоты). Затем выделившийся токоферол титруют сульфатом церия (IV) (индикатор дифениламин) до появления сине-фиолетового окрашивания.
Производные птеридина
Птеридин - гетероциклическая система, состоящая из двух конденсированных гетероциклов пиримидина и пиразина:
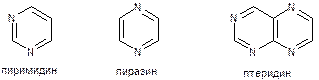
К этой группе относится: Фолиевая кислота.
Кислоту фолиевую хранят в хорошо укупоренной таре, в сухом, темном месте, так как она гигроскопична и разлагается под действием света. Особенно быстро процесс разложения происходит в кислой среде в растворах под воздействием ультрафиолетового излучения.
Требования к условиям хранения различных групп ЛВ находятся в зависимости от их физико-химических свойств и воздействия различных факторов внешней среды. Они регламентируются «Инструкцией по организации хранения в аптечных учреждениях различных групп лекарственных средств и изделий медицинского назначения», утвержденной приказом МЗ РФ №377 от 13 ноября 1996 г.
Метод осаждения
Навеску анализируемого вещества растворяют в воде или другом растворителе и осаждают определяемый элемент реактивом в виде малорастворимого соединения. Полученный осадок отфильтровывают, промывают, высушивают, прокаливают и взвешивают. Зная массу осадка, вычисляют содержание определяемого элемента в массовых долях или процентах от взятой навески.
Осажденной формой называют соединение, в виде которого определяемый компонент осаждается из раствора.
Гравиметрической (весовой) формой называют соединение, которое взвешивают.
Метод выделения
Основан на выделении определяемого компонента из анализируемого вещества и его точном взвешивании.
Метод отгонки
В этом методе определяемый компонент выделяют в виде летучего соединения действием кислоты или высокой температуры.
· Прямая отгонка (определяемый компонент выделяют из пробы в виде газообразного продукта, улавливают и затем определяют его массу).
· Косвенная отгонка (массу газообразного продукта определяют по разности масс анализируемого компонента до и после термической обработки).
В практике фармацевтического анализа этот метод широко применяется при определении влажности лекарственных препаратов, растительного сырья.
Методы анализа антибиотиков
Активность устанавливают диффузионным или турбидиметрическим методами. ГФ XI рекомендует для количественного определения метод диффузии в агар, заключающийся в сравнении действия определенных концентраций испытуемого и стандартного образца антибиотика на тест-микроорганизм.
Поскольку состав агаровой среды и условия выполнения биологического испытания одинаковы, величина зоны диффузии (в которой развитие тест-микроорганизма подавляется антибиотиком) зависит только от химической природы антибиотика и его концентрации.
Единица действия (ЕД) представляет собой меру, которой выражается биологическая активность антибиотиков. За ЕД принимают минимальное количество антибиотика, подавляющего развитие тест-микроорганизма в определенном объеме питательной среды.
К ускоренным микробиологическим методам относят методы, основанные на подавлении изменений рН питательной среды в процессе роста тест-микроорганизмов (уреазный метод).
Сердечные гликозиды - безазотистые соединения растительного происхождения, характеризующиеся кардиотоническим действием. Данные препараты играют исключительно важную роль в терапии больных с острой и хронической сердечной недостаточностью любого генеза. При определении активности лекарственного сырья и многих препаратов сердечных гликозидов используют биологическую стандартизацию. Наиболее часто активность сердечных гликозидов выражают в лягушачьих единицах действия (ЛЕД) и кошачьих единицах действия (КЕД). Одна ЛЕД соответствует минимальной дозе стандартного препарата, в которой он вызывает остановку сердца у большинства подопытных лягушек, кошек, голубей. Так, размельченный порошок листьев наперстянки по активности соответствует такой пропорции: один грамм порошка листьев равен 50-66 ЛЕД или 10-13 КЕД. В процессе хранения активность листьев уменьшается.
Витамины представляют собой группу веществ различной химической структуры, необходимых в малых количествах для нормальной жизнедеятельности организма. Ряд витаминов входят в состав ферментных систем и являются своеобразными биологическими катализаторами химических или фотохимических процессов, происходящих в живой клетке (тиамин, рибофлавин, пиридоксин, пантотеновая кислота и др.).
Для качественной и количественной оценки витаминов в природных источниках используют как биологические, так и физико-химические методы. Принцип оценки биологической активности заключается в том, что животных (крыс, голубей, морских свинок) переводят на диету, содержащую белки, жиры, углеводы, минеральные соли и все витамины, кроме исследуемого. Затем устанавливают, какое количество испытуемого витамина может излечить или предохранить животное от авитаминоза. Параллельно проводят аналогичное испытание со стандартным препаратом.
Биологический метод оценки активности витаминов очень трудоемок, точность его сравнительно невелика. Поэтому для испытания подлинности и количественного определения витаминов обычно используют физические, химические и физико-химические методы.
28. Стабильность и сроки годности ЛС (влияние влаги, CO2, света, кислорода воздуха, примесей).
Под сроком годности лекарственных средств понимают период времени, в течение которого они должны полностью сохранять свою терапевтическую активность, безвредность и по уровню качественных и количественных характеристик соответствовать требованиям ГФ или ФС (ФСП), в соответствии с которыми были выпущены и хранились в условиях, предусмотренных указанными статьями.
По истечении срока годности ЛС не может быть использовано без переконтроля качества и соответствующего изменения установленного срока годности. Существует определенная взаимосвязь между понятием «срок годности», имеющим временной смысл, и понятием «стабильность», обусловливающим качество ЛС (его устойчивость).
Температура – с увеличением увеличивается скорость реакции; с понижением (понижается активность MgSO4, CaCl2, раствора адреналина).
Свет – повышается скорость разложения; кристаллические сухие вещества более устойчивы, чем растворы; изменение цвета при длительном освещении; некоторые вещества сохраняют свою активность (содержащие железо, при этом повышается их стабильность).
Влага – снижает фармакологическую активность; + и – влияет на ЛВ; гигроскопичность.
Окисление — процесс, являющийся одной из причин разложения ЛВ. Некоторые из них (производные фенолов) окисляются, находясь в кристаллическом состоянии. Процесс окисления заметно активизируется при растворении. Особенно легко окисляются ЛВ, проявляющие активные восстановительные свойства (альдегиды, гидразиды, производные фенотиазина и др.).
Система мер, направленных на предохранение ЛВ от окисления, сводится прежде всего к уменьшению влияния атмосферного кислорода или максимальному удалению примесей, катализирующих процесс окисления. Используя окислители, можно смоделировать процесс окисления. Если затем сравнить полученные продукты окисления стандартного образца и продукты разложения ЛВ, то можно сделать заключение о механизме процесса окисления. Это позволяет решать вопрос о путях стабилизации, так как станут известны факторы, влияющие на скорость реакции окисления.
Методы повышения стабильности:
1) физические (твердые вещества – в плотно укупоренной таре; суспензии – в сухом состоянии; инъекции – в ампулах запечатанных);
2) химические (окисление, металлы).
29. Фармакокинетика и биодоступность.
Фармакокинетика – раздел фармакологии о всасывании, распределении, депонировании, метаболизме и выделении ЛВ.
Проведение фармакокинетических исследований возможно только на основе применения современных методов биофармацевтического анализа, позволяющих проследить процесс всасывания и распределения ЛВ в органах и тканях. Они включают выяснение влияния различных биофармацевтических факторов на терапевтическую эффективность ЛВ; изучение их биологической доступности и разработку методов ее определения; создание способов определения ЛВ и их метаболитов в биологических жидкостях.
На фармакокинетику ЛВ оказывают влияние различные факторы: возрастные, генетические, половые, масса тела, питание, беременность, а также различные патологические процессы, например заболевания печени, почек, сердечно-сосудистой системы, желудочно-кишечного тракта, эндокринные, инфекционные и другие заболевания.
Биодоступность – количество неизменного вещества, которое достигло плазмы крови, относительно исходной дозы препарата.
Одним из основных этапов любого исследования биологической доступности ЛС является использование биофармацевтического анализа для определения концентрации ЛВ (метаболита) в биологических жидкостях.
30. Рефрактометрия
Рефрактометрия основана на наличии зависимости величины показателя преломления света от концентрации раствора испытуемого вещества. Показатель преломления зависит также от температуры, длины волны света, концентрации вещества и природы растворителя. Рефрактометрию используют для установления подлинности лекарственных веществ по молярной рефракции. Для количественного определения выбирают интервал линейной зависимости между концентрацией раствора и коэффициентом преломления. В этом интервале концентрацию (х) вычисляют по формуле: х=(n – nO)/F, где n — показатель преломления раствора вещества; nO — показатель преломления растворителя; F — фактор, равный величине прироста показателя преломления при увеличении концентрации вещества на 1% (устанавливается экспериментально).
Рефрактометрические определения выполняют на рефрактометрах, при стабильной температуре (20±0,3ОC) и длине волны линии D спектра натрия (589,3 нм) в диапозоне показателей преломления от 1,3 до 1,7. Прибор юстируют по эталонным жидкостям или воде очищенной, для которой nD20 = 1,3330.
Спектрофотометрия в УФ-, видимой, ИК-областях спектра в оценке качества ЛС.
Используют спектрофотометрические методы анализа по поглощению веществами монохроматического электромагнитного излучения.
Фотометрические методы анализа основаны на использовании закона Бугера-Ламберта-Бера:
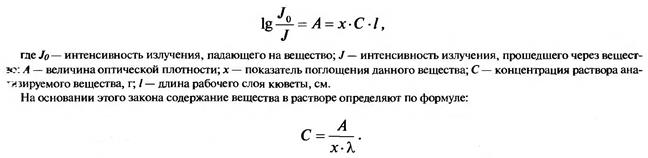
В случае несоответствия закону вначале с помощью стандартного раствора устанавливают зависимость оптической плотности от концентрации, а затем строят калибровочный график, с помощью которого выполняют расчеты.
Диапазоны света:

Спектрофотометрия в УФ- и видимой областях – 1 из широко используемых физико-химических методов в фармацевтическом анализе.
Анализируемые ЛВ должны иметь в структуре молекулы хромофорные группы (сопряженные связи, ароматическое ядро и др.), обусловливающие различные электронные переходы в молекулах и поглощение электромагнитного излучения.
Кривая зависимости интенсивности светопоглощения от длины волны (нм) называется спектром поглощения вещества и является его специфической характеристикой. Измерение спектров поглощения растворов анализируемых веществ в УФ (190-380 нм) и видимой (380-780 нм) областях производят с помощью спектрофотометров различных марок (СФ-26, СФ-46 и др.). В качестве растворителей используют свободные от примесей воду, растворы кислот и щелочей, этанол, хлороформ и другие органические растворители.
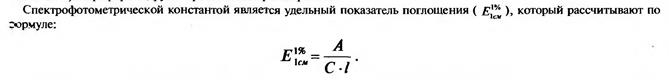
Удельный показатель поглощения представляет собой величину оптической плотности раствора, содержащего 1,0 г вещества в 100 мл раствора, измеренную в кювете с рабочей длиной 1 см. Установив по стандартному образцу величину E и преобразовав эту формулу, можно рассчитать концентрацию анализируемого вещества с относительной погрешностью до ±2%.
Константа измеряется в различных единицах; в молях – молярный коэффициент поглощения, в % - удельный показатель поглощения
Идентификацию ЛВ можно провести по, Е, характеру спектральных кривых в различных растворителях, положению максимума и минимума светопоглощения или их отношению (при различных длинах волн). Для количественного спектрофотометрического анализа важен выбор аналитической полосы поглощения. Последняя должна быть свободна от наложения полос поглощения других компонентов смеси и иметь достаточно высокий удельный показатель поглощения анализируемого вещества.
Спектрофотометрия в ИК-области. Природа полос поглощения в ИК области связана с колебательными переходами и изменением колебательных состояний ядер, входящих в молекулу поглощающего вещества. Поэтому поглощением в ИК-области обладают молекулы, дипольные моменты которых изменяются при возбуждении колебательных движений ядер. Область применения ИК-спектроскопии аналогична, но более широка, чем у УФ-метода. ИК-спектр однозначно характеризует всю структуру молекулы, включая незначительные ее изменения. Важные преимущества ИК-спектроскопии — высокая специфичность, объективность полученных результатов, возможность анализа веществ в кристаллическом состоянии. Для измерения ИК-спектров на однолучевых или двулучевых ИК-спектрофотометрах используют взвеси веществ в вазелиновом масле или помещают анализируемое вещество между пластинами из бромида калия.
Каждый ИК-спектр представляет собой серию полос поглощения, максимумы которых определяются волновым числом, измеряемым в см-1, и определенной интенсивностью. Для анализа ЛB обычно используют спектральную область от 4000 до 400 см-1.
ГФ XI рекомендует два способа установления подлинности по ИК-спектрам. Один из них основан на сравнении зарегистрированных в идентичных условиях ИК-спектров испытуемого ЛB и его стандартного образца. Второй способ заключается в сравнении ИК-спектра испытуемого ЛB с его стандартным спектром, прилагаемым к ФС и зарегистрированным в соответствии с указанными в ней требованиями.
| УФ | Видимый | ИК |
| p-электроны | Функциональные группы | |
| Определение подлинности и количественное определение | Определение подлинности | |
| Истинные растворы | Таблетки |
