Бромирование непредельных соединений
В пробирку поместите 4-5 капель смеси предельных и непредельных углеводородов (керосин) и добавьте при встряхивании 4-5 капель бромной воды. Интенсивно встряхивайте пробирку в течение 10-15 секунд. Отметьте наблюдаемые изменения. Запишите схему протекающей реакции на примере гексена-1.
Окисление алкенов в мягких условиях (реакция Вагнера)
В пробирку поместите 4-5 капель смеси предельных и непредельных углеводородов (керосин) и добавьте 2-3 капли разбавленного раствора перманганата калия. Несколько раз встряхните пробирку. Отметьте наблюдаемые изменения. Запишите схему протекающей реакции на примере гексена-1.
Результаты лабораторных работ оформите в виде таблицы:
| Название опыта | Схема реакции с указанием механизма | Условия реакции (температура, катализатор и т.п.) | Наблюдения (изменение окраски, выпадение или растворение осадка, появление характерного запаха) | Выводы |
Блок информации
Таблица 6
Типы химических связей атомов в молекулах органических
соединений
| Ковалентная | Электровалентная (ионная) | ||
| Неполярная | Полярная | Донорно-акцепторная | |
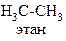 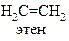 | 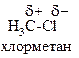 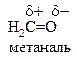 | 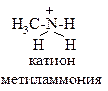 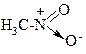 нитрометан (семиполярная связь) нитрометан (семиполярная связь) | 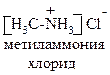 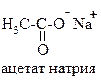 |
Таблица 7
Характеристика ковалентных связей
| Связь | Длина, нм | Энергия, кДж/моль (ккал/моль) | Полярность*, Д |
C-C C=C 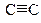 C-N C=N C-N C=N 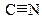 C-O C=O C-F C-Cl C-Br C-I H-C C-O C=O C-F C-Cl C-Br C-I H-C | 0,154 0,133 0,120 0,147 0,127 0,115 0,143 0,123 0,140 0,177 0,191 0,212 0,112 | 347 (83) 606 (145) 828 (198) 305 (73) 615 (147) 876 (210) 334 (80) 694 (166) 426 (102) 326 (78) 284 (68) 213 (51) 414 (99) | 0,5 0,9 3,5 0,8 2,7 1,8 1,6 1,5 1,5 0,3 |
Граф 3
Свойства насыщенных углеводородов (алканов)
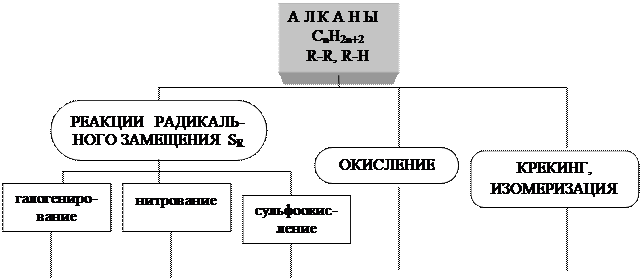
[O],to to
|
|
|
|
| ||||
Граф 4
Свойства ненасыщенных углеводородов ряда этилена (алкенов)
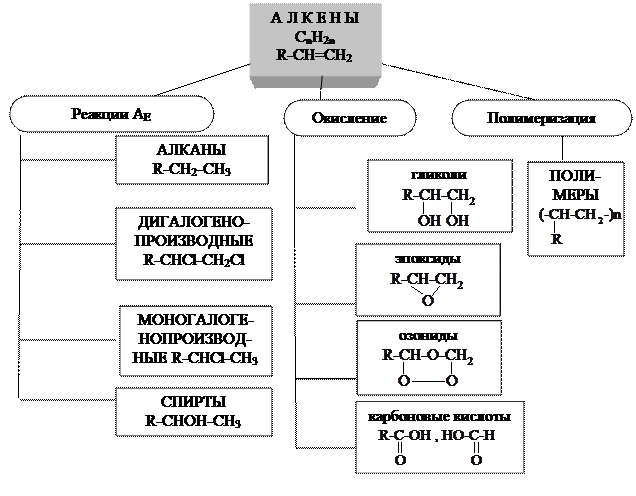
гидрирование
H2, Ni
O,HOH
(KMnO4)
галогенирова-
ние, Cl2
O2, Ag
to
гидрогалогени-
рование, HCl
гидратация O3
H2O, H+
KMnO4
H2SO4
Рисунок 1
Примеры сопряженных систем
Сопряженные системы с открытой цепью сопряжения
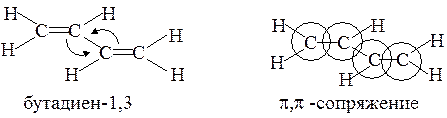
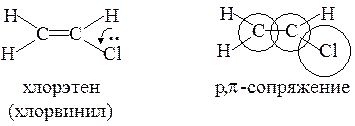
Система с замкнутой цепью сопряжения
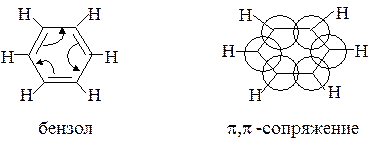
Указания по выполнению самостоятельной работы
Раздел для самостоятельного изучения: Конформационное строение молекул органических соединений. Конформации открытых цепей и их энергетическая характеристика.
Актуальность изучаемого раздела:Пространственное строение молекул тесно связано с физическими и химическими свойствами органических соединений. Особенно важно представление о конформационном строении углеродной цепи при решении вопроса о возможности внутримолекулярного взаимодействия функциональных групп.
План изучения
1. Конформация как геометрическая форма молекулы и как явление. Определение.
2. Проекционные формулы Ньюмена как способ отображения относительного расположения заместителей у соседних атомов углерода. Правила построения проекционной формулы Ньюмена.
3. Энергетический барьер вращения и его причины. Торсионное напряжение, ван-дер-ваальсово напряжение.
4. Энергетические характеристики конформационных состояний: заслонённые, заторможенные, скошенные конформации.
5. Конформации углеродной цепи. Пространственное сближение определённых участков как одна из причин преимущественного образования пяти- и шестичленных циклов.
Вопросы для самоконтроля
1. Изобразите строение и различные конформации, возникающие при вращении вокруг σ-связи C2-C3 в 3-гидроксипропановой кислоте, схематически указав их положение на энергетической кривой.
2. Изобразите в пространстве и на плоскости конфигурацию молекулы этилендиамина (1,2-этандиамина).
3. На одной из стадий цикла Кребса (цикл трикарбоновых кислот) образуется янтарная (бутандиовая) кислота. С помощью проекционных формул Ньюмена изобразите конформации янтарной кислоты по связи
C2-C3. Какая из них энергетически более выгодна?
Форма контроля. Проверка упражнений, тестовый контроль на занятии.
Блок информации для выполнения
самостоятельной работы
Таблица 8
