Углеводы. моносахариды
Мотивация цели. Моносахариды содержатся во всех живых организмах и имеют важное биологическое значение. Остатки моносахаридов входят в состав молекул нуклеиновых кислот, сердечных гликозидов, коферментов. Они являются структурными единицами полисахаридов, выполняющих в организме разнообразные функции. Некоторые моносахариды используются для получения лекарственных препаратов.
Цель самоподготовки.Необходимо усвоить стереоизомерию и таутомерные превращения моносахаридов, их химические свойства.
План изучения материала
1. Классификация и изомерия моносахаридов.
1.1. Классификация по количеству атомов углерода в цепи и по характеру оксогруппы. Примеры.
1.2. Стереоизомерия моносахаридов. Энантиомеры, определение относительной конфигурации. Диастереомеры, эпимеры.
2. Цикло-оксо-таутомерия моносахаридов на примере глюкозы, галактозы, фруктозы, рибозы и дезоксирибозы. α- и β-аномеры. Сравнительная устойчивость таутомерных форм.
3. Свойства моносахаридов, обусловленные открытой таутомерной формой (оксо-формой).
3.1. Реакции окисления моносахаридов:
- окисление слабыми окислителями (гидроксидом меди (II), аммиачным раствором оксида серебра), значение этих реакций для идентификации моносахаридов;
- окисление слабыми окислителями в нейтральной или слабокислой среде (получение гликоновых кислот), глюконат кальция;
- окисление сильными окислителями в кислой среде (получение глюкаровых кислот);
- получение уроновых кислот, их значение.
3.2. Реакции восстановления моносахаридов. Получение ксилита и сорбита. Их значение.
3.3. Качественная реакция на фруктозу (реакция Селиванова).
4. Реакции циклических форм моносахаридов.
4.1. Реакции по полуацетальному гидроксилу. Образование O- и
N-гликозидов, их номенклатура. Условия гидролиза гликозидов.
4.2. Реакции по спиртовым гидроксилам.
- реакции моносахаридов как многоатомных спиртов (взаимодействие с Cu(OH)2);
- реакции алкилирования с образованием простых эфиров;
- реакции ацилирования с образованием сложных эфиров карбоновых кислот;
- образование фосфатов моносахаридов.
5. Отдельные представители моносахаридов и их производных, их значение.
5.1. Пентозы – ксилоза, рибоза, дезоксирибоза, гексозы – глюкоза, манноза, галактоза, фруктоза.
5.2. Аминосахара – глюкозамин, галактозамин.
5.3. Аскорбиновая кислота
Рекомендуемая литература
А - с. 369-400.
А* - с. 377-391, 394-405.
А** - с. 349-363, 367-376
Б – тема 3.2, Обучающие задачи 1, 2, 4 (с. 202-208, 211-213).
Вопросы для самоконтроля(вопросы, обозначенные*, обязательны для выполнения в письменном виде)
1. Приведите проекционные формулы Фишера D-глюкозы, её энантиомера и двух эпимеров. Назовите их. Конфигурация какого атома определяет принадлежность к D- и L-стереохимическим рядам?
2. Приведите формулы Хеуорса α- и β-аномеров глюкопиранозы, галактопиранозы, маннопиранозы, рибофуранозы, 6-фосфата глюкопиранозы, 1,6-дифосфата фруктофуранозы
3*. Приведите схемы реакций:
а) α-D-галактопиранозы с метанолом в присутствии газообразного хлороводорода;
б) β-D-дезоксирибофуранозы с этиламином
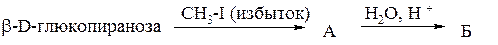 |
в)
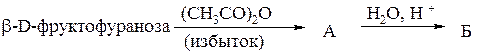 |
г)
Назовите продукты реакций.
4. Какие свойства глюкозы проявляются в реакции «серебряного зеркала»? Какую ещё реакцию можно применить для обнаружения глюкозы?
5*. Приведите схемы реакций получения глюконовой, глюкаровой и глюкуроновой кислот из глюкозы. Укажите условия реакций.
6. С помощью каких реакций можно различить следующие соединения: глюкоза, фруктоза, уксусный альдегид и глицерин?
План работы на предстоящем занятии
1. Определение исходного уровня знаний (тестовый контроль).
2. Разбор основных вопросов темы.
3. Выполнение лабораторной работы:
- Доказательство наличия гидроксильных групп в глюкозе;
- Восстановление гидроксида меди (II) глюкозой в щелочной среде (проба Троммера);
- Восстановление аммиачного раствора оксида серебра глюкозой;
- Реакция Селиванова на фруктозу.
4. Оформление лабораторного журнала, контроль выполнения лабораторной работы.
Лабораторная работа
