Способы приготовления препаратов и методы их исследования
Цель занятия.
После самостоятельного изучения теоретического материала и работы на практическом занятии студент должен знать:
1. Методы исследования структуры и функции клеток
2. Устройство светового микроскопа
3. Правила работы с микроскопом
4.Способы приготовления препаратов для световой микроскопии
5. Принцип работы электронного микроскопа
Приборы и материалы. Демонстрационный микроскоп Nikon Eclipse 50i, микроскоп Биолан, постоянные препараты
План изучения темы
1. Микроскопия
1.1. Световая микроскопия
1.1.1. Устройство микроскопа
1.1.2. Приготовление цитогистологического препарата
1.1.2.1. Взятие и фиксация материала
1.1.2.2. Обезвоживание и уплотнение материала
1.1.2.3. Приготовление срезов
1.1.2.4. Окрашивание препаратов и заключение в консервирующую
среду
1.1.2.4.1. Типы красителей
1.2.Электронная микроскопия
1.2.1. Принцип работы электронного микроскопа
1.2.1.1. Особенности: электронная волна, электромагнитные "линзы"
1.2.1.2. Ход лучей
1.2.2. Особенности приготовления препарата
Краткая теоретическая часть занятия
Приготовление гистологического препарата
| 1. По способу изготовления и характеру взятого материала различают следующие виды гистологических препаратов: а) срезы фиксированных тканей (толщиной 5-15 нм), б) препараты свежезамороженных срезов в) мазки (крови, костного мозга и т.д.) и отпечатки (напр., селезёнки), г) плёнки (брюшины, мягкой мозговой оболочки), или тотальные препараты Чаще всего используются срезы. 2. По длительности хранения: временные препараты, постоянные препараты. 3. Приготовление препарата обычно включает следующие этапы: а) взятие и фиксация материала, б) обезвоживание и уплотнение материала, в) приготовление срезов, г) окрашивание препаратов и заключение в консервирующую среду. |
Взятие и фиксация материала
| 1. Взятие материала от исследуемого объекта. Образец получают несколькими путями: - у живого объекта в результате оперативного иссечения кусочков тканей (биопсия), - от животных, умерщвленных специально для этих целей, - от трупов. Из соответствующего органа вырезают небольшие кусочки (0,5 x 1,0 x 1,0 см) и погружают их в фиксатор (формалин, метанол и т.д.) - обычно на сутки 2. Фиксация производится для предупреждения процессов аутолиза тканей. 3. После фиксации образцы промывают проточной водой в течение нескольких часов. |
Обезвоживание и уплотнение материала
| 1. Затем образцы уплотняют – для последующей их резке на микротоме. Часто в качестве уплотнителя используют парафин или целлоидин. 2. Предварительно образцы обезвоживают (иначе гидрофобный уплотнитель не сможет проникнуть в ткань). а) Для этого их “проводят” по батарее спиртов - 70%, 80%, 96%, 100% этанол - по 24 часа в каждом спирте. б) Т.к. парафин не растворим и в этаноле, образцы выдерживают затем в смеси этанол-ксилол и в чистом ксилоле. 3. Заливка: помещают образцы в смесь ксилол-парафин и затем в жидкий парафин на 1-2 ч при 52-56 о С. Дают парафину, остывая, затвердеть; - вырезают из него блок с заключённым образцом и - закрепляют на деревянном кубике. |
Приготовление срезов
| 1. Кубики (В) вставляют в специальный прибор - микротом, - служащий для приготовления срезов. 2. С помощью микрометрической механической системы (W) объекто-держатель вместе с кубиком перемещается за каждый шаг на определённое расстояние (10 мкм). б) Микротомный нож (К), направляемый под углом к поверхности парафинового блока, срезает с него тонкой слой органа (S) (срез) заданной толщины. 3. Срезы помещают на поверхность тёплой воды для их расправления, а затем - на предметное стекло. | 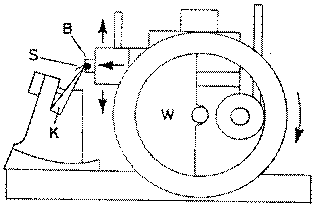 |
1.1.2.4. Окрашивание препаратов и заключение в консервирующую среду
| 1. Перед окрашиванием образцы освобождают от парафина, проводя по батарее растворителей: ксилол, спирт 100 %, 96 %, 80 %, 70 %, 60 %, вода (по 2-5 мин) 2. Для окрашивания предметные стёкла со срезами помещают на короткое время в раствор красителя, промывают водой, обрабатывают раствором другого красителя при необходимости) и вновь промывают водой. 3. Препарат снова обезвоживают (проводя по батарее спиртов с возрастающей концентрацией), а затем просветляют (в карбол-ксилоле и ксилоле) - для удаления лишней краски. |
Типы красителей
Все красители, используемые в гистологической технике, подразделяются на 3 типа.
| Тип красителя | Пример | Окрашиваемые структуры |
| Кислые красители | Кислоты и кислые соли: эозин (искусственная краска; название - от греч. эос - заря); кислый фуксин. | а) Окрашиваемые структуры называются оксифильными (имеющими сродство к кислым красителям). б) Это белковые компоненты цитоплазмы и неклеточные структуры (коллагеновые волокна). |
| Основные красители | Основные соли: гематоксилин (точнее, продукт его окисления - гематеин); азур 2, кармин. | а) Красящиеся структуры - базофильные (сродство к основным красителям). б) Это структуры, богатые нуклеиновыми или иными кислотами – ядра, рибосомы, аморфный компонент межклеточного вещества. |
| Нейтральные красители | Смесь двух красителей: основного (азур 2) и кислого (эозин). | а) Структуры, воспринимающие кислые красители, окрасятся эозином (специфические гранулы в эозинофильных лейкоцитах). б) Ядра всех клеток окрашиваются азуром 2. |
| Индифферент- ные красители | Судан III, Судан IV | Суданом окрашиваются жировые капли |
| 4. Наконец, на препарат наносят каплю канадского бальзама (в случае среза) или кедрового масла (на мазки крови) и накрывают покровным стеклом. |
