Первые представления о биологическом окислении
– А. Лавуазье(XVIII)
Биологическое окисление – это медленное горение.

С химической точки зрения, горение - это взаимодействие углерода
с кислородом с образованием углекислого газа.

В организме механизм образования СО2 -
Декарбоксилирование
Биологическое окисление протекает:
• при низкой температуре;
• в присутствии воды;
• без образования пламени.
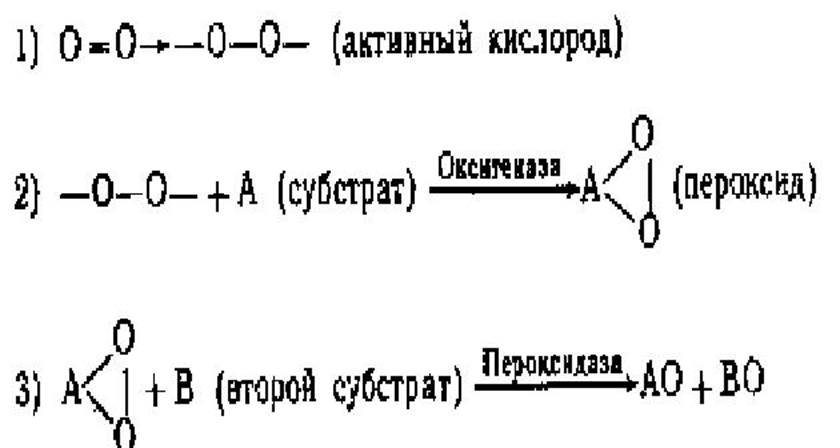
Теория «активации» кислорода
ОБРАЗОВАНИЕ ПЕРОКСИДОВ (акад. А.Н. Бах, Энглер, 1897)
Варбург
Активирование кислорода – ключевой процесс в тканевом дыхании
1912г – цитохромоксидаза
Бателли, Штерн – дегидрогеназы(1912г)
Теория активирования водорода
(акад. В.И. Палладин, 1912)
ДГ
А*Н2 (субстрат)  ½ О2
½ О2  Н2О
Н2О
Кейлин, 1933 – цитохромы –
промежуточные переносчики электронов
от водорода к кислороду
СОВРЕМЕННЫЕ ПРЕДСТАВЛЕНИЯ О БИОЛОГИЧЕСКОМ ОКИСЛЕНИИ

Биологическое окисление - процесс переноса электронов.

Если акцептором электронов является кислород, то такой процесс называется
ТКАНЕВЫМ ДЫХАНИЕМ.

Если акцептором электронов является другое вещество, кроме кислорода, то такой процесс называется
Анаэробным окислением
 Биологическое окисление
Биологическое окисление

• Процесс транспорта электронов
• Процесс многоступенчатый
• Процесс полиферментативный
• Конечный продукт тканевого дыхания – Н2О
• Энергия выделяется постепенно
Биологическое окисление
Многоступенчатый процесс транспорта электронов (на
начальных этапах и протонов)
осуществляемый комплексом ферментов, сопряженный с образованием энергии.
ФЕРМЕНТЫ И КОФЕРМЕНТЫ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ РЕАКЦИЙ
Биологическое окисление начинается с
ДЕГИДРИРОВАНИЯ
Этап осуществляется с помощью:
НАД – зависимые дегидрогеназы ФАД – зависимые дегидрогеназы
Это первичные акцепторы водорода
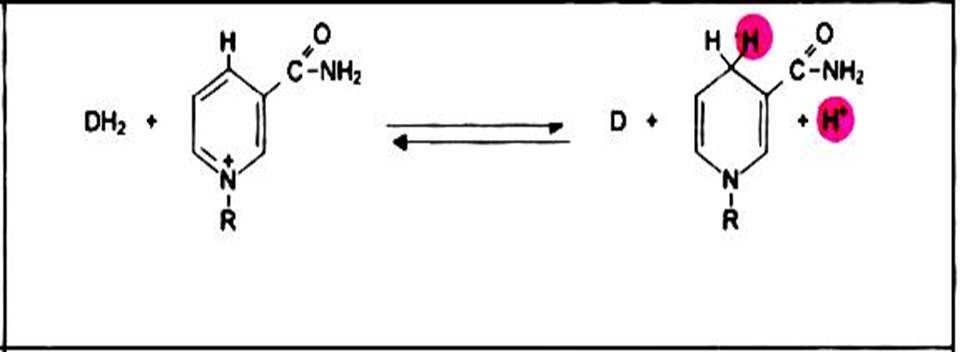
В НАД рабочей частью является витамин
РР - НИКОТИНАМИД.
+2ē +2Н+
-2ē -2Н+
НАД+ (НАДФ+)
Окисленная форма
НАД++ 2Н + + 2ē

НАДН (НАДФН) + Н+
Восстановленная форма
| + |
НАДН+Н
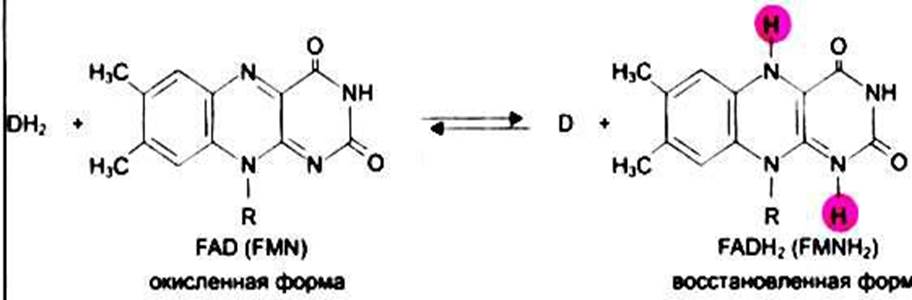
В ФАД и ФМН рабочей частью является ФЛАВИН (изоаллоксазин) – компонент В2
+2ē +2Н+
-2ē -2Н+
| Окисленная форма | Восстановленная форма | |
| + |
ФАД + 2Н + 2ē  ФАДН2
ФАДН2
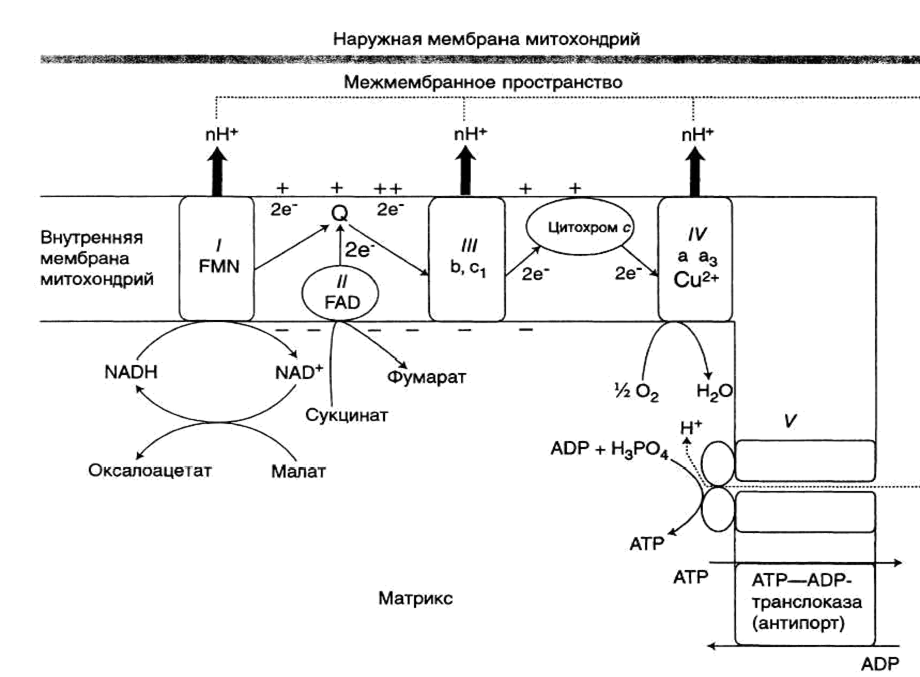
Компоненты дыхательной цепи:
В основном сложные белки, локализованные во внутренней мембране митохондрий и объединенные в комплексы
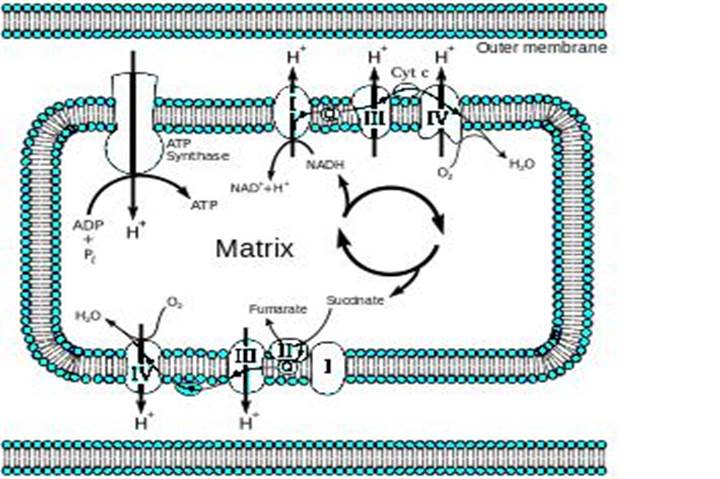
Наружная
 мембрана
мембрана
Внутренняя
ЦТК
Межмембранное пространство
Комплекс ферментов переноса электронов и протонов от субстрата к кислороду называется
ЭЛЕКТРОНТРАНСПОРТНАЯ ЦЕПЬ (ЭТЦ),
Или ЦЕПЬ ПЕРЕНОСА ЭЛЕКТРОНОВ (ЦПЭ)
Или ДЫХАТЕЛЬНАЯ ЦЕПЬ (ДЦ)
Компоненты дыхательной цепи:
• В основном сложные белки, локализованные во внутренней мембране митохондрий и объединенные в комплексы
КОМПОНЕНТЫ ДЫХАТЕЛЬНОЙ ЦЕПИ:
• Комплекс I (НАДН-дегидрогеназа)
• Комплекс II (СДГ)
• Убихинон (кофермент Q)
• Комплекс III (цитохромы b, с1)
• Цитохром с
• Комплекс IV (цитохромы а, а3 – цитохромоксидаза)
Комплекс I (НАДН-дегидрогеназа)
• Флавинзависимый фермент (кофермент ФМН)
• Субстрат – кофермент НАДН2
• Содержит железо-серные белки
• Донор протонов и электронов для убихинона
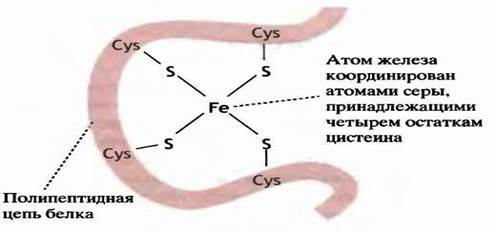
Комплекс II (СДГ)
• Флавинзависимый фермент (кофермент ФАД)
• Донор протонов и электронов для убихинона
Убихинон (кофермент Q)
• Quinone – хинон
• Ubiquitos – вездесущий
• Производное бензохинона с боковой цепью из 10
звеньев изопрена (коэнзим Q10)
• Небелковый компонент ДЦ
• Подвижный компонент
• Акцептор протонов и электронов от флавинзависимых дегидрогеназ
• Донор электронов для комплекса III
• Переносит протоны в межмембранное пространство митохондрий
• Цитохромы – сложные белки, небелковая часть – гем
• Каждый цитохром транспортирует только 1 электрон
• Главную роль в транспорте играет
железо,способное обратимо менять
валентность + e
Fe 3+  Fe2+
Fe2+

- e
Комплекс III
(коэнзим Q – дегидрогеназа)
• В составе цитохромы b, с1
• Акцептор электронов от коэнзима Q
• Донор электронов для цитохрома с
Цитохром с
• Не объединяется в комплекс
• Акцептор электронов от комплекса III
• Донор электронов для комплекса IV
Комплекс IV
(цитохромоксидаза)
• Содержит цитохромы а, а3,способные взаимодействовать с кислородом, ионы меди
• Акцептор электронов от комплекса III
• Донор электронов для кислорода