Декарбоксилирование аминокислот
В) метилирование и др.
Кроме индивидуальных путей обмена, известен ряд превращений, общий почти для всех а/к. Это реакции:
1) на радикал (R): - гидроксилирование;
- разрыв радикала;
- метилирования
Гидроксилирование:
1. При синтезе коллагена одновременно с трансляцией происходит гидроксилирование остатков пролина и лизина, катализируется этот процесс проколлаген-гидроксилазами, имеющими в активном центре атомы железа, в качестве кофермента используется аскорбат (витамин С). Симптомы дефицита витамина С, такие, как выпадение зубов, кровоточивость десен или повреждения кожи (цинга), объясняются нарушением биосинтеза коллагенов. Гидроксилирование пролина и лизина происходит в микросомальной дыхательной цепи при помощи цитохрома Р450, при этом один атом кислорода включается в вещество, а другой, связывая водород из среды, входит в состав воды (см. микросомальную дыхательную цепь)
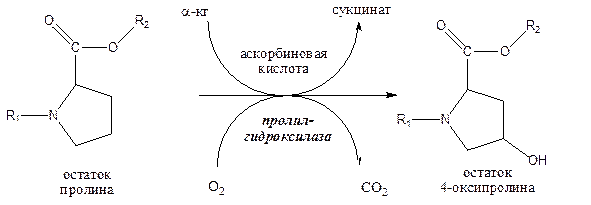
2. При гидроксилировании фенилаланина образуется аминокислота тирозин. Эта реакция катализируется фенилаланингидроксилазой.
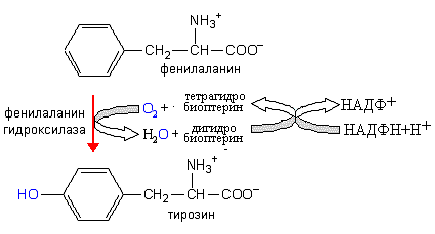
Нарушение функции фенилаланин гидроксилазы – причина фенилкетонурии.
Реакции метилирования:
Метионин на пути своего распада взаимодействует с АТФ с образованием S-аденозилметионина (SАМ). Эту молекулу называют «активный метионин», поскольку он является донором метильной группы в синтезе многих важных для клетки соединений.
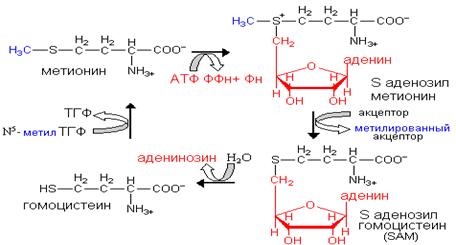 |
После передачи метильной группы образуется S-аденозилгомоцистеин, который путем гидролиза S—С-связи распадается на L-гомоцистеин и аденин.
Реакции разрыва цепи можно рассмотреть на примере триптофана и аригинина:
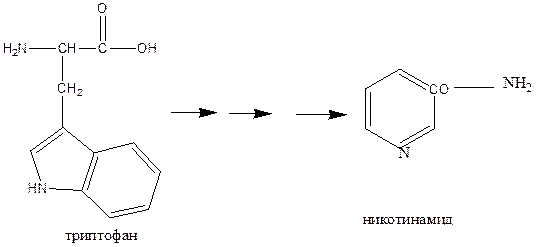
Распад молекулы триптофана до промежуточных продуктов проходит в основном по кинуренин-антранилатному пути, в результате которого после ряда реакций из триптофана образуется никотинамид (витамин РР).
Разрыв цепей аргинина приводит к образованию орнитина и мочевины в цикле синтеза мочевины:
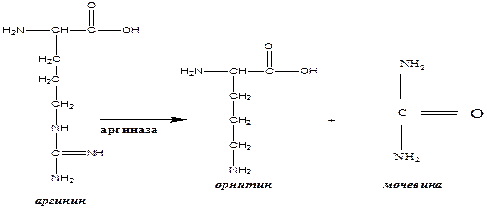
2. Реакции на карбоксильную группу:
а) декарбоксилирование (на примере гис, тир, трп, глу) – механизм, ферменты, биологическая роль;
Б) восстановление – ферменты, биологическая роль.
Декарбоксилирование аминокислот.
Общая схема процесса декарбоксилирования:
R-CH-COOH ---> R-CH2-NH2 + CO2
│
NH2
В живых организмах открыто 4 типа декарбоксилирования:
1. Альфа-декарбоксилирование (отщепляется COO-группа, стоящая по соседству с альфа-углеродным атомом.
R-CH-COOH ---> R-CH2-NH2
│
NH2
2. Омега- декарбоксилирование(характерно для микробов).
Таким путем из АСП образуется альфа-аланин.
HOOC-CH2-CH-COOH ---------> CH3-CH-COOH
│ -CO2 │
NH2 NH2
аспартат аланин
3. Декарбоксилирование, связанное с трансаминированием.
R1 R2R1 R2
│ │ │ │
CH-NH2 + C=O -----------> C=O + CH-NH2
│ │ - CO2 │ │
COOH COOH H COOH
альдегид новая а/к
4. Декарбоксилирование, связанное с конденсацией молекул.
R1 R2 R1
│ │ │
CH-NH2 + CO-S-КоА -----------> CH-NH2 + HSКоА
│ - CO2 │
COOH CO-R2
Реакции декарбоксилирования в отличие от других процессов обмена а/к являются необратимыми. Они катализируются специфическими ферментами - декарбоксилазами а/к, каждая из которых состоит из белковой части и простетической группы, представленной пиридоксальфосфатом.
Реакции декарбоксилирования аминокислот лежат в основе образования биогенных аминов. Продукты декарбоксилирования ароматических аминокислот и глутаминовой кислоты выполняют роль нейромедиаторов:
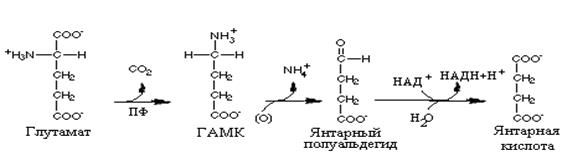
гамма-аминомасляная кислота - медиатор тормозных нейронов-образуется путем декарбоксилирования L-глутамата. Эта реакция катализируется пиридоксальфосфат-зависимым ферментом L-глутамат-декарбоксилазой. Она локализована главным образом в нейронах центральной нервной системы, преимущественно в сером веществе головного мозга.
В животных тканях с высокой скоростью протекает реакция декарбоксилирования гистидина, катализируемая специфической гистидиндекарбоксилазой:
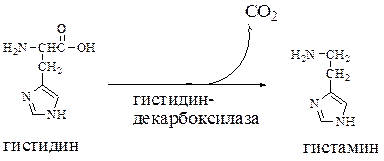
Гистамин - вазодилятатор, образуется в области воспаления, вызывая расширения сосудов в очаге воспаления, тем самым ускоряет приток лейкоцитов, участвует в секреции HCl, является медиатором боли.
В животных тканях с высокой скоростью декарбоксилируются цистеиновая и цистеинсульфиновая кислоты.
CH2-SO2H CH2-SO3H
│ [O] │
CH-NH2 -----> CH-NH2
│ │
COOH COOH
цистеин- цистеиновая к-та
Сульфиновая
К-та
│___ CO2 │____ CO2
│ │
CH2-SO2H [O] CH2-SO3H
│ -----> │
CH2-NH2 CH2-NH2
