Удельная электрическая проводимость растворов электролитов
Электрическая проводимость (электропроводность) обратна сопротивлению: L = 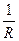 ;
; 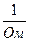 = См (6.1)
= См (6.1)
Единицей измерения в системе СИ является обратный Ом (Ом–1) или сименс, См.
Известно, что сопротивление любого проводника пропорционально его длине и обратно пропорционально сечению, S:
R = ρ • 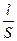 (6.2)
(6.2)
где ρ – удельное сопротивление, Ом•м, характеризующее природу проводника.
Подставляя уравнение (6.2) в уравнение в уравнение (6.1), получаем:
L = 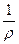 •
• 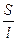 = æ •
= æ • 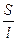
 (6.3)
(6.3)
где æ (каппа) – удельная электрическая проводимость, См/м, величина обратная удельному сопротивлению. Она характеризует свойства проводящей среды – раствора электролита.
Удельная электрическая проводимость представляет собой проводимость 1м3 раствора помещенного между параллельными электродами площадью 1м2, находящимися на расстоянии 1м.
В системе СИ единица измерения удельной электрической проводимости: См/м. В аналитической практике æ часто выражается в См/см.
1См/см = 102 См/м.
Удельная электропроводность максимальна у растворов сильных кислот и оснований из-за их полной диссоциации и высокой подвижности ионов Н+ и ОН–. Наименьшей удельной электропроводностью обладают растворы слабых электролитов из-за низкой концентрации ионов. Удельная электропроводность зависит от концентрации электролита. С повышением концентрации она проходит через максимум, а затем уменьшается. Это связано, для сильных электролитов, с возрастанием мешающего межионного взаимодействия, а для слабых – со снижением степени диссоциации.
Молярная (эквивалентная) электрическая проводимость растворов электролитов.
Молярная электрическая проводимость раствора электролита (λ, лямбда) равна удельной электрической проводимости его раствора с концентрацией 1 моль/м3.
λ = 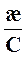 (6.4)
(6.4)
где æ – удельная электропроводность, См/м,
С – концентрация раствора электролита, моль/м3.
В системе СИ λ выражается в См • м2/моль.
λ = 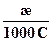 , См∙м2/моль (6.5)
, См∙м2/моль (6.5)
Поскольку в аналитической практике молярная концентрация выражается в моль/л (1моль/л = 103моль/м3), то для расчетов чаще используют формулу (6.6)
λ = 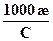 См∙см2/моль (6.6)
См∙см2/моль (6.6)
Влияние концентрации на молярную проводимость электролитов лучше проследить на графике зависимости λ от разбавления (1/С):
|
|
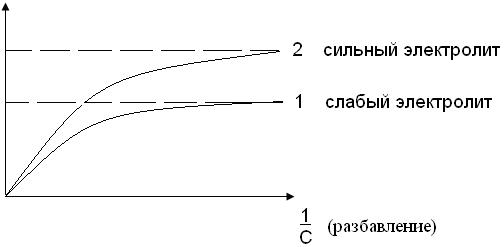
Рис.6.1. Зависимость молярной электрической проводимости от
Разбавления.
С разбавлением растворов электролитов молярная электрическая проводимость увеличивается и стремится к максимальному значению, называемому предельной молярной электрической проводимостью (λ∞).
Для слабых электролитов это объясняется тем, что при бесконечном разбавлении степень диссоциации достигает предельного значения, α =1. Отсюда можно рассчитать степень диссоциации слабого электролита при данной концентрации:
α = 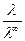 (6.7)
(6.7)
и константу диссоциации:
K = 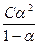 =
= 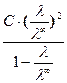 (6.8)
(6.8)
Для сильных электролитов при бесконечном разбавлении ионы удалены друг от друга на такие расстояния, что не мешают при их движении к электродам. Отсюда можно вычислить коэффициент электрической проводимости раствора:
f = λ/λ∞ (6.9)
Предельную молярную электропроводность иона λ∞К+ и λ∞An–можно вычислить и эти значения приведены в справочных таблицах
С помощью закона Кольрауша можно рассчитать предельную молярную электрическую проводимость данного электролита.
Предельная молярная электрическая проводимость электролита равна сумме предельных молярных проводимостей ионов, входящих в его состав. λ∞ = λ∞К+ + λ∞An– (6.10)
Значение λ определяют экспериментально, λ∞ - рассчитывают по закону Кольрауша.
