Костный мозг при некоторых заболеваниях Апластическая анемия
Апластическая анемия — заболевание, характеризующееся глубоким угнетением костномозгового кроветворения, ослаблением пролиферации и задержкой созревания костномозговых элементов с развитием панцитопении. Выделяют формы с поражением всех трех ростков кроветворения (апластическая анемия) и с преимущественным нарушением эритро-поэза при относительно сохраненном лейко- и тромбоцитопоэзе (парциальная форма, крас-ноклеточная аплазия).
Обычно заболевание развивается постепенно. Картина периферической крови характеризуется панцитопенией — анемией, чаще нормохромной, реже (20—22 %) — гиперхромной, тромбоцитопенией, лейкопенией — за счет снижения гранулоцитов с относительным лим-фоцитозом [Романова А.Ф. и др., 1997].
В пунктате костного мозга при апластической анемии число миелокариоцитов (эритро-цитарного и гранулоцитарного рядов) снижено вплоть до полного их исчезновения, с задержкой созревания этих клеток. Отмечают редукцию мегакариоцитопоэза. Наиболее выражено поражение эритроидного ростка. В тяжелых случаях наблюдают значительное уменьшение содержания ядерных элементов с угнетением эритропоэза, гранулоцитопоэза и мегакариоцитопоэза, вплоть до полного опустошения костного мозга. Для получения пунк-тата костного мозга у больных апластической анемией в отдельных случаях необходимо использовать три точки, так как даже при выраженной форме заболевания у больного возможны «горячие карманы» кроветворения.
Иммунный агранулоцитоз
Иммунный агранулоцитоз — заболевание или синдром, при котором возникает преждевременное разрушение клеток гранулоцитарного ряда, вызванное антителами. В периферической крови при иммунном агранулоцитозе снижено количество лейкоцитов до (2—1)109/л с отсутствием гранулоцитов в лейкоцитарной формуле или с резким снижением их количества и явлениями повреждения (пикноз и распад ядер, токсогенная зернистость, вакуолизация). Базофилы отсутствуют, иногда выявляют эозинофилию. Количество эритроцитов,
тромбоцитов, гемоглобина не изменено, за исключением случаев присоединения иммунной гемолитической анемии или тромбоцитопении. В пунктате костного мозга при легких формах агранулоцитоза на фоне сохранившегося гранулоцитопоэза содержание зрелых грануло-цитов снижено. Эритропоэз и мегакариоцитопоэз без изменений. При тяжелом течении агранулоцитоза содержание костномозговых элементов и гранулоцитов уменьшено. Созревание гранулоцитов на ранних стадиях нарушено, плазмоклеточная реакция выраженная. Присутствуют признаки угнетения эритропоэза и мегакариоцитопоэза. В стадии восстановления резкое увеличение в пунктате костного мозга числа промиелоцитов и миелоцитов, а в периферической крови умеренный лейкоцитоз с палочкоядерным сдвигом.
Лейкемоидные реакции
,
Лейкемоидные реакции — патологические изменения состава крови, сходные с картиной крови при лейкозах, но различающиеся по патогенезу. В возникновении лейкемоидных реакций этиологическую роль играют следующие факторы: вирусы, токсины тканевых гельминтов, продукты распада самих клеток крови при гемолизе и клеток опухолей, сепсис и др. При этом возможна гиперплазия кроветворных клеток при нормальных соотношениях элементов в костном мозге.
Лейкемоидные реакции могут быть одноростковые, двух- и трехростковые, миелоидного, эозинофильного, лимфотического, моноцитарного типа, симптоматические эритроцитозы.
Лейкемоидные реакции миелоидного типахарактеризуются картиной периферической крови, напоминающей хронический миелолейкоз. Это наиболее частый тип лейкемоидных реакций. К развитию такого типа реакций могут приводить инфекции (сепсис, скарлатина, рожа, гнойно-воспалительные процессы, дифтерия, пневмонии, туберкулез), ионизирующая радиация, шок, экзогенные и эндогенные интоксикации (прием сульфаниламидных препаратов, лечение кортикостероидами, уремия, отравление угарным газом), лимфогранулематоз, метастазы злокачественной опухоли в костный мозг, острый гемолиз, острая кровопотеря.
В периферической крови умеренный лейкоцитоз с сублейкемическим сдвигом в лейкоцитарной формуле, с токсической зернистостью и дегенеративными изменениями нейтро-фильных гранулоцитов. Количество тромбоцитов в пределах нормы.
Миелограмма характеризуется увеличением содержания молодых клеток нейтрофильно-го ряда с преобладанием более зрелых элементов (миелоцитов, метамиелоцитов). При хроническом миелолейкозе в отличие от лейкемоидных реакций фиксируют резкое увеличение клеточности костного мозга с возрастанием лейкоэритробластического соотношения и мега-кариоцитов. Эозинофильно-базофильная ассоциация, часто наблюдаемая при хроническом миелолейкозе, при лейкемоидной реакции отсутствует.
Лейкемоидные реакции эозинофильного типа.Причинами возникновения этого типа реакций служат в основном гельминтозы — трихинеллез, фасциолез, описторхоз, стронгилои-доз, лямблиоз, миграция личинок аскарид, амебиаз и др. Реже они встречаются при коллаге-нозах, аллергозах неясной этиологии, лимфогранулематозе, иммунодефицитных состояниях, эндокринопатиях.
При данном типе реакции в периферической крови высокий лейкоцитоз — до (40—50)109/л с высокой эозинофилией — 60—90 % за счет зрелых форм эозинофилов.
Исследование костного мозга позволяет провести дифференциальную диагностику этого типа реакции с эозинофильным вариантом хронического миелолейкоза и с острым эо-зинофильным лейкозом. Костномозговой пунктат при лейкемоидной реакции характеризуется наличием более зрелых, чем при лейкозах, эозинофильных клеток и отсутствием бласт-ных клеток, патогномоничных для лейкозов.
 Лейкемоидные реакции лимфатического и моноцитарного типа
Лейкемоидные реакции лимфатического и моноцитарного типа
Инфекционный мононуклеоз— острое вирусное инфекционное заболевание, в основе которого лежит гиперплазия ретикулярной ткани, проявляющееся изменениями крови, реактивным лимфаденитом и увеличением селезенки.
В периферической крови нарастающий лейкоцитоз от 10109/л до 30109/л за счет увеличения количества лимфоцитов и моноцитов. Количество лимфоцитов достигает 50—70 %, моноцитов — от 10—12 до 30—40 %. Помимо этих клеток, могут выявляться плазматические
клетки, атипичные мононуклеары, патогномоничные для данного заболевания. В период ре-конвалесценции появляется эозинофилия. Количество эритроцитов и гемоглобина обычно в пределах нормы и снижается только при инфекционном мононуклеозе, осложненном аутоиммунной гемолитической анемией.
В пунктате костного мозга на фоне нормальной клеточности небольшое увеличение содержания моноцитов, лимфоцитов, плазматических клеток, 10 % из них составляют атипичные мононуклеары.
Симптоматический инфекционный лимфоцитоз— острое доброкачественное эпидемическое заболевание, протекающее с лимфоцитозом преимущественно у детей в первые 10 лет жизни. Возбудитель заболевания — энтеровирус из группы Коксаки 12-го типа.
В периферической крови выраженный лейкоцитоз от (30—70)109/л до 100109/л за счет увеличения количества лимфоцитов до 70—80 %. В 30 % случаев обнаруживают эозинофилы (6—10 %), полисегментацию ядер нейтрофильных гранулоцитов. В миелограмме отсутствует лимфоидная метаплазия.
Симптоматический лимфоцитоз может быть симптомом таких инфекционных заболеваний, как брюшной тиф, паратифы, бруцеллез, висцеральный лейшманиоз и др.
Болезнь кошачьей царапины— острое инфекционное заболевание, возникающее после укуса или царапины кошки. В начале заболевания в периферической крови отмечается лейкопения, которая в период выраженных клинических проявлений сменяется умеренным лейкоцитозом — до (12—1б)-109/л со сдвигом влево. У отдельных больных возможны лимфоцитоз до 45—60 %, лимфоидные элементы, напоминающие атипичные мононуклеары при инфекционном мононуклеозе. Миелограмму обычно не исследуют.
Острые лейкозы
Острый лейкоз — опухоль, состоящая из молодых недифференцированных кроветворных клеток, с обязательным началом в костном мозге.
Для острых лейкозов характерны следующие признаки:клоновый характер (все клетки, составляющие лейкемическую опухоль, являются потомками одной стволовой клетки или клетки-предшественницы любого направления и уровня дифференцировки), опухолевая прогрессия, гено- и фенотипические (морфологические — атипизм, анаплазия, цитохимические — химическая анаплазия) особенности лейкозных клеток.
На основании морфологических особенностей лейкемических клеток в сочетании с их цитохимическими характеристиками острые лейкозы делят на две большие группы:
А. Острый лимфобластный лейкоз (ОЛЛ),происходящий из клеток-предшественниц лимфоидного направления дифференцировки (самая частая форма острого лейкоза у детей — 85 %, у взрослых на его долю приходится 20 %).
Б. Острые нелимфобластные лейкозы (ОнЛЛ),происходящие из миелоидных клеток-предшественниц (у детей они составляют 15 %, у взрослых 80 % от общего количества острых лейкозов).
Диагностика острых лейкозов
Постановка диагноза «Острый лейкоз» требует четкой морфологической верификации. Диагноз может быть установлен только морфологически — по обнаружению несомненно бластных клеток в костном мозге. Для диагностики острого лейкоза безусловно обязательно установление классической структуры ядра бластных клеток (нежно-хроматиновой — тонкосетчатой с равномерным калибром и окраской нитей хроматина).
Изменения в периферической крови.Ценную информацию при всех гемобластозах в первую очередь дает цитоморфологическое изучение клеток периферической крови. При остром лейкозе всем элементам кроветворения свойственны глубокие патологические изменения. В большинстве случаев острого лейкоза развивается анемия. Анемия может быть нормохром-ной, гиперхромной, реже гипохромной и углубляется по мере прогрессирования заболевания (содержание НЬ снижается до 60—20 г/л, а количество эритроцитов — до 1,5—1,01012/л). Другим характерным признаком острого лейкоза является тромбоцитопения (часто ниже критического уровня). Однако на протяжении заболевания и под влиянием лечения содержание тромбоцитов подвергается циклическим колебаниям: в начале болезни оно нередко нормальное, при обострении и прогрессировании уменьшается, в период ремиссии вновь
возрастает. Общее количество лейкоцитов варьирует в широких пределах — от лейкопени-ческих цифр до 100—300-109/л (более высокие показатели фиксируют редко). Лейкоцитоз в момент первичной диагностики острого лейкоза наблюдается менее чем в '/3 случаев, обычно он сопровождается высоким процентом бластных клеток [Владимирская Е.Б. и др., 1998]. Значительно чаще при первичном исследовании крови количество лейкоцитов бывает в норме или обнаруживается лейкопения с относительным лимфоцитозом. Обычно среди лим-фоидных элементов можно выявить бластные клетки, однако возможны случаи, когда типичные бластные клетки в крови отсутствуют. Лейкопенические формы составляют 40—50 % всех случаев острого лейкоза, при этом количество нейтрофилов может уменьшаться до катастрофических цифр (0,2—0,3109/л). Развитие цитопений (гранулоцитопения, анемия, тромбоцитопения) при остром лейкозе является следствием присущего этому заболеванию угнетения нормального кроветворения. Определенное значение в возникновении цитопений имеет аутоиммунный цитолитический механизм, который может осложнять течение любого лейкоза.
Начавшись как лейкопенический, острый лейкоз чаще сохраняет эту тенденцию на протяжении всего заболевания. Однако иногда приходится наблюдать смену лейкопении лейкоцитозом (у нелеченых больных по мере прогрессирования процесса), и наоборот (например, под влиянием цитостатической терапии). Для острого лейкоза характерно так называемое лейкемическое зияние: между клетками, составляющими морфологический субстрат болезни, и зрелыми лейкоцитами нет переходов.
Лейкоз, при котором в периферической крови выявляют патологические бластные клетки, называют лейкемическим, а лейкоз (или фаза лейкоза) с отсутствием бластных клеток в крови — алейкемическим.
Изменения в костном мозге.Пункция костного мозга — обязательное исследование в диагностике острого лейкоза. Исследование костного мозга необходимо и в тех случаях, когда диагноз острого лейкоза не вызывает сомнения уже после анализа периферической крови [Владимирская Е.Б. и др., 1998]. Это обусловлено основным правилом онкологии — только изучение субстрата опухоли дает основание для постановки диагноза.
В костном мозге в период манифестации острого лейкоза обычно преобладают бластные формы (более 60 %), как правило, отмечают резко суженный эритроцитарный росток и уменьшение числа мегакариоцитов с дегенеративным сдвигом в мегакариоцитограмме.
Диагностика цитопенических форм лейкоза затруднительна, так как картина крови часто напоминает таковую при апластической анемии и агранулоцитозе: анемия, лейкопения (гранулоцитопения и относительный лимфоцитоз). На основании костномозговой пункции ставится диагноз. Исключение составляет М7 (мегакариобластный) вариант острого лейкоза, при котором выраженное развитие фиброза костного мозга не позволяет получать полноценный пунктат (клеточность низкая, имеется большая примесь периферической крови). Важным диагностическим методом при данной форме острого лейкоза служит трепа-нобиопсия кости. Гистологическое исследование срезов кости помогает установить выраженную бластную гиперплазию костного мозга.
Диагноз острого лейкоза может быть поставлен в следующих случаях:
• когда бласты составляют не менее 30 % среди всех клеток костного мозга;
• если при преобладании в костном мозге эритрокариоцитов (более 50 %) бласты состав
ляют не менее 30 % среди неэритроидных клеток (при остром эритромиелозе);
• когда в костном мозге преобладают морфологически характерные гипергранулярные
атипичные промиелоциты (острый промиелоцитарный лейкоз).
В других, более редких, случаях обнаружение от 5 до 30 % миелоидных бластов среди всех клеток костного мозга позволяет говорить о диагнозе миелодиспластического синдрома (МДС), а именно о рефрактерной анемии с увеличенным содержанием бластов (ранее эту форму МДС называли малопроцентным острым лейкозом). При установлении лимфоидной природы бластных клеток приходится исключать злокачественную лимфому в стадии генерализации.
Трепанобиопсия костного мозга необходима при дифференциальном диагнозе острого лейкоза и лимфосаркомы. При ОЛЛ инфильтрация бластными клетками бывает диффузной, для лимфосаркомы более характерно гнездное расположение бластных клеток на фоне сохраненной гемопоэтической ткани.
Для идентификации той или иной формы при выявлении повышенного содержания бластных клеток в костном мозге можно использовать алгоритм диагностики острых миелоидных лейкозов (ОМЛ) и МДС, предлагаемый учеными ФАБ-группы (схема 1.1).
 Схема 1.1. АЛГОРИТМ ДИАГНОСТИКИ ОСТРЫХ МИЕЛОИДНЫХ ЛЕЙКОЗОВ (ОМЛ) И МИЕЛОДИСПЛАСТИЧЕСКОГО СИНДРОМА (МДС)
Схема 1.1. АЛГОРИТМ ДИАГНОСТИКИ ОСТРЫХ МИЕЛОИДНЫХ ЛЕЙКОЗОВ (ОМЛ) И МИЕЛОДИСПЛАСТИЧЕСКОГО СИНДРОМА (МДС)
 Исследование лейкоцитарной формулы крови и миелограммы
Исследование лейкоцитарной формулы крови и миелограммы

 Количество эритрокариоцитов (ЭКЦ) среди миелокариоцитов (МКЦ)
Количество эритрокариоцитов (ЭКЦ) среди миелокариоцитов (МКЦ)






 ЭКЦ < 50
ЭКЦ < 50
ЭКЦ > 50







 Процент бластов среди МКЦ
Процент бластов среди МКЦ
Процент бластов среди неэритроидных клеток (НЭК)
  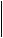                 | Бластов > 30 % МКЦ | ||
| т~ | |||
| ОМЛ: М1-М5; М7 | |||
| Определяем величину моноцитарного и грану-лоцитарного компонента как процент среди НЭК | |||
| \ | г | ||
| Определим один из вариантов ОМЛ: М1-5, 7 | |||
Бластов < 30 МКЦ

 ОМЛ (МЗ) или МДС
ОМЛ (МЗ) или МДС

 Исследуем
Исследуем
морфологические
черты МЗ
| Нет |

 Есть
Есть
| МДС |

 МЗ
МЗ
Бластов < 30 от НЭК

 МДС
МДС
Бластов > 30 от НЭК

 ОМЛ: М5
ОМЛ: М5
Властные клетки при остром лейкозе, несмотря на опухолевую природу, сохраняют известные морфологические и цитохимические черты сходства со своими нормальными аналогами. На этом принципе основана классификация нелимфоидных лейкозов. Установление цитоморфологического варианта острого лейкоза имеет большое значение в проведении дифференцированной химиотерапии.
Изменения в спинномозговой жидкости.Спинномозговая пункция при остром лейкозе — обязательная диагностическая процедура. Цель этой манипуляции - - раннее выявление, профилактика и лечение нейролейкоза. При манифестации острого лейкоза нейролейкоз выявляют в 3—5 % случаев, но обнаружение этого синдрома сразу же заставляет относить такого больного к группе высокого риска, что определяет выбор соответствующей программы лечения. Наличие в спинномозговой жидкости высокого уровня белка, цитоза более 5 клеток в 1 мкл позволяет предположить наличие нейролейкоза. Для окончательного установления диагноза готовят мазки и проводят морфологическое, цитохимическое и иммуноцитоло-гическое изучение клеток.
Острые нелимфобластные лейкозы
В настоящее время широко распространена Франко-американо-британская (ФАБ) классификация острых лейкозов, основанная на морфологических и цитохимических признаках лейкозных бластов. Изучение природы бластов при нелимфобластных лейкозах свидетельствует об их миелоидном происхождении, при этом родоначальницей опухолевого клона всегда является кроветворная стволовая клетка, потомки которой выполняют редуцированную программу дифференцировки.
ФАБ-классификация острых нелимфобластных лейкозов
МО — острый миелобластный лейкоз с минимальной миелоиднойдифференцировкой. При
данной форме лейкоза бласты без зернистости составляют более 30 % миелокариоцитов. Менее 3 % бластов содержат липиды или миелопероксидазу. Бласты относятся к миелоблас-там по результатам фенотипирования (CD13+, CD33+).
Ml— острый миелобластный лейкоз без созревания.Бласты без зернистости или с единичными азурофильными гранулами, могут содержать тельца Ауэра; нуклеолы единичные. Бласты должны составлять 90 % или более из неэритропоэтических клеток. Более 3 % бластов пероксидазоположительны и содержат липиды.
М2— острый миелобластный лейкоз с созреванием.Бласты морфологически и цитохи-мически не отличаются от Ml, составляют от 30 до 89 % неэритропоэтических клеток. Палочки Ауэра, как правило, единичные, обычные. Миелоциты, метамиелоциты и гранулоци-ты могут быть выявлены в вариабельном количестве (более 10 %) и часто имеют ненормальную морфологию. Моноцитарные клетки составляют менее 20 % неэритропоэтических клеток (НЭК).
МЗ— острый промиелоцитарный лейкоз.Большая часть клеток соответствует неопластическим промиелоцитам. Клетки часто разрушены, так что можно выявить свободно расположенные гранулы и палочки Ауэра. Ядра бластов расположены эксцентрично, варьируют в форме и размере, часто состоят из двух долей.
М4— острый миеломонобластный лейкоз.Общее количество бластов в костном мозге составляет более 30 %; при этом более 20 % бластов костного мозга и/или более 5109/л клеток периферической крови — монобласты, промоноциты или моноциты. Диагноз М4 ставят в том случае, когда изменения в костном мозге соответствуют М2, но в периферической крови обнаруживают более 5,0-109/л моноцитарных клеток. Промоноциты и моноциты отличаются отчетливой диффузной реакцией на наличие а-нафтилацетатэстеразы, ингибируемой NaF. Характерным признаком М4 является увеличение концентрации лизоцима в крови и моче более чем в 3 раза.
М5— острый монобластный лейкоз.Бласты составляют более 30 % миелокариоцитов. В костном мозге среди НЭК 80 % и более — монобласты, промоноциты и моноциты. М5 по типу бластов разделяют на две формы:
М5а — монобласты составляют 80 % или более от всех бластов;
М5б — монобласты составляют менее 80 %, а остальные — промоноциты и моноциты, причем последние две формы клеток составляют в среднем 20 % бластов.
Мб— острый эритромиелоз. Вкостном мозге эритрокариоциты составляют более 50 % всех клеток и имеют морфологию с дольчатостью и фрагментацией ядра, многоядерностью, гигантскими формами. Бласты составляют более 30 % НЭК и могут относиться к любому из ФАБ-вариантов бластов, кроме МЗ. Такие эритробласты часто выходят в периферическую кровь. Для эритрокариоцитов характерна диффузно-гранулярная реакция на наличие а-нафтилацетатэстеразы.
М7— острый мегакариобластный лейкоз(введен в ФАБ-классификацию в 1985 г.). Свыше 30 % клеток составляют незрелые, очень полиморфные бласты. Часто сильно базо-фильная цитоплазма бластов образует псевдоподии. Рутинная цитохимия не показательна. Часто бывает миелофиброз.
Особенности отдельных форм острых нелимфобластных лейкозов
Острый миелобластный лейкоз с минимальной миелоидной дифференцировкой (МО)—
бластных клеток в крови от 20 до 97 %, количество нейтрофилов варьирует от 2 до 60 %, лимфоцитов — от 0 до 75 % [Морозова В.Т., 1977]. В костном мозге может наблюдаться тотальная гиперплазия бластных элементов, редукция эритро- и мегакариоцитопоэза. Властные клетки отличаются большим полиморфизмом, встречаются макро- и мезоформы 12—20 нм в диаметре.
Острые миелобластный (Ml, М2) и миеломонобластный (М4) лейкозыимеют практически одинаковые морфологические признаки и не отличаются по клинической картине заболевания. На их долю приходится 62—73 % всех нелимфобластных лейкозов. Вместе с тем острый миеломонобластный лейкоз может быть представлен бластными клетками, принадлежащими к миелобластам и монобластам, однако при этой форме лейкоза бласты чаще имеют цитохимические признаки как моноцитарного, так и гранулоцитарного ряда.
4- 5812
Частота ремиссий при острых миело- и миеломонобластном лейкозах в условиях современной терапии составляет 60—80 % [Владимирская Е.Б. и др., 1998]. Продолжительность ремиссии достигает 12—24 мес, а продолжительность жизни больных может превышать 3 года. В 10 % случаев выздоровление.
Острый промиелоцитарный лейкоз (МЗ).Клеточный субстрат этой формы лейкоза составляют бласты, характеризующиеся обильной азурофильной зернистостью и напоминающие промиелоциты. Размер бластов 15—20 нм, и они имеют большое эксцентрично расположенное ядро неправильной формы, иногда двудольное, нежной хроматиновой структуры. Нуклеола в ядре не всегда четко отграничена. Число бластных клеток, содержащих азурофильную зернистость, не менее 50 %. Считается, что если зернистость обнаруживают в 30—40 % бластов и более — это промиелоцитарный лейкоз, если менее 20 % — миелобластный. Возможны цито-плазматические выросты, которые лишены гранул. Базофилия цитоплазмы выражена в различной степени. В костном мозге тотальная инфильтрация промиелоцитами. Число бластов в крови 40—85 % [Морозова В.Т., 1977]. Эритропоэз и мегакариоцитопоэз резко угнетены.
Острый промиелоцитарный лейкоз встречается в 5—10 % случаев ОнЛЛ. Клиническая картина заболевания характеризуется выраженным геморрагическим синдромом, который появляется на фоне умеренной тромбоцитопении (20—100109/л). Развитие геморрагического синдрома обусловлено диссеминированным внутрисосудистым свертыванием, а также высвобождением гепариноподобных веществ из лейкозных клеток. Прогноз и исходы лечения значительно улучшаются при введении в программу полихимиотерапии даунорубицина и ре-тиноевой кислоты.
Острый эритромиелоз (болезнь Ди Гульельмо, Мб)— редкая форма лейкоза (5 % случаев от всех ОнЛЛ). Изменения в пунктате костного мозга не отличаются от М2.
Картина крови в начале заболевания может быть алейкемической, но по мере развития болезни наступает лейкемизация: в кровь выходят эритрокариоциты или бласты, или и те, и другие. Анемия обычно умеренно гиперхромная, в крови встречаются нормобласты, ретику-лоциты составляют менее 1 %. Лейкопению и тромбоцитопению нередко выявляют уже в самом начале заболевания.
Острые лимфобластные лейкозы
Классификация ОЛЛ (табл. 1.35), разработанная ФАБ, основана на разделении лимфоб-ластных лейкозов по морфологическим особенностям бластов на три типа: микро-лимфоб-ласты (L1), менее дифференцированные клетки (L2), большие клетки, напоминающие им-мунобласты, идентичные опухолевым клеткам при лимфоме Беркитта (L3).
| Таблица 1.35. | Морфологические критерииФАБ классификации ОЛЛ | ||
| Форма ОЛЛ | Размер клетки | Ядро | Цитоплазма |
| L1 L2 L3 | Малый. Популяция гомогенная Состав популяции гетерогенен, преобладают крупные клетки Большие клетки. Популяция гомогенна | Круглое, иногда складчатое. Структура гомогенная, нежная Распределение хроматина может быть нежным и грубым. В ядрах встречаются расщелины, складки, углубления. Одна крупная нуклеола или более Форма ядра овальная или круглая. Грубое распределение хроматина. Одна крупная нуклеола или более | Обычно скудная. Базофилия слабой или средней степени Чаще обильная. Базофилия различной степени выраженности Умеренное количество интенсивно базофильной цитоплазмы с множеством вакуолей |
В костном мозге при остром лимфобластном лейкозе выраженная лимфатическая инфильтрация, с редуцированным эритро- и тромбоцитопоэзом. Основная масса клеток периферической крови и костного мозга характеризуется небольшим размером (9—14 нм) и округлой формой. Бласты более крупного размера имеют большое, расположенное в центре ядро с нежной хроматиновой структурой, занимающее почти весь объем клетки. В ядре определяется одна нуклеола. Цитоплазма имеет различную форму базофилии.
Большого практического значения разделение ОЛЛ на типы в соответствии с ФАБ-классификадией не имеет. Для определения прогноза и выбора оптимальной тактики лечения ОЛЛ более важное значение имеет фенотипическая классификация ОЛЛ, в основе которой лежат представления о стадиях дифференцировки нормальных Т- и В-лимфоцитов. В табл. 1.36 приведена классификация ОЛЛ, разработанная Европейской группой по иммунологической характеристике лейкемий (EGIL).
Таблица 1.36. Иммунологическая характеристика ОЛЛ (EGIL, 1995, по Байдуи Л.В., 1997)
| ОЛЛ Т-линии: CD3+ цитоплазматический или CD34-, но эти маркеры не играют роли в диаг про-Т-ОЛЛ (Т1) пре-Т-ОЛЛ (Т2) кортикальный Т-ОЛЛ (ТЗ) зрелый Т-ОЛЛ (Т4) ОЛЛ В-линии: CD 19+ и/или CD79a+ и/или С пан-В-клеточных маркеров; большинство случ про-В-ОЛЛ (В1) common-B-ОЛЛ (В2) пре-В-ОЛЛ (ВЗ) зрелый В-ОЛЛ (В4) | мембранный (большинство случаев ТдТ+, HLA DR-, ностике и классификации) CD7+ CD2+ и/или CD5+ и/или CD8+ CDla+ CD3+ мембранный, CDla— -D22+ цитоплазматический (экспрессия не менее двух 1ев ТдТ+, HLA DR+, зрелый В-ОЛЛ, часто ТдТ~) нет экспрессии других маркеров CD10+ цитоплазматический IgM+ цитоплазматический или поверхностный К+ или L+ |
В соответствии с фенотипической классификацией выделяют четыре варианта Т-ОЛЛ. Все Т-ОЛЛ отличаются экспрессией в цитоплазме или на мембране Т-лимфоцитов CD3 антигена (+). Про-Т-ОЛЛ (Т1) вариант имеет, кроме цитоплазматического CD3, лишь один мембранный пан-Т-маркер — CD7. Пре-Т-ОЛЛ (Т2) обладают дополнительной экспрессией еще одного или двух пан-Т-маркеров — CD2 и CD5 при отсутствии на мембране CD1 и CD3 (см. также главу 7, раздел «Фенотипирование гемобластозов»).
Для В-лимфоцитов на всех стадиях дифференцировки характерна экспрессия антигенов — CD 19, CD22 и CD79a, которые подтверждают принадлежность лейкозных бластов к В-линии. ОЛЛ из В-лимфоцитов (предшественников) характеризуется также постоянной и высокой экспрессией антигенов гистосовместимости второго класса (HLA DR) и терминальной деоксинуклеотидилтрансферазы (ТдТ). Выделение четырех фенотипических вариантов В-ОЛЛ основано на экспрессии определенных маркеров, приведенных в классификации (common-B-ОЛЛ — CD10, пре-В-ОЛЛ — цитоплазматический IgM и т.д.).
Стадии острого лейкоза
Для определения тактики лечения и прогноза важное значение имеет выделение стадий острого лейкоза. В течение острого лейкоза можно выделить следующие клинические стадии (табл. 1.37).
Начальная стадия острого лейкозанередко диагностируется ретроспективно; чаще клиницист сталкивается с первым острым периодом заболевания (первая атака болезни), который характеризуется выраженным угнетением нормальных ростков кроветворения, высоким бластозом костного мозга, выраженными клиническими проявлениями.
Полная ремиссия— состояния, при которых в пунктатах костного мозга число бластных клеток не превышает 5 %, а лимфоидных (вместе с 5 % бластных) — 40 %. Показатели периферической крови близки к норме. Возможны лейкопения не менее 1,5-10'/л и тромбоцито-пения не ниже 100109/л при тенденции к увеличению числа гранулоцитов и тромбоцитов. Отсутствуют клинические признаки лейкемической инфильтрации печени, селезенки и других органов.
Неполная ремиссияхарактеризуется положительной динамикой заболевания на фоне проводимого лечения: число бластных клеток в костном мозге не более 20 %, исчезновение бластов из периферической крови, ликвидация клинических проявлений нейролейкоза, неполное подавление внекостномозговых очагов лейкемической инфильтрации.
4- 51
Рецидивострого лейкоза — состояния, при которых нарастает число властных клеток в пунктате (более 5 %) и/или развитие внекостномозговых очагов кроветворения.
Терминальная стадия остроголейкоза характеризуется неэффективностью цитостатичес-кой терапии, и на этом фоне нарастают анемия, гранулоцитопения, тромбоцитопения, опухолевые новообразования.
Таблица 1.37. Критерииоценки эффективности терапии острого лейкоза [Ковалева Л.Г., 1978]






 Степень эффекта
Степень эффекта
Клинический статус
Картина крови
Миелограмма
| 2,0-107л Тромбоциты — 50,010^/л Прогрессирование процесса или худшие результаты, чем при клинико-гематологическом улучшении |
Полная клинико-гемато-логическая ремиссия
Неполная клинико-гема-тологическая ремиссия
Клинико-гематологичес-кое улучшение
Отсутствие эффекта
Нормализация (не менее 1 мес)
Нормализация
Значительное улучшение
Нормализация
То же
Гемоглобин — 90 г/л
Зрелые гранулоциты —
t r> in" /„
Властных клеток не более 5 % Властных клеток не более 20 %
Снижение количества бласт-ных клеток по сравнению с исходными значениями
 Хронические лейкозыХронический миелолейкоз
Хронические лейкозыХронический миелолейкоз
Хронический миелолейкоз (ХМЛ) — опухоль, возникающая из полипотентной стволовой клетки, что обусловливает вовлечение в патологический процесс при этом заболевании клеточных элементов всех рядов гемопоэза. Это подтверждают не только наличие патогно-моничной для ХМЛ аномальной Ph'-хромосомы почти во всех делящихся клетках миелопоэ-за (гранулоцитах, моноцитах, мегакариоцитах, эритрокариоцитах) при хроническом миело-лейкозе (у 88—97 % больных), но и лимфобластные кризы с обнаружением Ph'-хромосомы в бластных клетках.
В течении ХМЛ выделяют 3 фазы:
▲Медленная, или хроническая, фаза ХМЛ обычно продолжается около 3 лет.
▲Фаза акселерации длится 1 — 1,5 года. При соответствующем лечении можно вернуть
заболевание в хроническую фазу.
а Финальная фаза ХМЛ — фаза быстрой акселерации или бластного криза (3—6 мес), которая обычно заканчивается смертью.
Несмотря на поражение всех ростков костного мозга, основным пролиферирующим ростком, характеризующимся безграничным ростом в хронической фазе ХМЛ, является гра-нулоцитарный. Повышенная продукция мегакариоцитов и эритрокариоцитов менее выражена и встречается реже.
