Химические свойства аминов
ТЕМА ЛЕКЦИИ: АМИНЫ И АМИНОСПИРТЫ
Вопросы:
Общая характеристика: строение, классификация, номенклатура.
Методы получения
Физические свойства
Химические свойства
Отдельные представители. Способы идентификации.
Общая характеристика: строение, классификация, номенклатура
Аминами называются производные аммиака, молекуле которого атомы водорода замещены на углеводородные радикалы.
Классификация
1– В зависимости от числа замещенных атомов водорода аммиака различают амины:
– первичныесодержат аминогруппу аминогруппу (–NH2), общая формула: R–NH2,
– вторичные содержат иминогруппу (–NH),
общая формула: R1–NH–R2
– третичные содержат атом азота, общая формула: R3–N
Известны также соединения с четвертичным атомом азота: четвертичный гидроксид аммония и его соли.
2– В зависимости от строения радикала амины различают:
– алифатические (предельные и непредельные)
– алициклические
– ароматические (содержащие в ядре аминогруппу или боковой цепи)
– гетероциклические.
Номенклатура, изомерия аминов
1. Названия аминов по рациональной номенклатуре обычно производят от названий входящих в них углеводородных радикалов с присоединением окончания –амин: метиламин СН3–NН2, диметиламин СН3–NН–СН3, триметиламин (СН3)3N, пропиламин СН3СН2СН2–NН2, фениламин С6Н5– NН2 и т. д.
2. По номенклатуре ИЮПАК аминогруппу рассматривают как функциональную группу и ее название амино- ставят перед названием основной цепи:
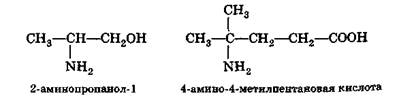 |
Изомерия аминов зависит от изомерии радикалов.
Способы получения аминов
Амины могут быть получены различными способами.
А) Действием на аммиак галогеналкилами
2NH3 + CH3I ––® CH3– NH2 + NH4I
Б) Каталитическое гидрирование нитробензола молекулярным водородом:
3Н2
С6Н5NО2 ––® С6Н5NН2 + Н2О
нитробензол кат анилин
В) Получение низших аминов (С1–С4) путем алкилирования спиртами:
3500C, Al2O3
R–OH + NH3 –––––––––––® R–NH2 +H2O
3500C, Al2O3
2R–OH + NH3 –––––––––––® R2 –NH +2H2O
3500C, Al2O3
3R–OH + NH3 –––––––––––® R3–N + 3H2O
Физические свойства аминов
Метиламин, диметиламин и триметиламин — газы, средние члены ряда аминов — жидкости, высшие — твердые тела. С увеличением молекулярной массы аминов увеличивается их плотность, повышается температура кипения и уменьшается растворимость в воде. Высшие амины в воде нерастворимы. Низшие амины имеют неприятный запах, несколько напоминающий запах испорченной рыбы. Высшие амины или не имеют запаха, или обладают очень слабым запахом. Ароматические амины представляют собой бесцветные жидкости или твердые вещества, обладающие неприятным запахом и ядовиты.
Химические свойства аминов
Химическое поведение аминов определяется наличием в молекуле аминогруппы. На внешней электронной оболочке атома азота имеется 5 электронов. В молекуле амина также, как и в молекуле аммиака, атом азота затрачивает на образование трех ковалентных связей три электрона, а два остаются свободными.
Наличие свободной электронной пары у атома азота дает ему возможность присоединять протон, поэтому амины подобны аммиаку, проявляют основные свойства, образуют гидроксиды, соли.
Солеобразование.Амины с кислотами дают соли, которые под действием сильного основания вновь дают свободные амины:
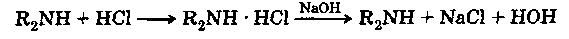 |
Аналогично строению молекулы хлорида аммония можно представить и строение солей аминов:
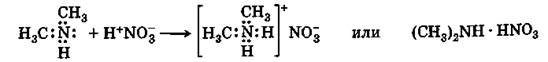 |
Амины дают соли даже со слабой угольной кислотой:
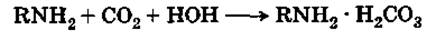 |
Присоединение алкилгалогенидов к третичным аминам идет по той же схеме:
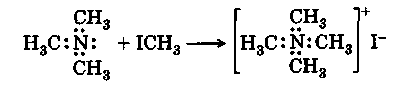 |
Как и аммиак, амины обладают основными свойствами что объясняется связыванием протонов в слабо диссоциирующий катион замещенного аммония:
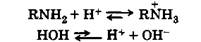 |
При растворении амина в воде часть протонов воды расходуется на образование катиона; таким образом, в растворе появляется избыток гидроксид-ионов, и он имеет щелочные свойства, достаточные для окрашивания растворов лакмуса в синий цвет и фенолфталеина в малиновый. Основность аминов предельного ряда колеблется в очень небольших пределах и близка к основности аммиака.
Эффект метильных групп несколько повышает основность метил- и диметиламина. В случае триметиламина метильные группы уже затрудняют сольватацию образующегося катиона и уменьшают его стабилизацию, а следовательно, и основность.
Соли аминов следует рассматривать как комплексные соединения. Центральным атомом в них является атом азота, координационное число которого равно четырем. Атомы водорода или алкилы связаны с атомом азота и расположены во внутренней сфере; кислотный остаток расположен во внешней сфере.
Ацилирование аминов.При действии на первичные и вторичные амины некоторых производных органических кислот (галогенангидридов, ангидридов и др.) образуются амиды:
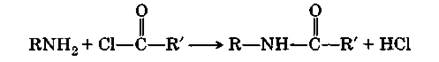 |
Третичные амины в эту реакцию не вступают.
Действие на амины азотистой кислоты.Эта реакция имеет важное аналитическое значение, так как позволяет различать первичные, вторичные и третичные амины неароматического характера.
При действии азотистой кислоты на первичные амины (кроме ароматических аминов) выделяется свободный азот и образуется чаще всего спирт:
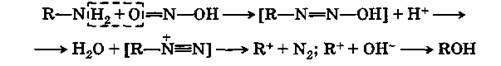 |
Вторичные амины с азотистой кислотой дают нитрозоамины — желтоватые жидкости, мало растворимые в воде:
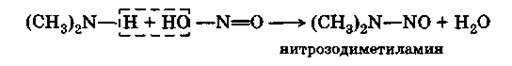 |
При обработке крепкой соляной кислотой нитрозоамины снова дают исходные амины:
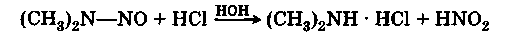 |
Третичные амины устойчивы к действию разбавленной азотистой кислоты на холоду (образуют соли азотистой кислоты), в более жестких условиях один из радикалов отщепляется и образуется нитрозоамин.
Диамины
Диамины играют важную роль в биологических процессах. Как правило, они легко растворимы в воде, обладают характерным запахом, имеют сильно щелочную реакцию, взаимодействуют с С02 воздуха. Диамины образуют устойчивые соли с двумя эквивалентами кислоты.
Этилендиамин(1,2-этандиамин) H2NCH2СН2NН2. Он является простейшим диамином; может быть получен действием аммиака на этиленбромид:
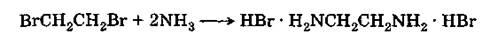 |
Тетраметилендиамин(1,4-бутандиамин), или путресцин, NН2СН2СН2СН2СН2NH2 и пентаметилендиамин (1,5-пентандиамин) NН2СН2СН2СН2СН2СН2NН2, или кадаверин. Они были открыты в продуктах разложения белковых веществ; образуются при декарбоксилировании диаминокислот и названы птомаинами (от греч.— труп), их считали ранее «трупными ядами». В настоящее время выяснено, что ядовитость гниющих белков вызвана не птомаинами, а присутствием других веществ.
Путресцин и кадаверин образуются в результате жизнедеятельности многих микроорганизмов (например, возбудителей столбняка и холеры) и грибков; они встречаются в сыре, спорынье, мухоморе, пивных дрожжах.
Некоторые диамины применяются в качестве сырья для получения полиамидных волокон и пластмасс. Так, из гекса-метилендиамина NН2СН2СН2СН2СН2СН2СН2NН2 получено весьма ценное синтетическое волокно — найлон (США) или анид (Россия).
Аминоспирты
Аминоспирты — соединения со смешанными функциями, в молекуле которых содержатся амино- и оксигруппы.
Аминоэтанол(этаноламин) НО—СН2СН2—NH2, или коламин.
Этаноламин — густая маслянистая жидкость, смешивается с водой во всех отношениях, обладает сильными щелочными свойствами. Hаряду с моноэтаноламином получаются также диэтаноламин и триэтаноламин:
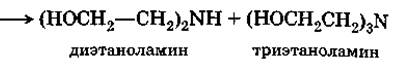 |
Этаноламины широко применяются в технике в качестве эмульгаторов и других поверхностно-активных веществ, а также в различных процессах газоочистки, в том числе для извлечения оксида углерода (IV) из топочных газов при производстве сухого льда (твердой двуокиси углерода).
Холин. Он представляет собой четырехзамещенное аммониевое основание. В нем с атомом азота связаны три метильные и одна окси-этильная группа:
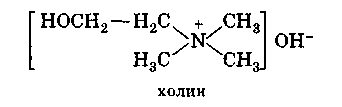 |
Холин входит в состав лецитинов — жироподобных веществ, весьма распространенных в животных и растительных организмах, и может быть выделен из них. Холин представляет собой кристаллическую, весьма гигроскопичную, легко расплывающуюся на воздухе массу. Он обладает сильными щелочными свойствами и с кислотами легко образует соли.
При ацилировании холина уксусным ангидридом образуется холинацетат, называемый также ацетилхолином:
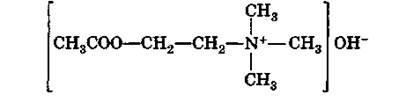 |
Ацетилхолин играет крайне важную биохимическую роль, так как является медиатором (посредником), передающим возбуждение от нервных рецепторов к мышцам.
