Особенности биотрансформации, поступления и выведения ксенобиотиков у разных организмов.
Основные представления о БА и скрининге ксенобиотиков. Примеры скрининга.
Свойство живых систем быть реакционно способным по отношению к любому ксенобиотику приводит к тому, что все химические соединения обладают биологической активностью.
Принцип «попадание-реакция» означает, что любое проявление биологической активности ксенобиотика связано с его способностью пройти путь от внешней среды до мишени, связаться с ней и вызвать ее реакцию.
Начало этого пути – первый контакт химического соединения с биологическим объектом может быть случайным (например, через загрязнение среды) или принудительным (например, введение лекарств), после чего чужеродное соединение и биологический объект взаимодействуют по соответствующим закономерностям.
Биологической активностью ксенобиотика называют его способность изменять функциональные возможности либо компонентов организма (in vitro или in vivo), либо живого организма в целом, либо сообщества организмов.
В практику должны вводиться только те соединения, которые подверглись биологическим испытаниям и только в соответствии с результатами этих испытаний. Таким образом, биологическим испытаниям должны подвергаться все синтезируемые ксенобиотики, т. е. необходимо создать производительную систему их испытаний на разные виды биологической активности.
Проверка большого массива ксенобиотиков на один или несколько видов биологической активности получила название скрининга.
В ХХ в. тотальная проверка большого массива химических соединений или природных объектов, направленная на выявление потенциальных лекарств, получила свое развитие как один из основных методов поиска новых лекарств и вообще химических соединений с заданным типом биологической активности.
Система тестирования ксенобиотиков по видам биологической активности может включать два взаимосвязанных подхода. Первый – уровень целевого объекта испытаний (человек, животное, растение, биогеоценоз), на который должно быть направлено действие искомого ксенобиотика, исходя из целей поиска (лекарства, ветеринарное средство, гербицид и т.д.), и второй подход – совокупность тест-объектов, базирующихся на использовании более примитивной организации живой материи, чем целевой. Использование второго подхода оправдано в тех случаях, когда первый не обеспечивает достаточной производительности и т.д.
Традиционный путь поиска, например, лекарственных средств (точнее, активных субстанций будущих лекарств) в современной фармакологии в довольно схематическом виде выглядит следующим образом. На фармакологических тестах организменного уровня определяют биологическую активность ряда химических соединений, затем улучшают их свойства путем химической модификации в соответствующих рядах соединений. После этого проводят новые испытания модифицированных веществ, снова их улучшают и т.д.; это делается до тех пор, пока указанная процедура не приведет к созданию наиболее эффективного в данном ряду соединения.
Однако эти реальные подходы ограничиваются одним или несколькими видами биологической активности и сравнительно малой выборкой ксенобиотиков из массива.
Изменение селективности мембран
мембрана обладает выраженной селективностью по отношению к различным веществам из-за того, что молекулярные и надмолекулярные структуры мембраны упорядочены. Нарушения этой упорядоченности сказываются на показателях селективности. Пока ПАВ относительно малы, большая часть связывающихся с мембраной молекул «разрыхляет» участки мембраны и каждая из них действует как бы независимо. Поэтому, наступающее снижение селективности примерно пропорционально числу связанных молекул и является суммой отдельных вкладов каждой из них. Но по мере роста концентрации ПАВ молекулы располагаются все плотнее, так что присутствие одной из них усиливает разрушающий эффект другой. Наконец, образуя большие скопления, приводящие в конечном счете к появлению пор, молекулы ПАВ, связанные с мембраной, еще более резко снижают ее селективность.
Активный транспорт
Активный транспорт веществ осуществляется за счет сопряжения электрохимических градиентов либо выполняется молекулярными машинами (АТФазами). Активный перенос происходит с затратой энергии и идет против градиента электрохимического потенциала.
Различают первичный и вторичный (или сопряженный) активный транспорт.
Первичный активный транспорт– трансмембранный векторный перенос веществ осуществляется непосредственно в ходе реакции энергетического преобразования в АТФазных системах или ОВЦ, т. е. используется энергия либо АТФ, либо энергия ОВ реакций. Он подразделяется на:
а) электрогенный активный транспорт – первичный активный перенос веществ через мембрану во время АТФазной или окислительно-восстановительной (ОВ) реакциях, сопровождаемых генерацией электрического потенциала; б) электронейтральный активный транспорт – первичный активный перенос веществ во время АТФазной или ОВ реакциях, не сопровождающихся генерацией электрического потенциала.
Вторичный активный перенос совершается, когда в качестве энергетических источников используются градиенты электрохимических потенциалов других ионов. Например, электрохимический градиент ионов Н+для сопряженного транспорта анионов, сахаров, аминокислот и других веществ в клетку (симпорт или котранспорт) или, напротив, для вывода ионов Na+ из клетки (антипорт или противотранспорт).
Согласно классической модели активного переноса, растворенная молекула соединяется с носителем. По одну сторону мембраны носитель в результате химической реакции, протекающей с поглощением метаболической энергии, например в форме АТФ, видоизменяется таким образом, что он приобретает сильное сродство к подлежащей переносу молекуле и присоединяет ее к себе (активация). Образовавшийся комплекс носителя с этой молекулой проходит через мембрану (переориентируется). Затем происходит вторая химическая реакция, в результате которой сродство носителя к транспортируемой молекуле уменьшается; она высвобождается и выделяется внутрь (релаксация). Затем цикл повторяется. Процессом, идущим с потреблением энергии, является модифицирование структуры носителя.
Наиболее широко в живых системах распространены и изучены Na+/K+–АТФаза (животные клетки и гликофиты, морские водоросли) и Н+–АТФаза, которые могут работать в режиме переноса Н+ и Н+/К+ обмена на плазматических мембранах растительных клеток, митохондрий. Все Na+/K+-АТФазные системы и их препараты имеют ряд общих свойств. Так, для их активации необходим Mg2+; вероятно, в системе имеется два центра связывания катионов – один из них расположен внутри клетки и связывает Na+, а другой – снаружи и связывает К+; оптимум рН составляет ~ 7,5; все эти АТФазы ингибируются различными гликозидами. В оптимальных условиях при расщеплении одной молекулы АТФ происходит перенос ионов со стехиометрией 3 Na+/2K+ (натрий наружу, калий внутрь). работа Н+–АТФазной помпы плазмалеммы растительных клеток:
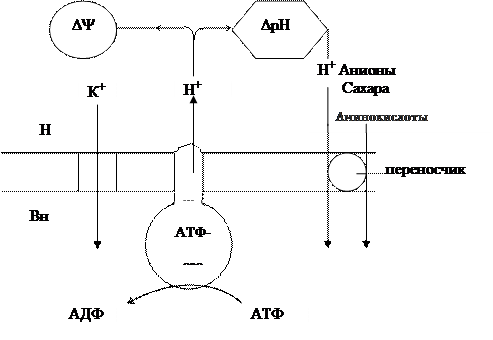 |
Выход протонов из клетки сопряжен с работой Н+–АТФазы плазмалеммы и является активным процессом, в результате которого на мембране создается электрохимический градиент D`mн. Электрохимический градиент любого вещества включает электрическую и концентрационную составляющие. В случае переноса положительно заряженной частицы наружу на мембране устанавливается более высокий по абсолютной величине потенциал DY (внутренняя сторона заряжена отрицательно по отношению к наружной) и изменяется разность концентраций переносимого иона, в данном случае DрН. Создавшаяся ситуация приводит к тому, что калий (или другой положительно заряженный катион) по градиенту электрохимического потенциала, а протон по градиенту концентрации входят в клетку. При своем движении внутрь клетки протон активирует переносчик, транспортирующий либо анион, либо аминокислоты, либо другие соединения.
Вторичный активный транспорт приводится в действие за счет энергии, запасенной в градиентах веществ, а не путем прямого гидролиза АТФ. Все они работают как котранспортные системы: одни функционируют по принципу симпорта, а другие – по принципу антипорта. В животных клетках котранспортируемым ионом обычно оказывается Na+. Например, активный транспорт некоторых сахаров и аминокислот внутрь животных клеток обусловливается градиентом Na+ через плазматическую мембрану. Всасывание глюкозы в клетки кишечника и почек достигается с помощью системы симпорта, в которой глюкоза и ионы Na+ связываются с различными участками на белке-переносчике глюкозы; Na+ стремится войти в клетку по своему электрохимическому градиенту и активирует переносчик, перемещающий глюкозу внутрь. Чем выше градиент Na+, тем больше скорость всасывания глюкозы. Наоборот, если концентрация Na+ во внеклеточной среде заметно уменьшается, транспорт глюкозы останавливается. Ионы Na+, проникающие в клетку вместе с глюкозой, выкачиваются обратно Na+/К+–АТФазой, поддерживающей градиент концентрации Na+.
благодаря вторичным механизмам клетки получают большие преимущества, если в качестве источника энергии могут использовать градиент электрохимического потенциала ионов. Однако при рассмотрении механизмов сопряжения потоков ионов и неэлектролитов (нейтральных молекул) необходимо помнить, что если выделяемые из клетки ионы (Н+ или Na+) способствуют транспорту углеводов, аминокислот, сахаров и др. веществ, то для каждой такой системы требуется отдельный переносчик, узнающий специфический субстрат.
В переносе веществ через мембраны принимают участие редокс-цепи мембран, т. е. окислительно-восстановительные реакции (например, ОВ дыхательной цепи). Исходным звеном РЦ выступают восстановленные пиридиннуклеотиды, а конечным акцептором электронов является О2.
По данному механизму транспортируются как галактоза, арабиноза, глюкоза-6-фосфат, глюконат и глюкуронат, большинство природных аминокислот
В теории транспорта с участием ОВ систем имеются свои проблемы, связанные, в частности, с тем, что окисление разных транспортируемых веществ должно идти разными путями. С другой стороны, многие факты, рассматриваемые как аргументы в пользу ОВ транспорта, можно объяснить в рамках другого механизма (например, протон-движущей силы).
31.Адсорбция
Многие ксенобиотики действуют непосредственно на поверхность клетки, адсорбируясь на клеточной поверхности (мембране). Адсорбирующая поверхность в клетке может на несколько порядков превышать объем. Белки и крупные молекулы в растворе находятся в коллоидном состоянии и обеспечивают огромную поверхность для адсорбции. Так, например, площадь поверхности белков, содержащихся в 1 см3 сыворотки крови человека, составляет 100 м2. С другой стороны, физико-химические характеристики веществ после их адсорбции на мономолекулярной пленке отличаются от их свойств в растворе, что имеет большую биологическую значимость. Когда говорят об адсорбции какого-либо вещества, подразумевают, что оно обратимо концентрируется на поверхности. Адсорбция определяется суммой всех химических связей, образующихся между молекулами или молекулами с поверхностью. Процесс адсорбции обусловлен теми же типами связей (в особенности ван-дер-ваальсовыми, водородными и ионными), что и химические реакции, происходящие во всем объеме вещества. Поверхность обладает двумя особенностями: Во-первых, на поверхности создается 100 % концентрация вещества. Поскольку адсорбируемое вещество обладает ничтожной растворимостью (растворимое не локализовалось бы на поверхности, а распределялось бы по объему), то при такой его концентрации вероятность химического взаимодействия значительно возрастает. Другая особенность поверхности заключается в том, что она содержит ненасыщенные валентности, которые в твердом веществе затрачиваются на связывание друг с другом составляющих его атомов.
На молекулу, которая адсорбируется из раствора на поверхности, действуют силы, стремящиеся возвратить ее в раствор. Мерой способности вещества возвращаться в среду является его растворимость, которую можно рассматривать как меру способности данного вещества десорбироваться.
Адсорбцию на поверхности подразделяют на неспецифическую и специфическую. Неспецифическая адсорбция характерна для веществ амфифильной природы, имеющих концевую гидрофильную группу, связанную с относительно большим гидрофобным остатком. Такие вещества занимают любую доступную им поверхность независимо от химической природы и физических свойств. В сосуде, содержащем мыльный раствор, мыло накапливается не только на поверхности раздела воздух–вода, но и на поверхности стекло–вода. Более того, мыло адсорбируется на любых предметах, погруженных в мыльный раствор. Это пример типичной неспецифической адсорбции, при которой нейтральные молекулы адсорбируются сильнее, чем ионы. Это происходит потому, что ион гидратируется сильнее, чем соответствующие неионизированные молекулы, и поэтому последние легче вытесняются из воды. Специфическая адсорбция свойственна гидрофобным веществам, которые стремятся разместиться на поверхности, имеющей химически комплементарный характер. Простейший пример – притяжение аниона к положительно заряженному участку поверхности, а катиона – к отрицательно заряженному. В таких случаях ион будет адсорбироваться сильнее, чем неионизированная молекула. Если при адсорбции не происходит образования ковалентных связей, то это обратимый процесс, и положение его равновесия устанавливается в соответствии с законом действующих масс. При выводе соотношения были сделаны следующие предположения:- энергия адсорбции постоянна и не зависит от степени заполнения поверхности;- адсорбция происходит на локальных центрах, и адсорбированные молекулы между собой не взаимодействуют;- максимальная возможная адсорбция соответствует полному заполнению монослоя.
Число молей вещества Г, адсорбированного на поверхности, выражается в виде функции равновесной концентрации вещества С в растворе.
С
Г = Гmax –––––– , (4.1)
Ксд + С
где Ксд – константна сорбции-десорбции; Гmax – число молей растворенного вещества, адсорбированного на поверхности адсорбента с образованием полностью заполненного монослоя; С – концентрация ксенобиотика в растворе.
Изотерму Лэнгмюра можно представить в линейной форме:
1 1 Ксд
––– = –––– + –––––– . (4.2)
Г Гмах Гмах С 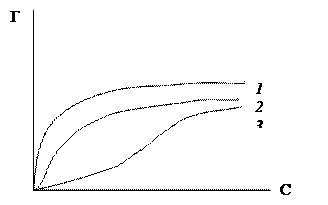 Это уравнение показывает, что адсорбент насыщается при высоких значениях С, т. е. при образовании монослоя. Это так называемая изотерма адсорбции. При адсорбции различных агентов часто наблюдается
Это уравнение показывает, что адсорбент насыщается при высоких значениях С, т. е. при образовании монослоя. Это так называемая изотерма адсорбции. При адсорбции различных агентов часто наблюдается
такое явление, когда биологический эффект от каждого последующего удвоения становится все
менее ощутимым, при этом кривая зависимости
эффекта от дозы также представляет собой гиперболу. Известно несколько типов кривых, характеризующих процесс адсорбции: 1. L-кривые, нормальные изотермы Лэнгмюра, характеризующие адсорбцию молекул, ориентированных на поверхности горизонтально. Чем больше вещества адсорбировано, тем более затруднена дальнейшая адсорбция. 2. S-кривые, соответствующие вертикальной ориентации молекул относительно поверхности. На этапе, который характеризуется начальным участком сигмоидной кривой, чем больше вещества уже адсорбировано, тем легче происходит дальнейшая адсорбция. Этот эффект получил название кооперативного.3. Н-кривые, характеризующие случаи с высокой степенью сродства; на этих кривых начальные значения концентраций адсорбированного вещества очень велики; такие кривые часто получаются, если вещество адсорбируется в виде мицелл, а также при адсорбции ионов, имеющих высокую степень сродства и способных обмениваться с ионами, обладающими малой степенью сродства. Выделяют еще С-кривые, соответствующие линейной зависимости между константами распределения в тех случаях, когда вещество проникает в адсорбент легче, чем растворитель.
32. Экологическая и токсикологическая характеристика оксидов азота, серы ифторсодержащих углеводородов.Немалую опасность представляет также и попадание в атмосферу окислов азота и серы, образующихся при сжигании ископаемого топлива. Количество выбросов окислов азота вместе с аммиаком оценено приблизительно в 200-350 млн т в год.Часть присутствующих в атмосфере оксидов (NO, SO) и диоксидов (N02, S02) азота и серы образуются в ходе естественно протекающих природных процессов - вулканических извержений, разрядов атмо-сферного электричества, жизнедеятельности микроорганизмов. Из ежегодно накапливающихся в биосфере оксидов азота на долю при-родных процессов приходится 1100 млн т этих соединений, антропо-генная часть составляет еще около 53 млн т.Следует помнить об образовании оксидов азота внутри помещений, накапливающихся в результате эксплуатации бытовых газовых приборов. Немалый вклад в их накопление вносит и курение. Основную токсикологическую опасность из окислов азота пред-ставляют диоксиды азота. В концентрации 100 мкг/м3 диоксид не вы-зывает каких-либо морфологических изменений в органах дыхания у крыс. Однако повышение концентрации диоксида азота до 600 мг/м3 в организме животных приводит к развитию бронхита и начальным проявлениям пневмосклероза.Длительное воздействие диоксида азота вызывает целый спектр изменений физиологических систем организма животных (нарушение рефлекторной деятельности, гематологические изменения и т. д.). Ди-оксид азота в концентрациях 40-140 мг/м3 при экспозиции не более часа может вызывать развитие бронхита и бронхопневмонии.Наиболее опасное проявление острого отравления оксидами азота - отек легких. Убедительных данных о канцерогенности, мутагенности и тератогенности оксидов азота в настоящее время не имеется. По существующим дан-ным, ежегодно в результате деятельности человека вырабатывается около 150 млн т серы, преимущественно в результате утилизации ис-копаемого топлива. При выплавке меди, свинца и цинка количество образующегося диоксида серы достигает 15 млн т.Определенное количество выброшенных в атмосферу окислов азота и серы удаляется в результате сорбции почвой, растительным покро-вом, водой и кислотных дождей. Последние снижают интенсивность фотосинтеза, вызывают гибель наземных растительных сообществ, подкисление водоемов и связанную с ним гибель гидробионтов.Воздействие оксидов серы на дыхательные пути приводит к увеличению респираторных заболеваний у населения, ослабляет иммунную защиту у людей и животных и т. д. При накоплении в атмосфере фторсодержащих углеводородов уменьшается содержание озона. Общие выбросы углеводородов в ат-мосферу составляют не менее 200 млн т в год; особенно опасны для живых организмов, объединенных общей областью распространения (биоты), полициклические ароматические углеводороды, в частности бенз(а)пирен, образующиеся при сгорании различных видов топлива и других высокотемпературных процессах и вызывающие мутагенные и канцерогенные эффекты.
33. Экологическая и токсикологическая характеристика тяжелых металлов.
Например, 1,5-2 тыс. т ртути ежегодно поступает в биосферу при переработке минералов и руд, 0,1-8 тыс. т - при сжигании топлива; ежегодно в биосферу при сжигании угля попадает около 3,5 тыс. т свинца, 56 тыс. т - в результате выветривания и 110 тыс. т выносят реки.Степень токсичности тяжелых металлов для человека и животных, а также для растений неодинакова и колеблется в весьма широких пре-делах. Так, цинк, титан характеризуются низкой токсичностью для человека и теплокровных животных, но даже в низких концентрациях они оказывают губительное действие на рыб и других обитателей водных экосистем.Наиболее часто металлы, в том числе и высокотоксичные, попадают в окружающую среду в результате промышленных сбросов в водоемы со сточными водами, не прошедшими эффективной очистки, а также использование пестицидов, в состав которых они входят.Для поврежде-ния механизмов природного самоочищения водоемов бывает доста-точным даже кратковременное повышение концентрации металлов в водной экосистеме, что весьма существенно при организации мониторинга тяжелых металлов в сточных водах.КадмийВесьма важным является фактор длительности воздействия кадмия на организм человека и животных в связи с его способностью накапливаться в печени, почках, поджелудочной и щитовидной железах и др. Кадмий характеризуется выраженной нефротоксичностью при попадании в организм с питьевой водой.Высокой чувствительностью к действию кадмия характеризуются водные организмы. Так, пребывание рыб (гуппи, карп, карась и др.) на протяжении суток в воде с содержанием Cd2+ 0,001-0,3 мг/л приводит к их гибели.
СвинецЕжегодно в земную атмосферу выбрасывается около миллиона тонн его соединений, значительная часть которых водорастворима, что обу- словливает экологическую опасность РЬ . Основной источник - эти-лированный бензин. Токсикологическая опасность свинца усугубляет-ся его активным всасыванием в пищеварительном тракте человека и животных, значительным объемом распределения в тканях и накоплением в костях. Депонированный в костях свинец способен поступать в кровь, с током которой доставляется в различные органы. В наибольшей степени опасному воздействию свинца подвергаются рабочие, занятые на его добыче в шахтах, а также при выплавке. В этом случае металл поступает в организм ингаляционным путем.Примерно 35 % свинца, попавшего в дыхательные пути человека, оседает в легких. Около 10 % свинца, поступившего с продуктами пи-тания в пищеварительный тракт, всасывается. Выведение свинца из организма человека осуществляется преимущественно (более 70 %) почками и в меньшей мере через пищеварительный тракт (~ 10 %).Определенную роль в накоплении свинца в экосистемах играют растения, получающие металл не только из атмосферы, но и из почвы. свинец об-наружен в листьях салата и бобов, но практически отсутствует в томатах, кочанной капусте, картофеле и моркови.Свинцовая интоксикация вызывает нарушение биосинтеза гемогло-бина на уровне ингибирования левулинатдегидратазы и гемсинтетазы. Имеются сведения о нарушении синтеза цитохрома Р-450 при свинцовой интоксикации.Главной мишенью воздействия свинца при хронических отравлени-ях являются центральная и периферическая нервные системы (свинцовая энцелопатия: появление головной боли, нарушение сна, памяти, возникновение тремора, галлюцинаций и т. д.). Для различных вариантов отравления свинцом характерно поражение почек, пищеварительного тракта.
Ртутьи ее соединения относятся к веществам общетоксического действия, вызывающим у людей летальный исход, попадая в организм с питьевой водой в количестве 75-300 мг в сутки. Наиболее токсична двухлористая ртуть (сулема), однократная летальная доза которой со-ставляет для человека р,2-0,5 г. Ртуть характеризуется высокой нефро- токсичностью, приводящей к быстро развивающейся почечной недос-таточности. Выведение ртути осуществляется почками, через пищеварительный тракт, потовыми и молочными железами.Начиная с концентрации 0,006-0,01 мг/л ртуть в виде водораство-римых солей оказывает губительное влияние на рыб и другие водные организмы.При отравлениях ртутью, особенно ее органическими соединения-ми, отчетливо выражены симптомы поражений нервной системы (парезы, параличи, нарушения зрения и слуха).
Основные представления о БА и скрининге ксенобиотиков. Примеры скрининга.
Свойство живых систем быть реакционно способным по отношению к любому ксенобиотику приводит к тому, что все химические соединения обладают биологической активностью.
Принцип «попадание-реакция» означает, что любое проявление биологической активности ксенобиотика связано с его способностью пройти путь от внешней среды до мишени, связаться с ней и вызвать ее реакцию.
Начало этого пути – первый контакт химического соединения с биологическим объектом может быть случайным (например, через загрязнение среды) или принудительным (например, введение лекарств), после чего чужеродное соединение и биологический объект взаимодействуют по соответствующим закономерностям.
Биологической активностью ксенобиотика называют его способность изменять функциональные возможности либо компонентов организма (in vitro или in vivo), либо живого организма в целом, либо сообщества организмов.
В практику должны вводиться только те соединения, которые подверглись биологическим испытаниям и только в соответствии с результатами этих испытаний. Таким образом, биологическим испытаниям должны подвергаться все синтезируемые ксенобиотики, т. е. необходимо создать производительную систему их испытаний на разные виды биологической активности.
Проверка большого массива ксенобиотиков на один или несколько видов биологической активности получила название скрининга.
В ХХ в. тотальная проверка большого массива химических соединений или природных объектов, направленная на выявление потенциальных лекарств, получила свое развитие как один из основных методов поиска новых лекарств и вообще химических соединений с заданным типом биологической активности.
Система тестирования ксенобиотиков по видам биологической активности может включать два взаимосвязанных подхода. Первый – уровень целевого объекта испытаний (человек, животное, растение, биогеоценоз), на который должно быть направлено действие искомого ксенобиотика, исходя из целей поиска (лекарства, ветеринарное средство, гербицид и т.д.), и второй подход – совокупность тест-объектов, базирующихся на использовании более примитивной организации живой материи, чем целевой. Использование второго подхода оправдано в тех случаях, когда первый не обеспечивает достаточной производительности и т.д.
Традиционный путь поиска, например, лекарственных средств (точнее, активных субстанций будущих лекарств) в современной фармакологии в довольно схематическом виде выглядит следующим образом. На фармакологических тестах организменного уровня определяют биологическую активность ряда химических соединений, затем улучшают их свойства путем химической модификации в соответствующих рядах соединений. После этого проводят новые испытания модифицированных веществ, снова их улучшают и т.д.; это делается до тех пор, пока указанная процедура не приведет к созданию наиболее эффективного в данном ряду соединения.
Однако эти реальные подходы ограничиваются одним или несколькими видами биологической активности и сравнительно малой выборкой ксенобиотиков из массива.
Особенности биотрансформации, поступления и выведения ксенобиотиков у разных организмов.
Основные пути поступления токсических ксенобиотиков (промышленных ядов, пестицидов) в организм человека– это органы дыхания и кожа, а также пищеварительный тракт.
Проникая через биологические мембраны в сосудистое русло, ксенобиотик далее попадает в ткани к клеточным мишеням. Ряд гидрофильных ксенобиотиков выводится из организма человека в неизменном виде, но большая часть выделяется только после метаболических превращений.
Существенным фактором, влияющим на распределение ксенобиотиков и их способность к дальнейшей биотрансформации и экскреции является растворимость в липидах (коэффициент распределения).
Экскреция ксенобиотиков и их метаболитов через различные выделительные системы – заключительный этап в процессе поступления и трансформации. Экскреция осуществляется через почки, легкие, кожу, кишечник, слюнные, потовые, слезные, сальные железы, а также молочные железы при лактации.
Почечная экскреция ксенобиотиков – основной путь удаления из организма ксенобиотиков и продуктов их биотрансформации. В основе почечной экскреции лежат следующие биологические процессы: клубочковая фильтрация (вода, глюкоза, аминокислоты, белки с молекулярной массой менее 60 кД и ксенобиотики-неэлектролиты), канальцевая секреция (осуществляется с помощью ферментных систем мембранного транспорта, этим путем в мочу попадают химические вещества, являющиеся органическими кислотами или органическими основаниями), канальцевая реабсорбция (обратное всасывание метаболитов и ксенобиотиков в канальцах нефрона, кроме реабсорбции путем активного транспорта, в проксимальных и дистальных канальцах нефрона неионизированные формы веществ подвергаются реабсорбции и экскреции путем пассивной диффузии).
У растений нет специализированных путей поступления и выведения ксенобиотиков. Поступление чужеродных веществ в растения происходит главным образом через корни и листья.
Ксенобиотик проникает в ткань листа через устьица или кутикулу. Через кутикулу соединения диффундируют медленнее, чем через устьица.В последующем распределении ксенобиотиков в тканях и органах растений большую роль играют сосуды ксилемы и флоэмы. Ксенобиотики, переносимые по сосудам ксилемы (например, ряд гербицидов), поступая в корни растений, быстро создают фототоксические концентрации в наземных органах растений. В то же время очень редко отмечается аккумуляция флоэмнобильных ксенобиотиков в корнях при поступлении их через листья. Такая ситуация обусловлена главным образом экскрецией чужеродных веществ в ризосферу.Растения не имеют системы выделения, сравнимой с системой выделения животных, но их защитный механизм может включать связывание посторонних веществ некоторыми молекулами углеводов и накопление их в местах, лишенных метаболической активности (например, в вакуолях). Микроорганизмы способны разлагать многие сложные органические соединения на диоксид углерода и воду.
Различия между организмами в их реакции на действие ксенобиотиков могут быть очень существенными и обусловлены разной способностью метаболизировать эти вещества. В пределах одного вида уровень микросомной активности зависит от пола организма и стадии его развития. В разных органах – печени, кишечнике, легких и т. д. – активность также различна.
Микроорганизмыобычно содержат большое число ферментов, участвующих в процессах трансформации ксенобиотиков. Между микроорганизмами, обитающими во внешней среде и живущими внутри организма, существуют значительные различия в метаболизме ксенобиотиков. Так, многие микроорганизмы внешней среды, в отличие от кишечной микрофлоры, способны к более глубокой деградации ксенобиотиков (разрыву ароматических ядер и гетероциклических колец). Продукты расщепления служат для микроорганизмов единственным источником углерода.
В микробиологической трансформации ксенобиотиков различаются процессы метаболизма и кометаболизма. Под первым понимают превращение соединения до конечного продукта реакции, который не участвует в трансформации. Кометаболизм – это изменение структуры молекулы ксенобиотика, катализируемое ферментами микроорганизмов, которые выросли на субстратах или их метаболитах. Субстраты оказывают индуцирующее действие на такие ферменты.
Среди микроорганизмов чаще всего встречаются штаммы, осуществляющие неполную деградацию ксенобиотиков. Поэтому полное разрушение, например, пестицидов требует, как правило, совместного действия нескольких организмов и абиотических факторов.
Очень важен тот факт, что генетическая способность некоторых штаммов бактерий разрушать тот или иной ксенобиотик зависит от наличия в клетках плазмид.
В метаболизме некоторых ксенобиотиков бактериями действуют окислительные ферменты – диоксигеназы. В отличие от монооксигеназ диоксигеназы внедряют два атома кислорода в субстрат.
Растения способны к метаболическому превращению ксенобиотиков, не имеют органа или специальной ткани, ответственных за их метаболизм. Различные части растений содержат ферменты, катализирующие превращение ксенобиотиковМикросомальная система, участвующая в процессах биотрансформации, распространена в разных растительных органах и тканях: корнях, корнеплодах, корневищах, листьях и зрелых плодах. Трансформация ксенобиотиков у растений происходит, как и у животных, за счет реакций окисления, восстановления, гидролиза и последующей конъюгации. Цель у растений, как и у животных, одна – инактивировать ксенобиотик и довести его до растворимого состояния с тем, чтобы в дальнейшем либо изолировать в клеточных вакуолях, либо вывести через корневую систему и листья. Для растений характерна конъюгация с глюкозой; иногда происходит конъюгация ксенобиотика с аминокислотой или белками
3) Влияние ксенобиотиков на физико-химические свойства цитоплазмы, проницаемость биологических мембран и метаболические процессы в клетке.Цитоплазма – главное содержимое любой живой клетки – основа клеточной организации. Физико-химические изменения в цитоплазме являются ведущими в процессах жизнедеятельности клетки.
Вязкость.цитозоль, заполняющее пространство между клеточными органеллами, содержит систему микрофиламентов. Коллоидный раствор может быть золем (невязким)илигелем (вязким). Внешние слои цитоплазмы по своей конституции ближе к гелям.
Взаимодействие гидратированных ионов ксенобиотиков с заряженными белковыми молекулами цитоплазмы может вызывать переходы золь – гель и обратно. Катионы, имеющие поливалентный заряд, притягиваются сильнее к заряженной коллоидной частице по сравнению с одновалентными. Поэтому в первом случае молекула коллоидной частицы теряет часть гидратной воды, и цитоплазма превращается в вязкую гелеобразную массу. Во втором случае из-за слабого притяжения гидратные оболочки белка и иона сливаются и цитоплазма оводняется, превращается в жидкий раствор – золь.
Движение цитоплазмы. Движение цитоплазмы в животных и растительных клетках довольно распространенное явление, которое играет важную роль в осуществлении обмена и распределении веществ внутри клетки, а также характеризует уровень жизнедеятельности клетки.Скорость движения цитоплазмы (СДЦ) зависит от света, температуры, рН, ксенобиотиков.
Изоэлектрическая точка цитоплазмы. Все амфолиты способны давать двойственные ионы: положительные и отрицательные (аминокислоты с группами NH2 и СООН). Кислые группы, теряя протон, становятся отрицательно заряженными СОО- +Н+, основная группа, присоединяя протон, становится положительно заряженной NН2+Н+→NН3+.При конденсации полипептидов образуется белковая молекула, сохраняющая амфотерный характер, а также кислые и основные группы. Эти ионные группы и определяют электрические свойства белковых молекул (заряд белковой молекулы равен сумме зарядов ионных групп).
На ионизацию кислых и основных групп белка сильно влияет значение рН среды. В кислой среде аминокислоты присоединяют ион водорода (R–NН2+Н+→R–NН3+), образуя положительный заряд, в щелочной диссоциирует карбоксильная группа (СООН←→СОО- +Н+), становясь отрицательно заряженной.
Значение рН, при котором белок имеет минимальный электрический заряд, принято называть ИЭТ.В растворе с рН, равном ИЭТ, белок не движется ни к одному из полюсов, тогда как в кислой перемещается к катоду, а в щелочной – к аноду. Различные ксенобиотики, имеющие кислотные или щелочные свойства, способны сдвигать величину рН в ту или иную сторону и тем самым изменять ИЭТ цитоплазмы.Влияние ксенобиотиков на проницаемость мемб
