Общая схема процесса трансляции и характеристика его отдельных элементов.
Трансляция (от лат. translatio — перевод) -процесс синтеза белка из аминокислот на матрице информационной (матричной) РНК (иРНК, мРНК),осуществляемый рибосомой.
Механизм Общая схема трансляции.
Инициация.
1. Узнавание стартового кодона (AUG), сопровождается присоединением тРНК аминоацилированной метионином (М) и сборкой рибосомы из большой и малой субъединиц.
Элонгация.
2. Узнавание текущего кодона соответствующей ему аминоацил-тРНК (комплементарное взаимодействие кодона мРНК и антикодона тРНК увеличено).
3. Присоединение аминокислоты, принесённой тРНК, к концу растущей полипептидной цепи.
4. Продвижение рибосомы вдоль матрицы, сопровождающееся высвобождением молекулы тРНК.
5. Аминоацилирование высвободившейся молекулы тРНК соответствующей ей аминоацил-тРНК-синтетазой.
6. Присоединение следующей молекулы аминоацил-тРНК, аналогично стадии (2).
7. Движение рибосомы по молекуле мРНК до стоп-кодона (в данном случае UAG).
Терминация.
Узнавание рибосомой стоп-кодона сопровождается (8) отсоединением новосинтезированного белка и в некоторых случаях (9) диссоциацией рибосомы.
Синтез белка является основой жизнедеятельности клетки. Для осуществления этого процесса в клетках всех без исключения организмов имеются специальные органеллы — рибосомы. Рибосомы представляют собойрибонуклеопротеидные комплексы, построенные из 2 субъединиц: большой и малой. Функция рибосом заключается в узнавании трёхбуквенных (трехнуклеотидных) кодонов мРНК, сопоставлении им соответствующих антикодонов тРНК, несущих аминокислоты, и присоединении этих аминокислот к растущей белковой цепи. Двигаясь вдоль молекулы мРНК, рибосома синтезирует белок в соответствии с информацией, заложенной в молекуле мРНК.[1]
Для узнавания аминокислот в клетке имеются специальные «адаптеры», молекулы транспортной РНК (тРНК). Эти молекулы, имеющие форму клеверного листа, имеют участок (антикодон), комплементарный кодону мРНК, а также другой участок, к которому присоединяется аминокислота, соответствующая этому кодону. Присоединение аминокислот к тРНК осуществляется в энерго-зависимой реакции ферментами аминоацил-тРНК-синтетазами, а получившаяся молекула называется аминоацил-тРНК. Таким образом, специфичность трансляции определяется взаимодействием между кодоном мРНК и антикодоном тРНК, а также специфичностью аминоацил-тРНК-синтетаз, присоединяющих аминокислоты строго к соответствующим им тРНК (например, кодону GGU будет соответствовать тРНК, содержащая антикодон CCA, а к этой тРНК будет присоединяться только аминокислота глицин).
Механизмы трансляции прокариот и эукариот существенно отличаются, поэтому многие вещества, подавляющие прокариотическую трансляцию, в значительно меньшей степени действуют на трансляцию высших организмов, что позволяет использовать их в медицинской практике как антибактериальные средства безопасные для организма млекопитающих.
Процесс трансляции разделяют на
· инициацию — узнавание рибосомой стартового кодона и начало синтеза.
· элонгацию — собственно синтез белка.
· терминацию — узнавание терминирующего кодона (стоп-кодона) и отделение продукта.
Рамка считывания
Поскольку каждый кодон содержит три нуклеотида, один и тот же генетический текст можно прочитать тремя разными способами (начиная с первого, второго и третьего нуклеотидов), то есть в трех разных рамках считывания. За некоторыми интересными исключениями, значимой является информация, закодированная только в одной рамке считывания. По этой причине крайне важным для синтеза белка рибосомой является её правильное позиционирование на стартовом AUG-кодоне — инициация трансляции.
Инициация
Синтез белка в большинстве случаев начинается с AUG-кодона, кодирующего метионин. Этот кодон обычно называют стартовым или инициаторным. Инициация трансляции предусматривает узнавание рибосомой этого кодона и привлечение инициаторной аминоацил-тРНК. Для инициации трансляции необходимо также наличие определённых нуклеотидных последовательностей в районе стартового кодона (последовательность Шайна — Дальгарно у прокариот и последовательность Козак у эукариот). Немаловажная роль в защите 5'-конца мРНК принадлежит 5'-кэпу. Существование последовательности, отличающей стартовый AUG от внутренних совершенно необходимо, так как в противном случае инициация синтеза белка происходила бы хаотично на всех AUG-кодонах.
Процесс инициации обеспечивается специальными белками — факторами инициации (англ. initiation factors, IF; инициаторные факторы эукариот обозначают eIF, от англ. eukaryotes).
Механизмы инициации трансляции у про- и эукариот существенно отличаются: прокариотические рибосомы потенциально способны находить стартовый AUG и инициировать синтез на любых участках мРНК, в то время как эукариотические рибосомы обычно присоединяются к мРНК в области кэпа и сканируют её в поисках стартового кодона.
У прокариот
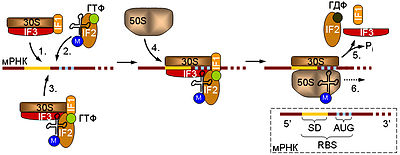
Схема инициации трансляции у прокариот.
Начальная стадия предусматривает связывание малой рибосомной субъединицы (30S) с мРНК. Это может происходить двумя способами: либо сначала к мРНК присоединяется комплекс, содержащий рибосомную субчастицу (1), а затем к нему привлекается тРНК в комплексе с IF2 и ГТФ (2), либо 30S субъединица изначально связывается с тРНК, а уже потом садится на мРНК (3). К образовавшемуся комплексу приходит большая (50S) рибосомная субъединица (4), инициаторные факторы отсоединяются от 30S субчастицы, что сопровождается гидролизом ГТФ белком IF2 (5), и собранная рибосома начинает элонгировать цепь (6). В правом нижнем углу дана схема инициаторного участка прокариотической мРНК. Отмечены 5' и 3' концы молекулы. RBS — сайт связывания рибосомы, SD — последовательность Шайна — Дальгарно, AUG — инициаторный кодон
Малая рибосомная субъединица (30S) прокариот, если она не вовлечена в данный момент в трансляцию, существует в комплексе с инициаторными факторами IF1, IF3, и, в некоторых случаях, IF2. Рассмотрим основные функции этих белков:
· IF3, связанный с 30S-субъединицей, предотвращает ассоциацию с большой (50S) субъединицей рибосомы, тем самым сохраняя её свободное состояние до связывания с матричной РНК. Этот белок также принимает участие в связывании мРНК и тРНК, а также IF2.
· IF2 взаимодействует с тРНК, а также обладает способностью расщеплять ГТФ.
· IF1 является, по-видимому, не обязательным фактором (у некоторых видов он отсутствует) повышающим сродство малой субчастицы к IF2 и IF3.
Комплекс 30S субчастицы с инициаторными факторами способен узнавать специальные последовательности мРНК, так называемые участки связывания рибосомы (англ. RBS, ribosome-binding site). Эти участки содержат, во-первых, инициаторный AUG, и, во-вторых, специальную последовательность Шайна — Дальгарно с которой комплементарносвязывается рибосомная 16S РНК. Последовательность Шайна — Дальгарно служит для того, чтобы отличать инициаторный AUG от внутренних кодонов, кодирующих метионин. После того, как 30S-субъединица связалась с мРНК к ней привлекается инициаторная аминоацил-тРНК и IF2, если они ещё не были включены в комплекс. Затем присоединяется 50S-субчастица, происходит гидролиз ГТФ и диссоциация инициаторных факторов. Собранная рибосома начинает синтезировать полипептидную цепь.
У эукариот
У эукариот существуют два основных механизма нахождения рибосомой стартового AUG: кэп-зависимый (сканирующий) и кэп-независимый (внутренняя инициация).
· При сканирующем механизме рибосома (точнее, её малая субъединица) садится на 5'-конец мРНК в области кэпа и двигается вдоль молекулы мРНК, «сканируя» один кодон за другим, пока не наткнётся на инициаторный AUG. Для привлечения рибосомы к 5'-концу мРНК требуется специальная структура, кэп — 7-метилгуанин, прикреплённый к 5'-концевому нуклеотиду мРНК.
· При механизме внутренней инициации, называемом у эукариот также IRES-зависимым механизмом, рибосома садится на внутренний участок мРНК, называемый IRES (англ. Internal Ribosomal Entry Site, участок внутренней посадки рибосомы) — участок мРНК, обладающий выраженной вторичной структурой, позволяющей ему направлять рибосомы на стартовый AUG. По IRES-зависимому механизму инициируется синтез лишь на небольшой части клеточных мРНК, а также на РНК некоторых вирусов.[2]
В дополнение к основным механизмам инициации, при наличии перед стартовым кодоном поли(А)-лидера (например, в мРНК вирусов семейства оспы) реализуется нестандартный механизм инициации. В этом случае инициаторный комплекс не содержит факторовe IF3 и eIF4F, и после сборки на 5'-нетранслируемой области осуществляет не последовательное сканирование мРНК, а т.н. АТФ-независимое "бесфазное блуждание". При этом инициация протекает значительно быстрее, чем в случае работы по классическому сканирующему механизму.[3]
Также у эукариот возможна реинициация трансляции, когда после окончания трансляции рибосома с белковыми факторами не диссоциирует от мРНК, а перескакивает с 3' на 5' конец мРНК и начинает инициацию ещё раз. Это возможно благодаря т.н. циклизации мРНК в цитоплазме, то есть физическому сближению старт- и стоп-кодонов с помощью специальных белков.
Кэп-зависимый механизм
В отличие от прокариот, инициация трансляции у которых обеспечивается лишь тремя белковыми факторами, трансляция подавляющего большинства мРНК эукариот, содержащих 5'-кэп[m7G(5')ppp(5')N] и 3' поли(А)-хвост, требует участия, по крайней мере, 13 общих эукариотических факторов инициации (eIF), представленных 31 полипептидом. Инициация трансляции включает события между диссоциацией рибосомы во время терминации в предыдущем цикле трансляции и сборкой рибосомы, готовой к элонгации, на старт-кодоне мРНК. Во время инициации аппарат трансляции решает следующие задачи:
1. диссоциация и антиассоциация рибосомных субъединиц;
2. выбор инициаторной метионил-тРНК (Met-tRNAiMet);
3. связывание 5'-кэпа, связывание поли(А), сканирование;
4. выбор правильного старт-кодона;
5. объединение рибосомных субъединиц на старт-кодоне
Диссоциация и антиассоциация субъединиц рибосом
Диссоциация рибосомных субъединиц в конце терминации — активный процесс, в котором участвуют eIF, а также факторы элонгации и терминации. Антиассоциация уже диссоциированных субъединиц обеспечивается eIF и служит для предотвращения преждевременного объединения рибосомных субъединиц.[4][5][Л 2][6] Главная роль в выполнении этой задачи принадлежит eIF3, мультисубъединичному фактору, состоящему из 13 различных субъединиц (общей молекулярной массой 800 кДа) у млекопитающих, 11 субъединиц у растений и шести субъединиц у дрожжейSaccharomyces cerevisiae.[7][8] eIF3 связывается с 40S субъединицей рибосомы (40S) посредством своей j-субъединицы, которая, в свою очередь, взаимодействует с «каркасной» (scaffolding) b-субъединицей и предотвращает ассоциацию 40S с 60S рибосомной субъединицей (60S).[9][10] Эти активности eIF3 зависят от его взаимодействия с eIF1 и тройственным комплексом eIF2/GTP/Met-tRNAiMet.[11] Связывание eIF1 с 40S является кооперативным с eIF3[12][13], так же как и связывание eIF1 с eIF1А (гомологом бактериального IF1)[14]. Таким образом, eIF1А, вероятно, также участвует в антиассоциации, по крайней мере, непрямым образом.
