Специфические и общие пути катаболизма
Углеводы, белки и жиры в организме гидролизуются, а образующиеся при этом продукты гидролиза – моносахариды, аминокислоты, жирные кислоты и глицерин подвергаются превращениям, в ходе которых часть из них окисляется до углекислого газа и воды, являющимися продуктами окисления углерода и водорода. Если бы система, в которой каждый из продуктов гидролиза биополимеров, представляющий собой субстрат для последующего окисления, имел бы свой метаболический путь, то такая система была бы очень громоздкой и ненадежной. Однако, Природа решила задачу унификации метаболических путей, организовав катаболические процессы таким образом, что на промежуточных этапах этих процессов образуется минимальное число одних и тех же метаболитов, которые получаются при окислении разных веществ. И, действительно, как видно из схемы, большинство субстратов окисления превращаются в пировиноградную кислоту – пируват (С3), а затем в ацетил-КоА (С2), причем последний может образовываться и при окислении пирувата. Ацетил-КоА полностью окисляется в цикле трикарбоновых кислот (ЦТК – он же цикл Кребса или цитратный цикл). Цикл Кребса является общим путем катаболизма для углеводов, белков и жиров. Энергия, выделяющаяся в ходе катаболических реакций, частично рассеивается виде теплоты, большая же ее часть расходуется в анаболических реакциях. Передача энергии осуществляется с помощью интермедиаторов, основной из них – АТФ. Эндергонические процессы – это синтез аденозинтрифосфата (АТФ) из аденозиндифосфата (АДФ) и неорганического фосфата, а также синтез и других веществ с макроэргическими связями. Этот процесс протекает благодаря сопряжению энергии с катаболическими реакциями. Экзергонический процесс – это гидролиз АТФ, а также других трифосфатов. Гидролиз поставляет необходимую энергию для биосинтеза.
Ниже приведена схема сопряжения анаболических и катаболических процессов:
|
 S1 окисленный субстрат, ΔG < 0
S1 окисленный субстрат, ΔG < 0  АДФ + фосфат АТФ + Н2О, ΔG < 0
АДФ + фосфат АТФ + Н2О, ΔG < 0
 сопряжение
сопряжение
|
 АТФ + Н2О → АДФ + фосфат, ΔG < 0
АТФ + Н2О → АДФ + фосфат, ΔG < 0  S2 продукт биосинтеза, ΔG > 0
S2 продукт биосинтеза, ΔG > 0
Большая часть АТФ в организме образуется в результате окислительного фосфорилирования, которое происходит в цепи передачи электронов (ЦПЭ). Основными субстратами этого процесса являются НАД*Н и ФАД*Н2, образующиеся преимущественно в ЦТК, поэтому одной из основных задач катаболизма является синтез АТФ – своеобразного аккумулятора энергии, необходимого для последующих реакций анаболизма. Большинство биосинтезов носят восстановительный характер, так как продукты биосинтеза являются менее окисленными по сравнению с исходными веществами. Роль восстановителя в таких процессах играет НАД*Н. Таким образом, ключевая роль в метаболизме принадлежит ограниченному числу соединений. Это пируват и ацетил-КоА, вещества которыми заканчиваются специфические пути катаболизма; АТФ, продукты гидролиза, к которым поступает энергия для анаболических процессов; НАД*Н и ФАД*Н2 – коферменты, при окислении которых образуется основная часть АТФ в организме.
Катаболизм углеводов
Процессы обмена углеводов у человека начинаются в ротовой полости, так как в состав слюны входит фермент амилаза, который способен расщеплять крахмал и гликоген до дисахарида – мальтозы, которая ферментом мальтазой расщепляет последнюю до глюкозы. Поступление глюкозы в клетки различных органов зависит от гормона инсулина, который регулирует скорость переноса глюкозы через мембраны клеток. переносчиками – белками.
Обмен глюкозы в клетке начинается с ее фосфорилирования:
 глюкоза + АТФ глюкозо-6-фосфат + АДФ
глюкоза + АТФ глюкозо-6-фосфат + АДФ
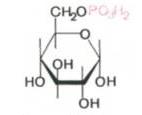
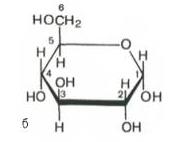
+ АТФ → + АДФ
В отличие от свободной глюкозы, глюклзо-6-фосфат не способен проходить через клеточные мембраны, поэтому фосфорилированная глюкоза как бы «запирается» в клетке, и там запасается в форме гликогена – животного крахмала, который синтезируется из молекул глюкозо-6-фосфата.
Катаболизм глюкозы в клетке может идти по трем основным направлениям, которые различаются по способу изменения углеродного скелета молекулы:
1. Дихотомический путь, при котором происходит расщепление связи С-С между третьим и четвертым атомами углерода, и из одной молекулы гексозы получаются две триозы (С6 →2С3).
2. Апотомический путь (пентозофосфатный), при котором гексоза превращается в пентозу (С6 → С5) в результате окисления и отщепления одного (первого) углеродного атома.
3.Глюкуроновый путь, когда происходит окисление и отщепление шестого углеродного атома
Главным путем распада глюкозы, ведущим к высвобождению энергии является дихотомический путь, а в этом пути, в свою очередь, окислить глюкозу и получить ее энергию можно двумя способами:
1.Независимый анаэробный распад глюкозы до молочной кислоты – гликолиз.
глюкоза →2-лактат + 134 кДж
Часть этой энергии расходуется на образование двух молекул АТФ, а остальная рассеивается в виде теплоты.
2.Аэробный (кислородзависимый) распад глюкозы до углекислого газа и воды
Это процесс обратный фотосинтезу:
С6Н12О6 + 6О2 ↔ 6СО2 + 6Н2О + 2850 кДж
60% этой энергии запасается в виде макроэргических связей АТФ, то есть в биологически доступной форме. Как видно из приведенных уравнений, аэробный путь, несомненно, более выгоден по сравнению с гликолизом, так как в нем из одинакового количества глюкозы образуется в двадцать раз больше АТФ. Аэробный распад осуществляется большинством тканей организма за исключением эритроцитов. Для злокачественных клеток основной путь получения энергии – гликолиз. Мышцы используют гликолиз в случае больших нагрузок, когда затруднен доступ кислорода и тогда в натруженных мышцах образуется молочная кислота.
Цепь реакции гликолиза глюкозы включает в себя одиннадцать реакций, из которых первые десять - общие с аэробным распадом, а одиннадцатая – это синтез молочной кислоты из пировиноградной кислоты (ПВК) с помощью НАД*Н. Рассмотрим последовательно реакции при аэробном распаде глюкозы:
1 реакция – это фосфорилирование глюкозы, ее активация.
2 реакция – это изомеризация, глюкозо-6-фосфат превращается в фруктозо-6-фосфат.
3 реакция - фруктозо-6-фосфат фосфорилируется до фруктозо-1,6-дифосфата.
Первые три реакции представляют собой так называемую подготовительную стадию, на этом этапе еще идет затрата энергии АТФ на реакции фосфорилирования:
|

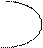
 глюкоза
глюкоза
|
 глюкозо-6-фосфат
глюкозо-6-фосфат
2- изомеризация
|
 фруктозо-6-фосфат
фруктозо-6-фосфат
|
 3
3 
 фруктозо-1,6-дифосфат
фруктозо-1,6-дифосфат
 4 4
4 4
|
|

|
 Н3РО4
Н3РО4  6
6

|
 1,3-дифосфоглицерат (ангидрид органической и фосфорной кислоты)
1,3-дифосфоглицерат (ангидрид органической и фосфорной кислоты) 

|
|

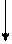 фосфоенолпируват
фосфоенолпируват
|

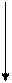 3-фосфоглицерат 10
3-фосфоглицерат 10 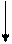 пируват
пируват
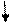
 2-фосфоглицерат общий путь
2-фосфоглицерат общий путь
 9 Н2О АТФ
9 Н2О АТФ
Следующий этап – это реакции гликолетической оксиредуктации, в которых идет распад шестиуглеродного скелета на два трехуглеродных и окисление их до пирувата.
4 реакция - фруктозо-1,6-дифосфат в своей открытой ациклической форме распадается с помощью фермента альдолазы на два трехуглеродных фрагмента: глицеральдегидфосфат и диоксиацетонфосфат.
5 реакция - изомеризация, превращение диоксиацетонфосфата в глицеральдегидфосфат.
Дальнейший катаболизм происходит только через глицеральдегидфосфат, две молекулы которого в 6-ой реакции окисляются НАД+ в 1,3-дифосфоглицерат, а выделяющаяся при этом энергия запасается в виде АТФ. В данном случае окисление альдегида приводит к ангидриду органической и фосфорной кислоты. Две молекулы 1,3-дифосфоглицерата превращаются в процессе гидролиза в 3-фосфоглицерат, а далее, в 8-ой реакции происходит перенос фосфатной группы из положения 3 в положение 2.
9 реакция- отщепление воды с получением фосфоенолпирувата, а затем происходит кето-енольное превращение, сопряженное с гидролизом, когда от диоксиацетонфосфата отщепляется одна молекула фосфорной кислоты и енольная форма превращается в кетоформу.
КАТАБОЛИЗМ ЛИПИДОВ
У высших животных и человека липиды поступают в желудок, и выходят из него почти не затронутые кислой средой. В щелочной среде тонкого кишечника липиды гидролизуются под действием липаз. Гидролизованные липиды всасываются в кровь и переносятся в различные органы для дальнейшего метаболизма.
В кровь поступают сквозь стенку кишечника глицерин, ЖК, моно- и диглицериды. В крови ЖК снова этерифицируются глицерином, который связан с белками крови и переносится в жировую ткань или печень, где откладывается. В печени идёт гидролиз с образованием ЖК, которые окисляются до СО2 и Н2О. При окислении высвобождается большое количество энергии.
Процесс окисления ЖК включает много стадий. ЖК разрушается (синтезируется) до фрагментов С-С (природные ЖК состоят из чётного числа атомов углерода). При катаболизме, ЖК сначала превращаются в тиоэфиры с коферментом А, с выделением АТФ, затем окисляются в ненасыщенные кислоты, окислителем служит ФАД.
С15Н31СООН – пальмитиновая кислота

 О HSКоА О ФАД
О HSКоА О ФАД
 СН3(СН2)12СН2СН2С
СН3(СН2)12СН2СН2С  ОН
ОН  СН3(СН2)2СН2СН2С
СН3(СН2)2СН2СН2С  SКоА
SКоА
АТФ -Н2
 О
О
 СН2(СН2)12СН=СНС
СН2(СН2)12СН=СНС  SКоА
SКоА
Затем идёт присоединение Н2О по месту двойной связи с образованием β-гидрокситиоэфира.

 О +Н2О β α О
О +Н2О β α О

 СН2(СН2)12СН=СН-С
СН2(СН2)12СН=СН-С  SКоА СН3(СН2)12СН-СН2 С SКоА
SКоА СН3(СН2)12СН-СН2 С SКоА
|
ОН
Окисление и превращение в β-кетоэфир
 О
О

 СН3(СН2)12С-СН2-С SКоА
СН3(СН2)12С-СН2-С SКоА
 Н2 ||
Н2 ||
О
Молекулы кетоэфира расщепляются с образованием двух частиц тиоэфира уксусной кислоты (ацетилКоА) и КоА тиоэфир ЖК, которые содержат на « атома углерода меньше чем в исходной кислоте (катализатор этого процесса β-кетоацилтиолаза)

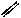 О О
О О


 СН3(СН2)12С-СН2-С SКоА + НSКоН СН3(СН2)12С SКоА +
СН3(СН2)12С-СН2-С SКоА + НSКоН СН3(СН2)12С SКоА +
||
О
 О
О
 +СН3С SКоА
+СН3С SКоА
Стадии катаболизма повторяются каждый раз, в каждом цикле отщипляется по С-С, пока вся кислота не превратится в ацетилКоА. В этой последовательности нужна одна молекула АТФ, что бы получить тиоэфир исходной ЖК.
КАТАБОЛИЗМ БЕЛКОВ
Белки подобно углеводам и липидам постоянно обмениваются, однако в отличии от углеводов и липидов белки прозапас не откладываются. Специфическим химическим элементом в составе белков является азот для которого характерен, т. н. азотистый баланс, у здорового человека поддерживается азотистое равновесие, т. к. количество азота поступившее с пищей равно количеству выделенного азота.
Начинается путь катаболизма белков с гидролиза (протеолиза) под действием ферментов протеазы и пептидазы.
Гидролиз белков начинается в желудке под действием фермента пепсина, этому способствует кислая среда желудочного сока рН=1-2 возникает благодаря выделению желудочных клеток соляной кислоты.
В тонком кишечнике при рН=7,8-8,4 , распад белков катализируется ферментами поджелудочной железы трипсином и химитрипсином.
АК – продукт гидролиза белков, поступающие из ЖКТ, являются важным фондом пополнения аминокислотного запаса клеток и тканей. Ограниченное поступление из вне даже одной из незаменимых АК вызывает резкий распад собственных белков тканей, АК используются в синтезе собственных белков, нуклеотидов, порфиринов и т. д.
В сутки взрослому человеку необходимо 100 г белка. Белки могут быть полноценными – в наличии все незаменимые АК и неполноценными – в наличии не все незаменимые АК. За сутки распадается и синтезируется 400 г белка. За 35 дней обновляются все белки.
О состоянии белкового обмена можно судить по азотистому балансу. Поскольку белки органов отличаются строгой видовой и тканевой специфичностью, живой организм обладает способностью использовать вводимый белок только в гидролизованном состоянии.
Всасывание АК через мембрану тонкого кишечника происходит под действием глутатиона. АК поступают в кровь воротной вены, затем в печень, где подвергаются ряду превращений.
Катаболизм аминокислот.
Совокупность превращений аминокислот от момента поступления в кровь до выделения из организма в виде мочевины и воды, и СО₂ называется промежуточным обменом.
Так как белки образованы большим количеством аминокислот, то не существует одной инвариантной схемы их катаболизма.
Условно промежуточный обмен делят на:
а) общие пути обмена аминокислот.
б) специфические пути превращения отдельных аминокислот.
а):
1. трансаминирование
2. дезаминирование (окислительное, гидролитическое, внутримолекулярное, восстановительное)
3. декарбоксилирование.
Самая популярная реакция в обмене аминокислот - трансаминирование.
Катализатором является трансамилазы, содержащие кофермент перидоксальфосфат.
СООН СООН СООН СООН




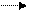 СН−NН₂ + С =О С=О + СН-NН₂
СН−NН₂ + С =О С=О + СН-NН₂





 СН₂ СН₃ СН₂ СН₃
СН₂ СН₃ СН₂ СН₃

СООН ПВК СООН аланин
аспарагиновая ЩУК
кислота
2. Дезаминирование (или окислительное дезаминирование)
Многие аминокислоты превращаются в СО₂ и Н₂О через цикл Кребса.
Для того чтобы это произошло, аминокислоты необходимо освободить от N.
Во многих случаях это достигается окислением.
СООН СООН СООН


 +НАД⁺ +H₂O
+НАД⁺ +H₂O
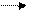
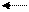
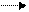
 СН−NН₂ С =NH С=О + NН₃
СН−NН₂ С =NH С=О + NН₃


 -H₂⁻
-H₂⁻
R R R
имин
Обязательный этап распада аминокислот - образование аммиака.
В некоторых случаях ( при окислительном дезаминировании глутаминовой кислоты) получается α-кетоглутаровая кислота, обращающаяся в ц. Кребса, а при окислении аланина-ПВК.
СООН СООН СООН СООН



 (О) (О)
(О) (О)

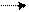
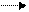 СН−NН₂ С =О СН-NН₂ С=О +NH₃
СН−NН₂ С =О СН-NН₂ С=О +NH₃



СН₂ СН₂-NН₃ СН₃ СН₃


 ПВК
ПВК
СН₂ СН₂


СООН СООН
аланин
-Гидролитическое дезанимирование.
С образованием гидроксикарбоновых кислот (аммиак уходит из кислоты)
СООН СООН



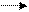 СН−NН₂ + Н₂О СН -ОH + NН₃
СН−NН₂ + Н₂О СН -ОH + NН₃

R R
-Внутримолекулярное дезаминирование приводит к образованию ненасыщенных аминокислот.
СООН СООН


 СН−NН₂ СН + NН₃
СН−NН₂ СН + NН₃
 ‖
‖
СН₂ СН


R R
-Восстановительное дезанимирование.
СООН СООН

 (Н)
(Н)
 СН−NН₂ СН₂ + NН₃
СН−NН₂ СН₂ + NН₃


R R
Образующийся при любом дезаминировании аммиак (NH₃) подлежит обезжириванию в организме, так как попадание его в кровь вызывает токсичное действие и основной путь обезвреживания: образование мочевины (карбамид).
В крови здорового человека от 2-8 ммолей мочевины. (20-25гр. выделяется в сутки)
3. Декарбоксилирование.
При декарбоксилировании аминокислоты превращаются в биологически активные амины.
Это происходит под влиянием ферментов декарбоксилазы, а коферментом служит активная форма витамина В₆
СООН NH₂


 В₆
В₆


 СН−NН₂ СН₂ + СО₂
СН−NН₂ СН₂ + СО₂
R R
При декарбоксилировании триптофана образуется триптамин, который обладает сосудисто-суживающими свойствами.
Серотонин, который образуется при декарбоксилировании 5 гидрокситриптофана.
Он активизирует выброс гормонов надпочечников.
Общий путь катаболизма.
Специфические катаболические пути углеводов, жиров, белков в дальнейшем объединяются в цикле трикарбоновых кислот.
Общим метаболитом является пировиноградная кислота, дальнейшее окисление которой приводит к выделению углекислого газа и воды. Если бы пировиноградная кислота сгорала в колориметрической бомбе, то
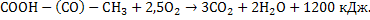
В живой клетке эта энергия извлекается в результате окисления путем дегидрирования и первая стадия на общем пути катаболизма является окислительное декарбоксилирование пирувата. В результате этого процесса пировиноградная кислота превращается в ацетил КоА. В этом сложном превращении участвуют НАД+ и кофермент А:
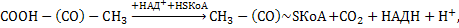
Цикл Кребса (цикл трикарбоновых кислот).
Цикл Кребса представляет собой систему из замкнутых реакций, в результате которых образуются углекислый газ и вода, запасается небольшое количество энергии и образуется большое количество восстановленных коферментов, которые затем, с помощью переносчиков, попадают в дыхательную цепь и обуславливают там синтез АТФ в процессе окислительного фосфорилирования.
Таким образом, основной задачей цикла трикарбоновых кислот является окончательное окисление органических веществ и регенерация восстановленных коферментов. Кроме того, в цикле Кребса образуется ряд промежуточных продуктов, которые используются в качестве субстратов для биосинтеза важных соединений: аминокислот, парфиринов, глюкозы. Поэтому цикл трикарбоновых кислот является центральным типом метаболизма.
Цикл включает в себя девять реакций, в результате каждого цикла образуется две молекулы углекислого газа. Цикл действует в аэробных условиях.

ЦПЭ. Тканевое дыхание.
