Окислительное фосфорилирование АДФ. Механизм. Сопряжение и разобщение окисления и фосфорилирования в дыхательной цепи. Коэффициент Р/0. Регуляция дыхательной цепи
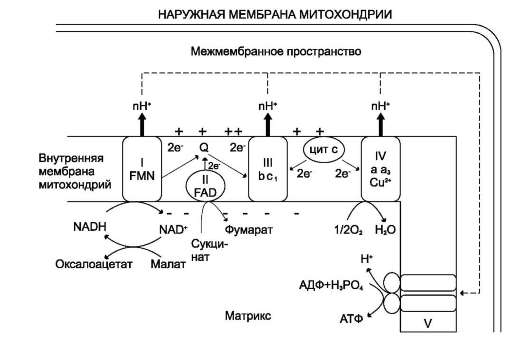
Характеристика компонентов дыхательной цепи (ферментативных комплексов):
1)НАДН-дегидрогеназа(НАДН-КоQ-оксидоредуктаза) – встроена во внутреннюю мембрану митохондрий. Это флавин-зависимый фермент, в состав которого входит витамин В2. , имеет 2 простетические группы: ФМН и Железосерные белки. Функция: а)Принимает электроны от НАДН и передает их на коэнзим Q (убихинон).
б) Переносит 4 иона Н+на наружную поверхность внутренней митохондриальной мембраны.
2) КоQ (убихинон) – небелковый переносчик, является жирорастворимым не заряжен. Поэтому он принимает электроны и протоны с ФАДН2, т.е. ч/з 2й вход в дыхательную цепь.
3) Цитохромы (b, c1, c, а, а3)– сложные белки (гемпротеины), небелковой частью которых является гем, содержащийFе3+(окисленная форма). Fе гема может обратимо принимать и отдавать электроны.
4) УбихинолДГ (КоQ-цитохром с-оксидоредуктаза)– это ферментный комплекс, состоящий из цитохромов b и с1, включающий также FеS-центры. Функция:
а) Принимает электроны от ко-Q и передает их на цитохром; б)Переносит 2 иона Н+ на наружну
5) Цитохром с-кислород-оксидоредуктаза- В этом комплексе находятся цитохромы а и а3, В комплексе также имеется 2 иона меди. Функция: а) Принимает электроны от цитохрома с и передает их на кислород с образованием воды. б)Переносит 4 иона Н+ на наружну
6) АТФ-синтаза– комплекс, две большие группы: одна группа формирует субъединицу Fо –по ней выкачанные наружу протоны водорода устремляются в матрикс. Другая группа образует субъединицу F1 –используя энергию протонов, синтезирует АТФ.
Сопряжение в дыхательной цепи— это такое состояние, когда окисление (перенос электронов) сопровождается фосфорилированием, то есть синтезом АТФ.
Разобщение— это состояние дыхательной цепи, когда окисление идет, а фосфорилирование не происходит, то есть пункты фосфорилирования выключены.Е в виде тепла. Разобщение вызывают липофиль-ные вещества, которые способны переносить протоны водорода с внешней стороны внутренней мембраны митохондрий на внутреннюю, минуя АТФ-синтетазу. 2,4-ДНФ (динитрофенол), яды промышленных производств, бактериальные токсины, набухание митохондрий, жирные кислоты, ионофоры (вещества, переносящие ионы через мембрану). Разобщители повышают скорость переноса электронов по дыхательной цепи и выводят ее из под контроля АТФ.
Выделяют три основных группы ингибиторов:
1. действующие на I комплекс, например, амитал (производное барбитуровой кислоты), ротенон, прогестерон,
2. действующие на III комплекс, например, экспериментальный антибиотик антимицин А,
3. действующие на IV комплекс, например, сероводород (H2S), угарный газ (СО), цианиды (-CN).
Окисление молекулы NADH в ЦПЭ сопровождается образованием 3 молекул АТФ; электроны от FAD-зависимых дегидрогеназ поступают в ЦПЭ на KoQ, минуя первый пункт сопряжения. Поэтому образуются только 2 молекулы АТФ.
Отношение количества фосфорной кислоты (Р), использованной на фосфорилирование AДФ, к атому кислорода (О), поглощённого в процессе дыхания, называют коэффициентом окислительного фосфорилирования и обозначают Р/О. Следовательно, для NADH Р/О = 3, для сукцината Р/О = 2.
Дыхательный контроль–Если АТФ не используется и его концентрация в клетках возрастает, то прекращается и поток электронов к кислороду.
| 13. | Субстратное фосфорилирование АДФ. Отличия от окислительного фосфорилирования. Основные пути использования АТФ. Цикл АДФ-АТФ. Понятие о свободном окислении и его значение. Тканевые особенности окислительно-восстановительных процессов. |
субстратное фосфорилирование — процесс образования АТФ, не связанный с мембранами. В этом случае АТФ образуется За счет того, что фосфатная группа перемещается от (субстрата) к АДФ (например, образование АТФ при гликолизе).
Этот способ связан с передачей макроэргического фосфата субстрата на АДФ. К таким веществам относятся метаболиты гликолиза (1,3-дифосфоглицериновая кислота, фосфоенолпируват), цикла трикарбоновых кислот (сукцинил-SКоА) и креатинфосфат. Энергия гидролиза их макроэргической связи выше, чем 7,3 ккал/моль в АТФ, и роль указанных веществ сводится к использованию этой энергии для фосфорилирования молекулы АДФ до АТФ.
Отличия: разные источники энергии, для окислительного необходимы движение электронов в дых цепи, для субстратного необ-ма энергия макроэргической связи.оксилительное на мембране митохондрий, субстратное в цитозоле,
Существует три основных способа использованияАТФ: 1. биосинтез веществ, 2. транспорт веществ через мембраны,
3. изменение формы клетки и ее движение. Эти процессы вкупе с процессом образования АТФ получили название АТФ-цикл:
Использование АТФ как источника Е возможно только при условии непрерывного синтеза АТФ из АДФ за счёт Е окисления орг-их соединений. Цикл АТФ-АДФ - основной механизм обмена энергии в биологических системах. 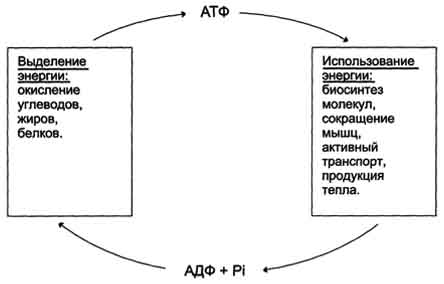
свободное окисление, не сопряженное с синтезом АТФ: микросомальное (в гладком эндоплазматическом ретикулуме) и пероксисомалъное. Основная роль свободного окисления - пластическая и антитоксическая: гидроксилирование углеводородных компонентов, в том числе ароматических; синтез стероидных гормонов и желчных кислот; обезвреживание токсинов и т.д. В свободном окислении участвуют особые флавиновые ферменты и цитохромы Ь; и Р450. Процессы свободного окисления сосредоточены в цитозоле, в мембране эндоплазматической сети клетки, в мембранах лизосом, пероксисом и аппарата Гольджи, на внешних мембранах митохондрий и хлоропластов. Они идут также в ядерном аппарате клетки.
Тканевые и возрастные особенности окислительных процессов.Анаэробные ткани могут получать энергию без кислорода. Такими тканями являются: скелетные мышцы, эритроциты, периферические нервы, мозговое вещество почек, кость, хрящ, соединительная ткань. Аэробные ткани получают энергию с использованием кислорода и полностью зависят от кровотока. К таким тканям относятся: головной мозг, сетчатка глаза, сердце, кора почек, печень, слизистая тонкого кишечника. Потребление кислорода, а значит, и интенсивность окислительных процессов с возрастом падают.
| 14. | Функции углеводов. Потребность организма в углеводах. Переваривание углеводов. Нарушения переваривания и всасывания углеводов.. Роль печени в обмене углеводов. |
Углеводы - это оксопроизводные многоатомных спиртов и продукты их конденсации.
Функции углеводов:
1. Углеводы служат источником энергии 17,18 кДж).
2. Углеводы входят в состав структурно функциональных компонентов клеток. К ним относятся пентозы нуклеотидов и нуклеиновых кислот, углеводы гликолипидов и гликопротеинов
3. Из углеводов могут синтезироваться соединения других классов (липиды и аминокислоты).
4. Выполняют структурообразовательную функцию, то есть входят в состав клеточных и межклеточных структур
5 специфическиеф функции (как оплодотворение, узнавание клеток при тканевой дифференциации, отторжение чужеродных тканей и т. д. ).
Потребностьв углеводах взрослого организма составляет 350-400 г в сутки, при этом целлюлозы и других пищевых волокон должно быть не менее 30-40 г.
Ферменты участвующие в переваривании углеводов:
-А-амилаза слюны и А-амилаза поджелудочной железы. Эти ферменты расщепляют А-1-4-гликозидные связи в крахмале и гликогене, действуют в слабощелочной среде,активируются ионами хлора
-амило-1,6-гликозидаза вырабатывается в кишечнике и расщепляет 1,6 гликоидные связи в крахмале и глиикогене
-сахараза образуется в кишечнике и расщепляет сахарозу с образованием глюкозы и фруктозы
-мальтаза образуется в кишечнике и расщепляет мальтозу на 2 молекулы глюкозы
-лактаза образуется там же, расщепляет лактозу с образованием галактозы и глюкозы.
углеводы в жкт расщепляются до моносахаридов- глюкозы.фруктозы и галактозы , которые всасываются путем активного транспорта или диффузно и попадают в кровь, а затем в печень 1.фруктоза через спец. белки переносчики фруктозы 2.глюкоза лиюо через переносчики глюкозы, либо чеое натрий-зависимые белок-переносчики,3.галактоза через натриевые переносчики 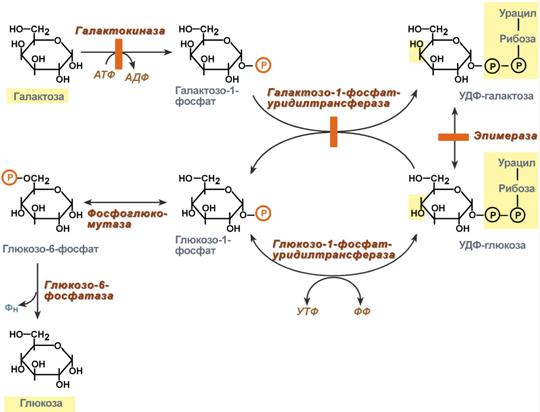
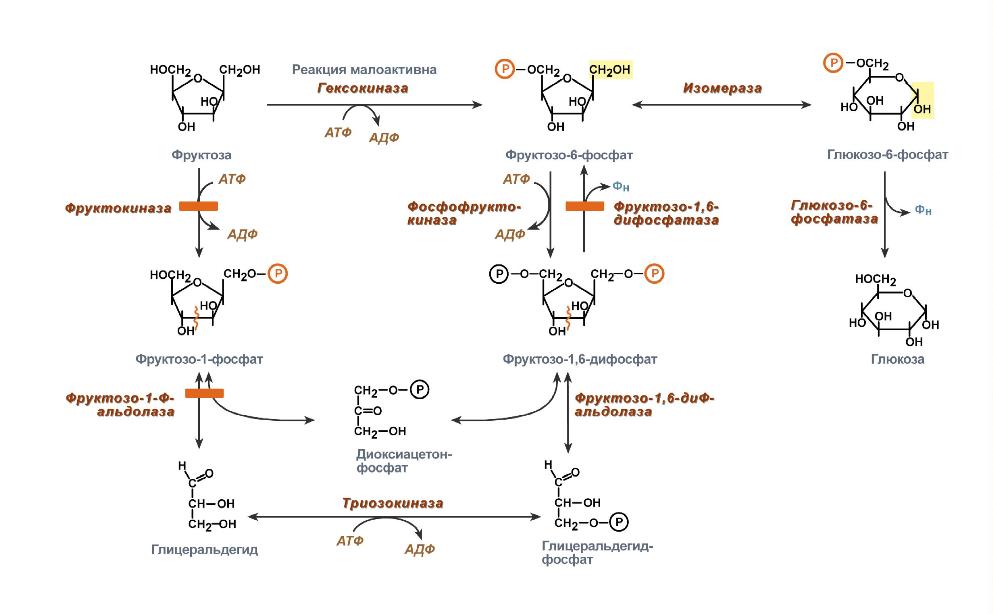
Нарушение этого процесса может возникать:
1) при поражении поджелудочной железы и слизистой кишечника;
3) отравлениях ферментными ядами
4) Недостаточной выработке дисахаридаз кишечника: лактазы, сахаразы, мальтазы и изомальтазы
.Приобретенная недостаточность. заболевания стенок ЖКТ: энтериты, колиты, когда нарушается образование ферментов. ухудшается всасывание моносахаров. Наследственная недостаточность. При наследственной (первичной) патологии лактазы симптомы проявляются после первых кормлений. Патология сахаразы обнаруживается при введении в рацион сладкого.Недостаточность лактазы может проявляться не только у младенцев, но и в подростковом и взрослом возрасте, что является физиологическим возрастным изменением.
Роль печени в обмене углеводов
1 унификация моносахаридов
2 гликогенная функция при избытке глюкозы в крови, в печенипроисходит синтез гликогена
3 синтез углеводов из метаболитов неуглеводного характера(глюконеогенез0
4 синтез гликопротеинов крови
5 образование глюкуроновой кислоты которая участвует в обезвреживании токсинов(билирубина)
| 15. | Биосинтез и мобилизация гликогена: последовательность реакций, физио- логическозначение. Регуляция обмена гликогена. Гликогенозы и агликогенозы. |
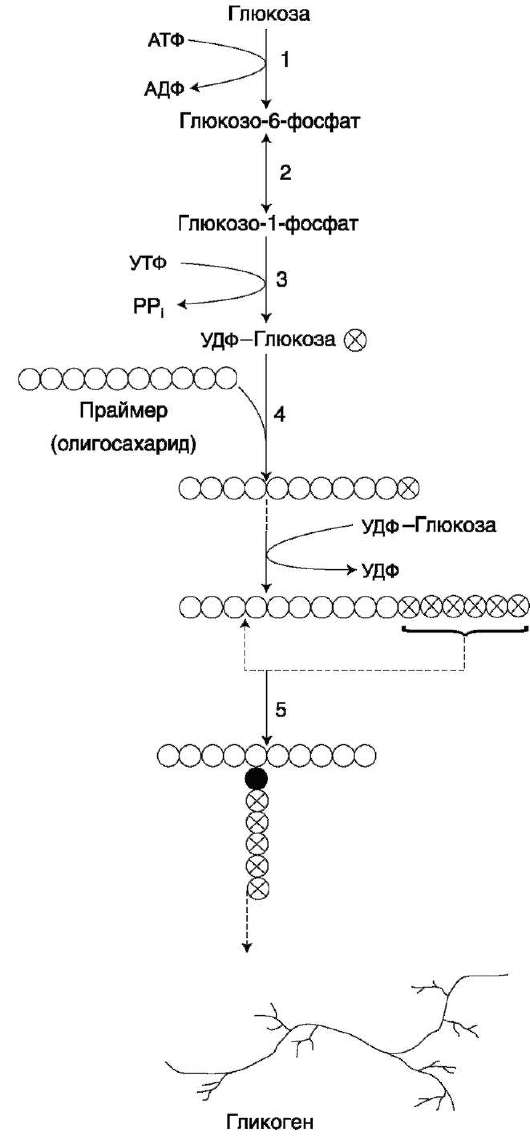 синтез 1 - глюкокиназа или гексокиназа; 2 - фосфоглюкомутаза; 3 - УДФ-глюкопирофосфорилаза; 4 - гликогенсинтаза 5 - фермент «ветвления» (амило-1,4→ 1,6-глюкозилтрансфераза), светлые и заштрихованные кружки - глюкозные остатки, закрашенные кружки - глюкозные остатки в точке ветвления.
синтез 1 - глюкокиназа или гексокиназа; 2 - фосфоглюкомутаза; 3 - УДФ-глюкопирофосфорилаза; 4 - гликогенсинтаза 5 - фермент «ветвления» (амило-1,4→ 1,6-глюкозилтрансфераза), светлые и заштрихованные кружки - глюкозные остатки, закрашенные кружки - глюкозные остатки в точке ветвления.
распад гликогена гликогенолиз двумя путями:гидролитический путь в лизосомах поддействием гамма амилазы при участии воды без образования промежуточных метаболитов и фосфоролитический путь(фосфоролиз):
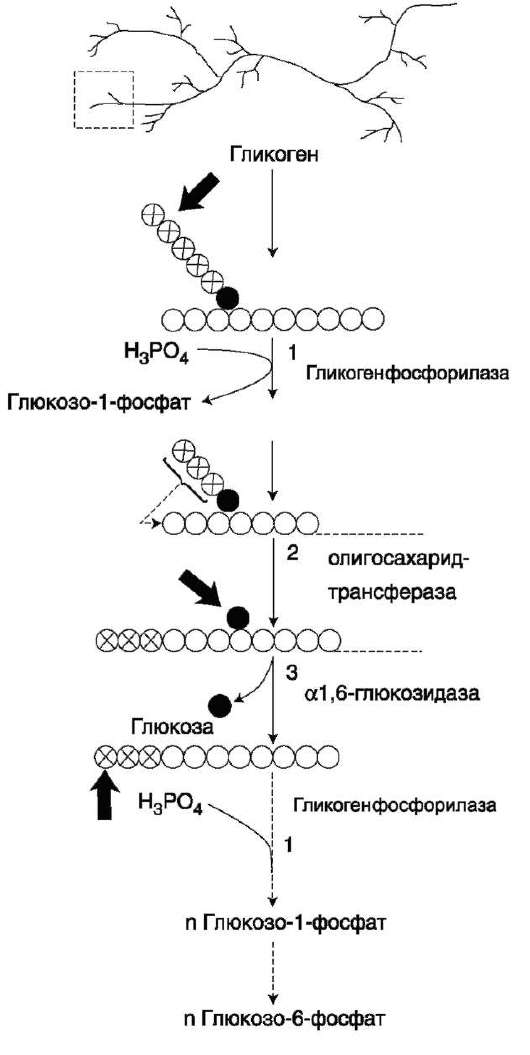
Закрашенный кружок - глюкозный остаток, связанный α-1,6-гликозидной связью; светлые и заштрихованные кружки - глю-козные остатки в линейных участках и боковых ветвях, связанные а-1,4-гликозидной связью. 1 - гликоген-фосфорилаза; 2 - олигосахаридтрансфераза; 3 - α-1,6-глюкозидаза.
-печень запасает глюкозу в виде гликогена для поддержания постоянной концентрации глюкозы в крови, и, следовательно, обеспечивает поступление глюкозы в другие ткани
функция мышечного гликогена заключается в освобождении глюкозо-6-фосфата, потребляемого в самой мышце для окисления и использования энергии;
*синтез гликогена - процесс эндергонический. Так на включение одного остатка глюкозы в полисахаридную цепь используется 1 моль АТФ и 1 моль УТФ;
синтез усиливается инсулином а распад катехоламинами глюкагоном глюкокортикостероидами цАМФ и Са.
Гликогенозы. нарушен распад гликогена. Гликоген накапливается в клетках в больших количествах, что может привести к их разрушению. симптомы: увеличение размеров печени, мышечная слабость, гипогликемия натощак. Известно несколько типов гликогенозов. Они могут быть вызваны недостаточностью глюкозо-6-фосфатазы, фосфорилазы или g-ами-лазы.
Агликогенозы вызываются недостаточностью ферментов, участвующих в синтезе гликогена. В результате нарушается синтез гликогена и снижается его содержание в клетках. Симптомы: резкая гипогликемия натощак, особенно после ночного перерыва в кормлении. Гипогликемия приводит к отставанию в умственном развитии. Больные погибают в детском возрасте.
| 16. | Анаэробный распад глюкозы: последовательность реакций, физиологическое значение. Роль анаэробного распада глюкозы в мышцах. Дальнейшая судьба молочной кислоты. |
Гликолиз - это расщепление глюкозы до молочной кислоты в анаэробных условиях.
Гликолиз состоит из двух стадий: подготовительной и главной.
В подготовительной стадии глюкоза расщепляется с образованием диоксиацентонфосфата (ДОАФ) и 3-фосфоглицеринового альдегида, при этом рас-ходуются 2 молекулы АТФ;
В главной стадии фосфотриозы превращаются в лактат (молочную кислоту), при этом образуются 4 молекулы АТФ. Синтез АТФ в гликолизе происходит путем субстратного фосфорилирования.
Таким образом, анаэробное окисление глюкозы приводит к образованию 2 молекул лактата и 2 молекул АТФ.
Ключевыми ферментами гликолиза являются: гексокиназа (начальный фермент), фосфофруктокиназа (лимитирующий фермент), пируваткиназа. АТФ и цитрат ингибируют фосфофруктокиназу, АДФ - активирует.
Преимущества гликолиза:
- быстрый процесс;
- анаэробный.
Недостатки гликолиза:
- малоэффективный процесс;
- продуктом гликолиза является лактат, накопление которого в клетках и в крови вызывает метаболический ацидоз
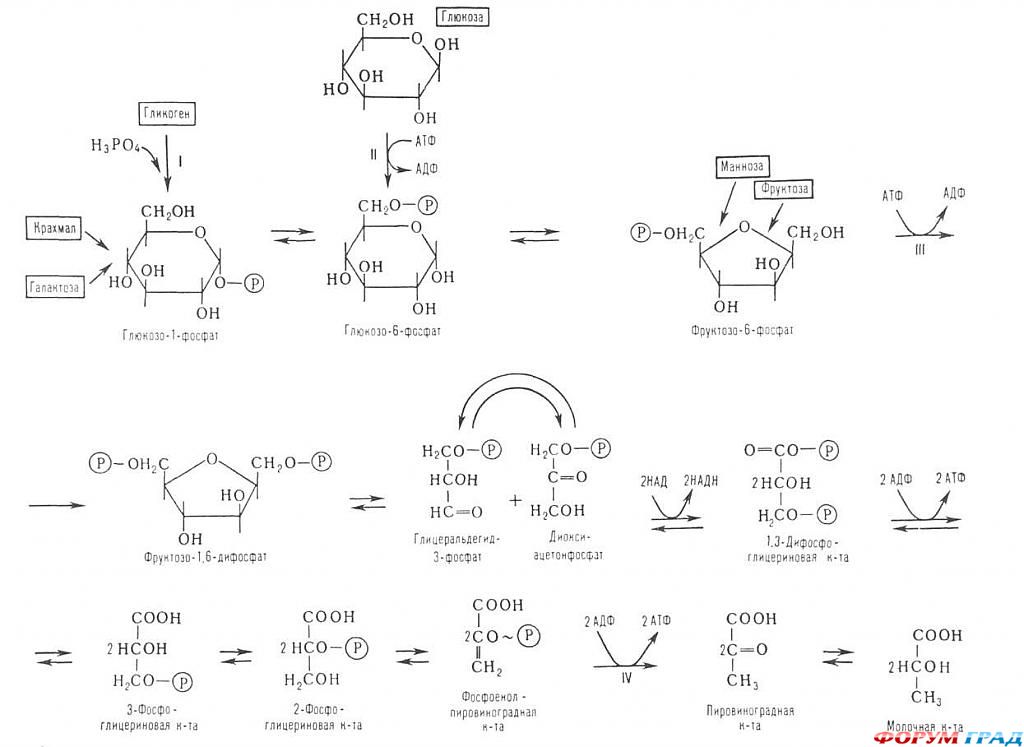
С6Н1206 + 2 Н3РО4 + 2 АДФ = 2 С3Н6О3 + 2 АТФ + 2 Н2О.
значение:
Анаэробный гликолиз, несмотря на небольшой энергетический эффект, является основным источником энергии для скелетных мышц в начальном периоде в условиях, когда снабжение кислородом ограничено. Кроме того, зрелые эритроциты извлекают энергию за счет анаэробного окисления глюкозы, потому что не имеют митохондрий
Под действием лактатдегидрогеназы молочная кислота окисляется снова, образуя пируват, который и участвует в дальнейших превращениях. . Это вещество выводится в кровь и утилизируется, превращаясь в печени в глюкозу, или при доступности кислорода превращается в пируват, который вступает в общий путь катаболизма, окисляясь до СО2 и Н2О
