| № п/п | Вопросы |
| Модуль 1. Химические основы биологического взаимодействия органических соединений |
| Реакции электрофильного присоединения и замещения в органической химии |
| 1. | Реакции электрофильного замещения характерны для 1) бензола 2) бутана 3) циклобутана 4) бутена |
| 2. | Реакции присоединения характерны для 1) метана 2) бутана 3) циклогексана 4) циклопропана |
| 3. | При взаимодействии 2-метилбутадиена-1,3 с 1 молем хлороводорода преимущественно образуется 1) 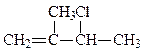 2) 2) 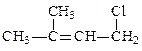 3) 3) 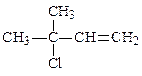 4) 4) 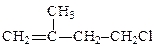 |
| 4. | При гетеролитическом разрыве ковалентной связи 1) у каждого из ранее связанных атомов остается по одному электрону 2) разрыв старых и образование новых связей происходит одновременно 3) электронную пару, связывающую атомы, забирает один из партнеров связи 4) гетеролитический разрыв ковалентной связи невозможен |
| 5. | Продукт гидратации пентина-1 в присутствии солей ртути (ii) и серной кислоты 1) СН3СН2СН2СН=СН2ОН 2) СН3-С(ОН)2-СН2СН2СН3 3) СН3-СО-СН2СН2СН3 4) СН3СН2СН2СН2СН=О |
| 6. | Продукт хлорирования бензойной кислоты 1) орто-хлорбензойная кислота 2) мета-хлорбензойная кислота 3) пара-хлорбензойная кислота 4) 2,4,6-трихлорбензойная кислота |
| 7. | Электроноакцепторные заместители 1) увеличивают скорость реакций SE в бензольном ядре 2) понижают скорость реакций SE в бензольном ядре 3) увеличивают скорость реакций SR в бензольном ядре 4) понижают скорость реакций SR в бензольном ядре |
| 8. | Реакции радикального замещения характерны для 1) бутана 2) бутена 3) бутина 4) бутадиена-1,3 |
| 9. | Электронодонорные заместители 1) увеличивают скорость реакций SE в бензольном ядре 2) понижают скорость реакций SE в бензольном ядре 3) увеличивают скорость реакций SR в бензольном ядре 4) понижают скорость реакций SR в бензольном ядре |
| 10. | Бромирование пропена - реакция 1) присоединения 2) замещения 3) гидрирования 4) изомеризации |
| 11. | Галогенирование пропана - реакция 1) присоединения 2) замещения 3) гидрирования 4) изомеризации |
| 12. | При нитровании фенола преимущественно образуется 1) орто-нитрофенол 2) мета-нитрофенол 3) пара-нитрофенол 4) 2,4,6-тринитрофенол |
| 13. | 2 моль брома присоединяет 1 моль 1) бутина-2 2) бутена-2 3) бутана 4) циклобутана |
| 14. | Реакция 1,4 –присоединения характерна для 1) бутадиена-1,3 2) бутена-2 3) бутена-1 4) бутина-1 |
| 15. | Толуол из бензола получают в результате реакции 1) ацилирования 2) алкилирования 3) галогенирования 4) сульфирования |
| 16. | Продукт гидратации пропина 1) альдегид 2) спирт 3) карбоновая кислота 4) кетон |
| 17. | Продукт гидратации ацетилена 1) альдегид 2) спирт 3) карбоновая кислота 4) кетон |
| 18. | Структура радикала изопропила 1. 1) СН3-СН2- 2. 2) СН3-СН2- СН2- 3. 3) СН3-СН(СН3) - СН2- 4) СН2 = СН- |
| 19. | Схема реакции электрофильного замещения 1) С6Н6 + Br2 → C6H5Br + HBr 2) H2C = CH2 + Br2 → CH2Br – CH2Br 3) H3C – CH3 + Br2 → H3C – CH2Br + HBr 4) ∆ + Br2 → CH2Br – CH2 – CH2Br |
| 20. | Алкилирование бензола – это реакция 1) SR 2) SE 3) AN 4) AE |
| 21. | Галогенирование пропана – это реакция 1) SR 2) SE 3) AN 4) AE |
| 22. | Гидрогалогенирование циклопропана - это реакция 1) SR 2) SE 3) AN 4) AE |
| 23. | Галогенирование циклопропана – это реакция 1) SR 2) SE 3) AN 4) AE |
| 24. | Галогенирование циклогексана – это реакция 1) SR 2) SE 3) AN 4) AE |
| 25. | Продукт гидратации этилена 1) этанол 2) этин 3) этаналь 4) этановая кислота |
| 26. | Продукт гидратации пропена 1) пропаналь 2) пропанол-1 3) пропанол-2 4) пропановая кислота |
| 27. | FeCl3 С6Н6 + Сl2 → C6H5Cl + HCl – это реакция 1) SR 2) SE 3) AN 4) AE |
| 28. | Электронодонорный заместитель 1) – СН=СН2 2) – СООН 3) – NO2 4) – NH2 |
| 29. | Электроноакцепторный заместитель 1) – СН3 2) – ОН 3) – NН2 4) – SO3H |
| 30. | Схема реакции радикального замещения 1) С6Н6 + Br2 → C6H5Br + HBr 2) H2C = CH2 + Br2 → CH2Br – CH2Br 3) H3C – CH3 + Br2 → H3C – CH2Br + HBr 4) ∆ + Br2 → CH2Br – CH2 – CH2Br |
| 31. | hν СН3 – СH2 – CH3 + Cl2 → CH3 – CH(Cl)-CH3 + HCl - это реакция 1) SR 2) SE 3) AN 4) AE |
| 32. | СН2 = СH – CH3 + Cl2 → CH2(Cl) – CH(Cl)-CH3 - это реакция 1) SR 2) SE 3) AN 4) AE |
| 33. | Наличием в алкенах л-связи обусловлены реакции 1) замещения 2) обмена 3) присоединения |
| 34. | в реакции пропена с HBr по правилу Марковникова образуется 1) 1-бромпропан 2) 2-бромпропан 3) 1,2 -дибромпропан 4) 1,3-дибромпропан |
| 35. | СН2 = СН2 + [О] + Н2O → СН2(ОН) - СН2(ОН) – это реакция 1) Вюрца 2) Вагнера 3) Зинина 4) Кучерова |
| Кислотно-основные свойства органических соединений |
| 36. | Наиболее сильными кислотными свойствами обладает 1) СН3СООН 2) ClCH2COOH 3) BrCH2COOH 4) FCH2COOH |
| 37. | Наиболее сильными основными свойствами обладает 1) 4-аминобензойная кислота 2) 4-аминонитробензол 3) анилин (аминобензол) 4) 4-аминохлорбензол |
| 38. | Самая сильная кислота Бренстеда 1) СН3СН2СН2ОН 2) СН3СН2СН2SН 3) СН3СН = СН2 4) СН3СН2СН2NН2 |
| 39. | Самая сильная сн-кислота Бренстеда 1) НС ≡ СН 2) Н2С = СН2 3) Н3С – СН3 |
| 40. | Самое сильное основание Бренстеда 1) С6Н5NH2 2) CH3NH2 3) (СН3)2NH 4) (CH3)3N |
| 41. | Самое слабое основание Бренстеда 1) С6Н5NH2 2) CH3NH2 3) (СН3)2NH 4) (CH3)3N |
| 42. | Самая сильная кислота Бренстеда 1) анилин 2) фенол 3) пара-нитроанилин 4) пара-нитрофенол |
| 43. | Самое сильное основание Бренстеда 1) анилин 2) фенол 3) пара-нитроанилин 4) пара-нитрофенол |
| 44. | Кислота Бренстеда - это 1) донор протона 2) акцептор протона 3) донор электронной пары 4) акцептор электронной пары |
| 45. | С раствором HCl взаимодействует 1) С6H5OH 2) (C3H7)2NH 3) CH3СООН |
| 46. | Основание Бренстеда - это 1) донор протона 2) акцептор протона 3) донор электронной пары 4) акцептор электронной пары |
| 47. | Самая сильная SН-кислота Бренстеда 1) СН3СН2СН2SН 2) СН3SН 3) СН3СН2SН |
| 48. | Кислота Льюиса – это 1) донор протона 2) акцептор протона 3) донор электронной пары 4) акцептор электронной пары |
| 49. | Основание Льюиса - это 1) донор протона 2) акцептор протона 3) донор электронной пары 4) акцептор электронной пары |
| 50. | Кислота Бренстеда 1) предоставляет протон 2) присоединяет протон 3) предоставляет электронную пару 4) присоединяет электронную пару |
| 51. | NH- кислота Бренстеда 1) С2H5NO2 2) C2H5NH2 3) C2H5CN 4) NH4Cl |
| 52. | Основность уменьшается в ряду 1) метанол, этанол, пропанол 2) этиламин, этантиол, этанол 3) этиламин, этанол, этантиол 4) пропанол, этанол, метанол |
| 53. | Кислотность увеличивается в ряду 1) метанол, этанол, пропанол 2) этиламин, этантиол, этанол 3) этиламин, этанол, этантиол 4) пропанол, метанол, этанол |
| 54. | ОН-кислотой Бренстеда является 1) фенол 2) этантиол 3) этиламин 4) этан |
| 55. | Ацетилен - это кислота Бренстеда 1) СН- 2) ОН- 3) NH- 4) SH- |
| 56. | Основность усиливается в ряду 1) анилин, аммиак, метиламин 2) метиламин, аммиак, анилин 3) метиламин, анилин, аммиак 4) анилин, метиламин, аммиак |
| 57. | Основность ослабевает в ряду 1) анилин, аммиак, метиламин 2) метиламин, аммиак, анилин 3) метиламин, анилин, аммиак 4) анилин, метиламин, аммиак |
| 58. | Кислотность фенола понижает заместитель 1) – СООН 2) - COH 3) – NH2 4) – NO2 |
| 59. | Кислотность фенола увеличивает заместитель 1) – NH2 2) -Cl 3) -CH3 4) – NO2 |
| 60. | Основность анилина понижает заместитель 1) – СООН 2) - Cl 3) – NH2 4) – CH3 |
| 61. | Самая сильная ОН-кислота в водном растворе 1) СН3ОН 2) СН3СН2ОН 3) (СН3)2СНОН 4) (СН3)3СОН |
| 62. | Наиболее сильная кислота 1) СН3СООН 2) ClCH2COOH 3) Cl3CCOOH 4) Cl2CHCOOH |
| 63. | Наиболее слабая кислота 1) СН3СООН 2) ClCH2COOH 3) Cl3CCOOH 4) Cl2CHCOOH |
| 64. | Наиболее сильная кислота 1) α -хлормасляная 2) масляная 3) γ-хлормасляная 4) β –хлормасляная |
| 65. | Наиболее слабая кислота 1) α -хлормасляная 2) масляная 3) γ-хлормасляная 4) β –хлормасляная |
| 66. | Самая слабая КИСЛОТА Бренстеда 1) СН3СН2СН2ОН 2) СН3СН2СН2SН 3) СН3СН = СН2 4) СН3СН2СН2NН2 |
| 67. | Самое сильное основание Бренстеда 1) СН3СН2СН2ОН 2) СН3СН2СН2SН 3) СН3СН = СН2 4) СН3СН2СН2NН2 |
| 68. | Самое слабое основание Бренстеда 1) СН3СН2СН2ОН 2) СН3СН2СН2SН 3) СН3СН = СН2 4) СН3СН2СН2NН2 |
| 69. | С NaOH взаимодействует 1) С2H5SH 2) C2H5OH 3) C2H5OC2H5 4) H2C=CH2 |
| 70. | Самая сильная кислота Бренстеда 1) СН- 2) NH- 3) OH- |
| Реакционная способность спиртов, эфиров, фенолов и их тиоаналогов |
| 71. | Внутрикомплексный хелат образуется при взаимодействии гидроксида меди (II) c 1) СН2ОН-СН2-СН2ОН 2) СН3СН2СН2ОН 3) СН2ОН-СНОН-СН2ОН 4) С6Н5ОН |
| 72. | Продукт внутримолекулярной дегидратации 2-метилпентанола-2 1) СН3СН2СН=С(СН3)2 2) СН3СН2СН2С(СН3)=СН2 3) СН3СН=СН2 4) СН3СН2СН2СН=С(СН3)2 |
| 73. | Продукт межмолекулярной дегидратации этанола 1) этаналь 2) этилен 3) диэтиловый эфир 4) этан |
| 74. | При бромировании фенола преимущественно образуется 1) 2-бромфенол 2) 4-бромфенол 3) 2,6-дибромфенол 4) 2,4,6-трибромфенол |
| 75. | Продукт РЕАКЦИИ СН3СН2-О-СН2-СН3 + Н2SO4 → 1) диэтилоксонийгидросульфат 2) этанол 3) этантиол 4) этансульфоновая кислота |
| 76. | Кофермент а - представитель 1) спиртов 2) простых эфиров 3) фенолов 4) тиолов |
| 77. | Функциональная группа фенолов 1) –ОН 1. 2) –СООН 3) –СНО 4) – NH2 |
| 78. | Функциональная группа спиртов 1) -NO2 2. 2) –ОН 3. 3) –СООН 4. 4) –СНО |
| 79. | СН3 – СН (CH3) – ОН 1) 1 -метилэтанол-1 2) 2-метилэтанол-2 3) пропанол-1 4) пропанол-2 |
| 80. | Пропанол-1 - продукт восстановления 1) пропана 2) пропаналя 3) пропилена 4) пропановой кислоты |
| 81. | вещество СН2 - СН – СН2 относится к классу | | | ОН ОН ОН 1) фенолов 2) альдегидов 3) простых эфиров 4) многоатомных спиртов |
| 82. | Этилат натрия C2H5ONA - продукт взаимодействия этанола с 1) гидроксидом натрия 2) натрием металлическим 3) гидрокарбонатом натрия 4) гидридом натрия |
| 83. | Спирт + карбоновая кислота ↔ сложный эфир + вода 1) реакция нейтрализации 2) реакция этерификации 3) реакция гидратации 4) реакция гидролиза |
| 84. | Нитроглицерин относится к классу 1) солей 2) сложных эфиров 3) простых эфиров 4) нитроалканов |
| 85. | Качественной на мнгоатомные спирты является реакция 1) с Сu(ОН)2 2) с СuО 3) с КМnO4 4) с Сu(ОН)2 при нагревании |
| 86. | Формула фенола 1) СН3СООН 2) С2Н5ОН 3) С6Н5ОН 4) С6Н5СН2ОН |
| 87. | Формула бензилового спирта 1) СН3СООН 2) С2Н5ОН 3) С6Н5ОН 4) С6Н5СН2ОН |
| 88. | Фенолят натрия C6H5ONa - продукт взаимодействия фенола 1) с гидроксидом натрия 2) с нитратом натрия 3) с хлоридом натрия 4) с сульфатом натрия |
| 89. | Фенол можно обнаружить с помощью 1) натрия 2) хлороводорода 3) водного раствора гидроксида калия 4) хлорида железа (III) |
| 90. | Фенол и бензол реагируют с 1) Вг2 2) Na 3) водным раствором NaOH 4) нитрующей смесью |
| 91. | Соединение С2Н5 - О – С2Н5 относится к классу 1) спиртов 2) простых эфиров 3) сложных эфиров 4) альдегидов |
| 92. | Карболовая кислота – это 1) фенол 2) этанол 3) метанол 4) Толуол |
| 93. | Пикриновая кислота – это 1) 2,4,6-трибромфенол 2) 2,4-динитрофенол 3) 2,4,6-тринитрофенол 4) 2,4,6-тринитротолуол |
| 94. | Этанол реагирует 1) с гидроксидом калия 2) с гидрокарбонатом калия 3) с калием 4) с оксидом калия |
| 95. | Водородная связь образуется между молекулами 1) спиртов 2) фенолов 3) альдегидов 4) алканов |
| 96. | С6Н5СН2ОН относится к классу 1) спиртов 2) карбоновых кислот 3) фенолов 4) альдегидов |
| 97. | Простой эфир – продукт 1) межмолекулярной дегидратации спиртов 2) внутримолекулярной дегидратации спиртов 3) окисления тиолов 4) окисления спиртов |
| 98. | Простым эфиром, тиолом, спиртом являются соответственно 1) CH3OCH3, CH3SCH3, CH3OH 2) CH3COOC2H5, C2H5SH, CH3OH 3) CH3OC2H5, C2H5SH, CH3OH 4) CH3COOC2H5, CH3SC2H5, CH3OH |
| 99. | Условия реакции межмолекулярной дегидратациии этанола 1) H2SO4 (конц.), t = 170 0C 2) H2SO4 (конц.), t = 140 0C 3) H3PO4, t = 300 0C 4) Cu, t. |
| 100. | СH3- S – S – CH3 – ЭТО 1) этантиол 2) диметилтиол 3) диметилдисульфид 4) диметилсульфид |
| Биологически важные реакции карбонильных соединений |
| 101. | Для альдегидов наиболее характерны реакции 1) нуклеофильного присоединения 2) нуклеофильного замещения 3) электрофильного присоединения 4) электрофильного замещения |
| 102. | Основания Шиффа образуются в результате реакции 1) самоокисления-самовосстановления 2) восстановления 3) присоединения-отщепления 4) присоединения |
| 103. | Положительную йодоформную пробу даёт 1) бутанол-1 2) этаналь 3) этанол 4) бутен-2 |
| 104. | 3-метилпентаналь образуется при окислении 1) 3-метилпентанола-3 2) 3-метилпентанола-2 3) 3-метилпентанола-1 4) 3-метилпентановой кислоты |
| 105. | Спирты при взаимодействии с альдегидами образуют 1) основания Шиффа 2) ацетали 3) оксимы 4) карбоновые кислоты |
| 106. | В реакцию альдольной конценсации всупает 1) метаналь 2) бензальдегид 3) бутаналь 4) 2,2-диметилпропаналь |
| 107. | Продукт реакции СН3СНО + LiAlH4 → 1) этанол 2) этаналь 3) этен 4) этановая кислота |
| 108. | Продукт окисления пропаналя 1) пропановая кислота 2) пропанон-2 3) пропен 4) пропан |
| 109. | Формалин – это 1) 40 %-ный раствор метаналя в воде 2) 40 %-ный раствор метанола в воде 3) 40 %-ный раствор этаналя в воде 4) 40 %-ный раствор этанола в воде |
| 110. | Продукт окисления первичного спирта 1) кетон 2) альдегид 3) алкан 4) карбоновая кислота |
| 111. | Продукт окисления вторичного спирта 1) кетон 2) альдегид 3) алкан 4) карбоновая кислота |
| 112. | Красный осадок образуется при нагревании свежеосажденного Сu(ОН)2 1) с фенолом 2) с уксусной кислотой 3) с этиленом 4) с формальдегидом |
| 113. | Качественная реакция на формальдегид – его взаимодействие 1) с водородом 2) с бромом в водном растворе 3) с хлороводородом 4) с аммиачным раствором оксида серебра |
| 114. | Метаналь – это 1) жидкость при н.у. 2) хорошо растворимый в воде газ с резким запахом 3) плохо растворимый в воде газ без запаха 4) хорошо растворимый в воде газ без запаха |
| 115. | Продукт восстановления пропаналя 1) пропановая кислота 2) пропанон-2 3) пропанол-2 4) пропанол-1 |
| 116.. | Ацетали образуются при взаимодействии альдегидов 1) с водородом 2) с аммиачным раствором оксида серебра 3) со свежеосажденным Си(ОН)2 4) со спиртами |
| 117. | Веществом «x» в схеме СН3СНО → x → С2Н4 является 1) уксусная кислота 2) этанол 3) метаналь 4) 1,1-дибромэтан |
| | Карбоновые кислоты - продукты взаимодействия альдегидов 1) с водородом 2) с аммиачным раствором оксида серебра 3) с NaHSO3 4) со спиртами |
| 119. | Спирты - продукты взаимодействия альдегидов 1) с водородом 2) с аммиачным раствором оксида серебра 3) со свежеосажденным Сu(ОН)2 4) со спиртами |
| 120. | Имины - продукты взаимодействия альдегидов 1) с водородом 2) с аммиачным раствором оксида серебра 3) с аминами 4) со спиртами |
| 121. | ЧИСЛО Л-СВЯЗЕЙ ОДИНАКОВО В МОЛЕКУЛАХ 1) С2Н2,СН3СНО 2) С2Н4,СН3СНО 3) СН3ОН, Н2СО 4) С6Н6, С2Н4 |
| 122. | Функциональная группа альдегидов 1) –СОН 2) –СООН 3) –ОН 4) -NО2 |
| | Гомолог этаналя 1) С2Н6О 2) С3Н6О2 3) С4Н8О 4) С5Н12О |
| 124. | Функциональная группа кетонов 1) карбонильная 2) –карбоксильная 3) –гидроксильная 4) –амино |
| 125. | О ⁄⁄ СН3 - СН2 – СН(CH3) - С – Н 1) пентаналь 2) 3-метилбутаналь 3) 4-метилбутаналь 4) 2-метилбутаналь |
| 126. | СНз – С - СНз || О 1) пропаналь 2) пропанол-2 3) пропанон-2 4) пропановая кислота |
| 127. | Фенолформальдегидная смола - продукт реакции 1) поликонденсации 2) дегидратации 3) полимеризации 4) дегидрирования |
| 128. | О ⁄⁄ СН2 = СН - С \ Н 1) пропаналь 2) пропен-2-аль 3) пропен-1-аль 4) пропен-2-ол-1 |
| 129. | В реакцию канниццаро вступает 1) бензальдегид 2) ацетальдегид 3) бензол 4) фенол |
| 130. | В реакцию альдольной конденсации вступает 1) метанол 2) метаналь 3) этанол 4) этаналь |
| 131. | Ацеталь - продукт взаимодействия альдегида 1) с 1 молем водорода 2) с 2 молями водорода 3) с 1 молем спирта 4) с 2 молями спирта |
| 132. | Полуацеталь – продукт взаимодействия альдегида 1) с 1 молем водорода 2) с 2 молями водорода 3) с 1 молем спирта 4) с 2 молями спирта |
| Карбоновые кислоты и их функциональные производные |
| 133. | Функциональная группа карбоновых кислот 1) -СOН 2) -СООН 3) -ОН 4) -С = O |
| 134. | Наиболее сильная кислота 1) СН3СООН 2) НСООН 3) С2Н5СООН 4) С6Н5СООН |
| 135. | Муравьиная кислота 1) С6Н5СООН 2) CH3COOH 3) НCOOH 4) C15H29COOH |
| 136. | Бензойная кислота 1) С6Н5СООН 2) C15H31COOH 3) С17Нз5СООН 4) C15H29COOH |
| 137. | Дает реакцию серебряного зеркала и окрашивает лакмус в красный цвет 1) уксусная кислота 2) муравьиная кислота 3) муравьиный альдегид 4) глюкоза |
| 138. | Формула предельных одноосновных карбоновых кислот 1) CnH2nCOOH 2) CnH2n+1COOH 3) CnH2nO 4) CnH2n-1COOH |
| 139. | СН3СООН + SOCl2 → CH3COCl + SO2 + HCl – это реакция 1) нуклеофильного присоединения 2) нуклеофильного замещения 3) электрофильного присоединения 4) электрофильного замещения |
| 140. | Уксусная кислота вступает в реакцию этерификации 1) с уксусным ангидридом 2) с аммиаком 3) с натрием металлическим 4) с пропанолом |
| 141. | Галогенангидриды - продукты взаимодействия карбоновых кислот 1) с НСl 2) с NaCl 3) c Cl2 4) c PCl5 |
| 142. | Соединение относится к классу 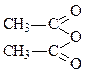 1) галогенанидридов 2) амидов 3) ангидирдов 4) сложных эфиров 1) галогенанидридов 2) амидов 3) ангидирдов 4) сложных эфиров |
| 143. | При нагревании янтарной кислоты протекает реакция 1) декарбоксилирования 2) элиминирования 3) внутримолекулярной дегидратации 4) межмолекулярной дегидратации |
| 144. | При нагревании щавелевой кислоты происходит реакция 1) декарбоксилирования 2) элиминирования 3) внутримолекулярной дегидратации 4) межмолекулярной дегидратации |
| 145. | НООС – СООН – это кислота 1) уксусная 2) пропионовая 3) щавелевая 4) малоновая |
| 146. | Гомологи уксусной кислоты 1) сильные электролиты 2) слабые электролиты 3) неэлектролиты 4) амфотерные соединения |
| 147. | Уксусную кислоту можно получить 1) взаимодействием ацетата натрия с водным раствором С02 2) взаимодействием ацетата натрия с серной кислотой 3) восстановлением ацетальдегида 4) окислением пропанола |
| 148. | Акриловую и пропионовую кислоты можно отличить с помощью 1) бромной воды 2) метилоранжа 3) хлорида натрия 4) гидроксида меди (II) |
| 149. | Сложные эфиры - продукты взаимодействия карбоновых кислот 1) с оксидами металлов 2) с активными металлами 3) с солями 4) со спиртами |
| 150. | Особые свойства муравьиной кислоты связаны с тем, что она 1) имеет наименьшую молярную массу 2) имеет наибольшую степень диссоциации 3) проявляет свойства как кислот, так и альдегидов 4) проявляет свойства как кислот, так и оснований |
| 151. | СН2 = СН - СООН – Структурная формула кислоты 1) щавелевой 2) глутаровой 3) акриловой 4) янтарной |
| | Один из продуктов реакции СН3СООН + С2Н5ОН → 1) этилацетат 2) этилформиат 3) метилэтиловый эфир 4) ацетальдегид |
| | СН3 - С ≡ N – структурная формула 1) ацетонитрила 2) ацетамида 3) уксусного ангидрида 4) ацетата аммония |
| | О ⁄⁄ СН3 - С – структурная формула \ NH2 1) ацетонитрила 2) ацетамида 3) уксусного ангидрида 4) ацетата аммония |
| | Реакция этерификации 1) необратимая 2) протекает в кислой среде 3) протекает в щелочной среде 4) протекает в обычных условиях |
| 156. | Щавелевая кислота НООС – СООН 1) одноосновная 2) двухосновная 3) непредельная 4) трехатомная |
| 157. | НООС - СН2 – СООН → СН3СООН + СO2 – это реакция 1) дегидратации 2) дегидрирования 3) декабоксилирования 4) карбоксилирования |
| 158. | Бензойная кислота С6Н5СООН 1) предельная 2) непредельная 3) ароматическая 4) сильный электролит |
| 159. | O ⁄⁄ R – C - структурная формула \ NH - NH2 1) амида 2) гидразина 3) гидразида 4) гидразона |
| 160. | Продукты кислотного гидролиза метилпропионата 1) метанол и пропановая кислота 2) пропанол и муравьиная кислотв 3) метанол и уксусная кислота 4) этанол и уксусная кислота |
| 161. | Салициловая кислота 1) 2- оксобензойная 2) 2 -оксибензойная 3) 3-оксибензойная 4) 4-оксибензойная |
| 162. | Продукты реакции метилпропионата с раствором NaOH 1) метанол и пропановая кислоты 2) пропанола и формиат натрия 3) метанол и пропионат натрия 4) пропанол и формиат натрия |
| 163. | Продукты реакции гидролиза СН3CОCl 1) СН3СООН и HCl 2) CH3OH и СН3Сl 3) (CH3CO)2O и HCl |
| 164. | СН3СООNH4 - это 1) амид уксусной кислоты 2) ацетамид 3) ацетат аммония |
| 165. | Продукт реакции карбоновой кислоты с аммиаком при нагревании 1) сложный эфир 2) гидразид 3) оксим 4) амид |
| 166. | Продукт реакции СН3СООН + PCl5 1) CH3COH 2) CH3COCl 3) (CH3CO)2O 4) CH3OH |
| 167. | При нагревании амида карбоновой кислоты образуется 1) амин 2) имин 3) нитрат 4) нитрил |
| 168. | Качественной на уксусную кислоту является реакция 1) с Cu(OH)2 2) c FeCl3 3) c NaOH 4) c С2Н5ОН |
| 169. | Непредельные карбоновые кислоты вступают в реакции 1) замещения 2) разложения 3) присоединения 4) гидролиза |
| | Метилфомиат – это 1) простой эфир 2) сложный эфир 3) ангидрид 4) соль |
| Модуль 2. Низкомолекулярные биоорганические соединения как метаболиты и регуляторы метаболизма |
| Гетерофункциональные соединения |
| 171. | Тривиальное название оксикислоты НООС-СН2- СН(ОН)-СООН 1) лимонная кислота 2) яблочная кислота 3) молочная кислота 4) винная кислота |
| 172. | Оксокислотами являются 1) пировиноградная, гликолевая, ацетоуксусная кислоты 2) щавелевоуксусная, α-оксоглутаровая, янтарная кислоты 3) лимонная, винная, молочная кислоты 4) пировиноградная, щавелевоуксусная, ацетоуксусная кислоты |
| 173. | Для ацетоуксусного эфира характерна 1) лактим-лактамная таутомерия 2) цикло-оксо таутомерия 3) кето-енольная таутомерия 4) енамино-иминная таутомерия |
| 174. | В организме у больных сахарным диабетом накапливается 1) пировиноградная кислота 2) молочная кислота 3) ацетоуксусная кислота 4) салициловая кислота |
| 175. | Новокаин и анестезин - производные 1) пара-аминобензойной кислоты 2) салициловой кислоты 3) фолиевой кислоты 4) угольной кислоты |
| 176. | Аспирин является производным 1) салициловой кислоты по гидроксильной группе 2) салициловой кислоты по карбоксильной группе 3) пара-аминобензойной кислоты по аминогруппе 4) пара-аминобензойной кислоты по карбоксильной группе |
| 177. | НО - СН2 – СООН – это кислота 1) молочная 2) яблочная 3) гликолевая 4) глиоксалевая |
| 178. | Мочевина СО(NH2)2 – функциональное производное кислоты 1) молочной 2) угольной 3) гликолевой 4) яблочной |
| 179. | Функциональное производное кислоты угольной кислоты 1) аспирин 2) анальгин 3) новокаин 4) мочевина |
| 180. | Функциональное производное кислоты угольной кислоты 1) аспирин 2) анальгин 3) фосген 4) новокаин |
| Пятичленные гетероциклические соединения |
| 181. | Представителем ароматических гетероциклов является 1) тетрагидрофуран 2) пирролидин 3) пиразолин 4) пиррол |
| 182. | Продукт восстановления пиррола 1) пирролидин 2) тетрагидрофуран 3) тиофан 4) пиперидин |
| 183. | Реагент для сульфирования фурана 1) серная кислота 2) тионилхлорид 3) пиридинсульфотриоксид 4) бисульфит натрия |
| 184. | Серотонин 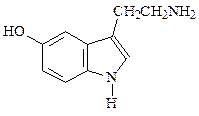 1) является производным пурина 2) является неароматическим гетероциклом 3) является производным пиримидина 4) является производным индола 1) является производным пурина 2) является неароматическим гетероциклом 3) является производным пиримидина 4) является производным индола |
| 185. | Структурный фрагмент гистамина 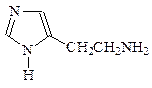 1) пиразол 2) имидазол 3) пурин 4) оксазол 1) пиразол 2) имидазол 3) пурин 4) оксазол |
| 186. | Пирролу соответствует утверждение 1) является ацидофобным гетероциклом 2) относятся к шестичленным гетероциклам 3) содержит два атома азота 4) при гидрировании образует пиридин |
| 187. | Тиофен имеет в цикле 1) 3 атома 2) 4 атома 3) 5 атомов 4) 6 атомов |
| 188. | Антипирин, амидопирин, анальгин созданы на основе 1) имидазола 2) пиразолона-5 3) хинолина 4) пиррола |
| 189. | Тиофен в качестве гетероатома содержит атом 1) кислорода 2) азота 3) фосфора 4) серы |
| 190. | Пиррол в качестве гетероатома содержит атом 1) кислорода 2) азота 3) фосфора 4) серы |
| 191. | Фуран в качестве гетероатома содержит атом 1) кислорода 2) азота 3) фосфора 4) серы |
| 192. | Реакция Юрьева применяется для получения 1) фурана 2) пиридина 3) анилина 4) индола |
| 193. | Реагент для нитрования фурана 1) NO2 2) HNO3 3) CH3COONO2 4) HNO2 |
| 194. | Реагент для нитрования пиррола 1) NO2 2) HNO3 3) CH3COONO2 4) HNO2 |
| 195. | Ацидофобным является 1) тиофен 2) анилин 3) пиррол 4) фенол |
| Шестичленные гетероциклические соединения |
| 196. | Шестичленный гетероцикл с одним атомом азота 1) пиридин 2) пиримидин 3) пурин 4) пиррол |
| 197. | Водный раствор пиридина окрашивает лакмус 1) в синий цвет 2) в красный цвет 3) в фиолетовый цвет 4) в желтый цвет |
| 198. | При нитровании пиридина образеутся 1) 2-нитропиридин 2) 3-нитропиридин 3) 4-нитропиридин 4) 6 -нитропиридин |
| 199. | Хинозол, 5-нок, энтеросептол - это производные 1) пиридина 2) пиримидина 3) хинолина 4) изохинолина |
| 200. | В состав тиамина (витамина в1) входит гетероцикл 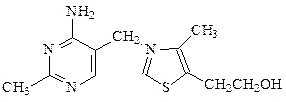 1) пиридин 2) пиримидин 3) пиррол 4) пиперидин 1) пиридин 2) пиримидин 3) пиррол 4) пиперидин |
| 201. | В состав молекулы никотиновой кислоты входит гетероцикл 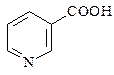 1) хинолин 2) пиперидин 3) пиримидин 4) пиридин 1) хинолин 2) пиперидин 3) пиримидин 4) пиридин |
| 202. | Структура пурина образована за счет конденсированных ядер 1) пиридина и имидазола 2) пиридина и пиразола 3) пиримидина и имидазола 4) пиримидина и пиразола |
| 203. | Взаимодействие пиридина С NaNH2 – это реакция 1) Кучерова 2) Зинина 3) Лебедева 4) Чичибабина |
| 204. | Продукт полного восстановления пиридина – это 1) пирролидин 2) тетрагидрофуран 3) тиофан пиперидин |
| Моносахариды |
| 205. | Глюкоза – это 1) многоатомный спирт 2) альдегидоспирт 3) кетоспирт 4) аминоспирт |
| 206. | Функциональная группа в циклической форме глюкозы 1) гидроксильная 2) карбоксильная 3) альдегидная 4) карбонильная |
| 207. | Глюкоза, как многоатомный спирт, взаимодействует 1) с гидроксидом меди (II) при комнатной температуре 2) с аммиачным раствором оксида серебра при нагревании 3) с водородом 4) с гидроксидом меди (II) при нагревании |
| 208. | Для полной этерификации 1 моль глюкозы необходимо 1) 2 моль уксусной кислоты 2) 3 моль уксусной кислоты 3) 4 моль уксусной кислоты 4) 5 моль уксусной кислоты |
| 209. | Эпимером D-Рибозы является 1) D-глюкоза 2) D-фруктооза 3) D-ксилоза 4) D-рибулоза |
| 210. | Приведенная формула соответствует 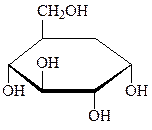 1) α-D-глюкопиранозе 2) β- D-глюкопиранозе 3) α-D-маннопиранозе 4) β- D-маннопиранозе 1) α-D-глюкопиранозе 2) β- D-глюкопиранозе 3) α-D-маннопиранозе 4) β- D-маннопиранозе |
| 211. | Красное окрашивание с резорцином дает (реакция Селиванова) 1) глюкоза 2) фруктоза 3) манноза 4) галактоза |
| 212. | По структуре к моносахаридам близок 1) витамин РР 2) витамин С 3) витамин В6, 4) витамин В1 |
| 213. | Реакцией моносахаридов с алкилгалогенидами получают 1) сложные эфиры 2) многоатомные спирты 3) гликозиды 4) простые эфиры |
| 214. | Сорбит – продукт реакции 1) мягкого окисления ксилозы 2) жесткого окисления глюкозы 3) восстановления глюкозы 4) восстановления галактозы |
| 215. | Альдоновые кислоты получают в результате 1) жесткого окисления альдоз 2) ферментативного окисления альдоз 3) мягкого окисления альдоз 4) восстановления альдоз |
| 216. | С6Н12О6 – формула 1) фруктозы 2) рибозы 3) дезоксирибозы 4) лактозы |
| 217. | С5Н10О4 – формула 1) глюкозы 2) фруктозы 3) рибозы 4) дезоксирибозы |
| Ди- и полисахариды |
| 218. | С12Н22О11 – формула 1) глюкозы 2) сахарозы 3) ксилозы 4) крахмала |
| 219. | Лактоза 1) состоит из двух остатков глюкозы 2) состоит из двух остатков галактозы 3) обладает восстанавливающими свойствами 4) содержит (1→3) гликозидную связь |
| 220. | На рисунке изображена 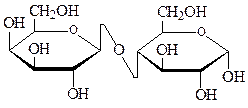 1) β-D-глюкопиранозил-(1→4)-α-D-глюкопираноза 2) α-D-глюкопиранозил-(1→4)-β-D-глюкопираноза 3) β-D-галактопиранозил-(1→4)-α-D-глюкопираноза 4) α-D-галактопиранозил-(1→4)-α-D-глюкопираноза 1) β-D-глюкопиранозил-(1→4)-α-D-глюкопираноза 2) α-D-глюкопиранозил-(1→4)-β-D-глюкопираноза 3) β-D-галактопиранозил-(1→4)-α-D-глюкопираноза 4) α-D-галактопиранозил-(1→4)-α-D-глюкопираноза |
| 221. | Солодовым сахаром называют 1) сахарозу 2) лактозу 3) целлобиозу 4) мальтозу |
| 222. | Продукт гидролиза сазарозы 1) D-глюкоза и D-глюкоза 2) D-глюкоза и D-фруктоза 3) D-глюкоза и D-галактоза 4) D-галактоза и D-фруктоза |
| 223. | Имеет строго линейное строение 1) целлюлоза 2) амилопектин 3) гликоген 4) декстран |
| 224. | Является гетерополисахаридом 1) крахмал 2) гликоген 3) целлюлоза 4) гепарин |
| 225. | В комплексе с йодом синий цвет имеет 1) амилоза 2) декстран 3) амилопектин 4) целлюлоза |
| 226. | Число моносахаридных остатков в олигосахаридах 1) 10-100 2) 2-10 3) 2-20 |
| 227. | Целлюлоза образует сложные эфиры при взаимодействии с 1) азотной кислотой 2) соляной кислотой 3) кислородом 4) водородом |
| 228. | Число ОН-групп в элементарных звеньях целлюлозы и крахмала 1) 5 2) 4 3) 3 4) 2 |
| 229. | ПАТОКОЙ НАЗЫВАЕТСЯ 1) СМЕСЬ ЦЕЛЛЮЛОЗЫ И ГЛЮКОЗЫ 2) смесь декстринов и глюкозы 3) смесь декстринов и фруктозы 4) смесь фруктозы и глюкозы |
| 230. | Конечный продукт гидролиза целлюлозы 1) фруктоза 2) α-глюкоза 3) β-глюкоза 4) мальтоза |
| 231. | Конечный продукт гидролиза крахмала 1) фруктоза 2) α-глюкоза 3) β-глюкоза 4) мальтоза |
| 232. | Реакция «серебряного зеркала» характерна для веществ 1) глюкозы, глицерина, сахарозы 2) глюкозы, сахарозы, формальдегида 3) глюкозы, муравьиной кислоты, уксусного альдегида 4) фруктозы, глицерина, формальдегида |
| 233. | Изменение угла вращения свежеприготовленных растворов сахаров 1) стереоизомерия 2) таутомерия 3) изомерия 4) мутаротация |
| α-Аминокислоты. Пептиды. Белки |
| 234. | Группу –SH содержит аминокислота 1) аланин 2) метионин 3) аспарагин 4) цистеин |
| 235. | Группу –СONH2 содержит аминокислота 1) лизин 2) валин 3) тирозин 4) глутамин |
| 236. | НЕЗАМЕНИМАЯ В ОРГАНИЗМЕ Α-АМИНОКИСЛОТА 1) глицин 2) треонин 3) аспарагин |
| 237. | При дезаминировании аминокислот in vitro образуется 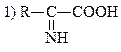 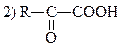 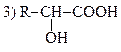 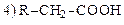 |
| 238. | Для количественного определения карбоксильных групп в α-аминокислотах используется реакция 1) реакция аминокислот с азотистой кислотой 2) реакция аминокислот с формальдегидом 3) биуретовая реакция 4) нингидриновая реакция |
| 239. | Правильное название трипептида 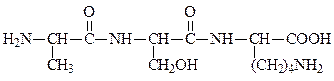 1) аланилтреониллизин 2) аланилсериллейцин 3) аланилтреониллейцин 4) аланилсериллизин 1) аланилтреониллизин 2) аланилсериллейцин 3) аланилтреониллейцин 4) аланилсериллизин |
| 240. | Реакция, основанная на способности пептидной группы белков и полипептидов образовывать с ионами меди в щелочной среде комплексные соединения фиолетового цвета 1) биуретовая 2) ксантопротеиновая 3) Коля 4) нингидриновая |
| 241. | Аминоуксусная кислота называется 1) глицином 2) аланином 3) лизином 4) валином |
| 242. | 2- аминопропионовая кислота называется 1) глицином 2) аланином 3) лизином 4) валином |
| 243. | Аминокислоты образуют пептиды в результате реакции 1) полимеризации 2) поликонденсации 3) гидратации |
| 244. | Пептидная связь образована фрагментом 1) - СОО- 2) - N = N- 3) - CО-NH- 4) - СО – NH2 |
| 245. | Денатурация белка сопровождается 1) разрушением вторичной, третичной и четвертичной структур 2) распадом молекулы белка на исходные аминокислоты 3) окислением аминокислот, входящих в состав белка 4) восстановлением аминокислот, входящих в состав белка |
| 246. | Аминокислоту можно получить при полном гидролизе 1) белка 2) крахмала 3) твердого жира 4) мыла |
| 247. | Число пептидных связей в молекуле трипептида 1) 3 2) 2 3) 4 4) 1 |
| 248. | Хлороводород образует соль при взаимодействии с 1) фенолом 2) аланином 3) нитробензолом 4) этаном |
| 249. | Амфотерными свойствми обладает 1) метиламин 2) анилин 3) аминоуксусная кислота 4) акролеин |
| 250. | Сложный эфир – продукт взаимодйствия глицина с 1) С2Н5ОН (кислая среда) 2) НВг 3) NH2CH2COOH 4) РCl5 |
| | Глицин образует хлорангидрид при взаимодействии с 1) С2Н5ОН (кислая среда) 2) НВг 3) NH2CH2COOH 4) РCl5 |
| 252. | Продукт взаимодействия аминокислоты с аммиаком при нагревании 1) амид 2) амин 3) ангидрид 4) гидразид |
| 253. | Незаменимая α-аминокислота 1) лейцин 2) цистеин 3) глутамин 4) аргинин |
| 254. | Новая аминокислота образуется в реакции 1) декарбоксилирования 2) дезаминирования 3) переаминирования 4) дегидратации |
| 255. | Н2N –CH-COOH + HNO2 → HO-CH-COOH + N2 + H2O – ЭТО РЕАКЦИЯ │ │ R R 1) окислительное дезаминирования in vivo 2) неокислительное дезаминирования in vivo 3) дезаминирование in vitro |
| 256. | Н2N –CH-COOH + СН3СОCl → O=C – NH -CH-COOH + HCl – ЭТО РЕАКЦИЯ │ │ │ R CH3 R 1) N-ацилирования 2) солеобразования 3) аминирования 4) дезаминирования |
| 257. | При частичном гидролизе белков образуются 1) аминокислоты 2) пептиды 3) пиримидиновые основания 4) пуриновые основания |
| 258. | Для обнаружения ароматических и гетероциклических аминокислот в составе белка используется реакция 1) ксантопротеиновая (HNO3 конц.) 2) биуретовая (свежеприготовленный Cu(OH)2) 3) образования осадка PbS 4) нингидриновая проба |
| 259. | Для обнаружения пептиддной связи в белках используется реакция 1) ксантопротеиновая (HNO3 конц.) 2) биуретовая (свежеприготовленный Cu(OH)2) 3) образования осадка PbS 4) нингидриновая проба |
| 260. | Для обнаружения серусодержащих аминокислот в составе белка используется реакция 1) ксантопротеиновая (HNO3 конц.) 2) биуретовая (свежеприготовленный Cu(OH)2) 3) образования осадка PbS 4) нингидриновая проба |
| Модуль 3. Биополимеры и их структурные компоненты. Липиды |
| Нуклеиновые кислоты. Нуклеотидные коферменты |
| 261. | Аденину комплементарен 1) цитозин 2) тимин 3) гуанин 4) гипоксантин |
| 262. | Пуриновое основание - это 1) аденин 2) цитозин 3) урацил 4) пиридин |
| 263. | Пуриновое основание - это 1) тимин 2) гуанин 3) цитозин |
| 264. | Частичный гидролиз нуклеиновых кислот приводит к образованию 1) смеси нуклеотидов 2) нуклеозидов 3) остатка моносахарида 4) остатка азотистого основания |
| 265. | Моносахарид, входящий в состав ДНК 1) глюкоза 2) фруктоза 3) рибоза 4) дезоксирибоза |
| 266. | Моносахарид, входящий в состав РНК 1) глюкоза 2) фруктоза 3) рибоза 4) дезоксирибоза |
| 267. | Кислота в составе нуклеотидов 1) соляная 2) уксусная 3) серная 4) ортофосфорная |
| 268. | Число водородных связей между гуанином и цитозином 1) 1 2) 2 3) 3 4) 4 |
| 269. | На рисунке изображен 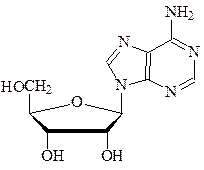 1) аденозин 2) 5'-адениловая кислота 3) аденозинмонофосфат 4) дезоксиаденозин 1) аденозин 2) 5'-адениловая кислота 3) аденозинмонофосфат 4) дезоксиаденозин |
| 270. | Связь между нуклеиновым основанием и углеводным остатком в нуклеозиде 1) амидная 2) сложноэфирная 3) N-гликозидная 4) С-гликозидная |
| 271. | Вирусы растений содержат 1) белки и РНК 2) белки и ДНК 3) белки, РНК и ДНК 4) РНК и ДНК |
| 272. | На рисунке изображен 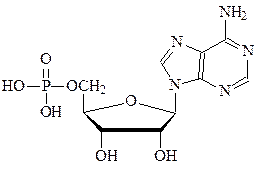 1) нуклеозид 2) кофермент НАДН 3) полисахарид 4) нуклеотид 1) нуклеозид 2) кофермент НАДН 3) полисахарид 4) нуклеотид |
| 273. | Строение второй цепи ДНК, соответствующейпоследовательности оснований АГТ в первой 1) ТЦУ 2) УЦА 3) ТЦА 4) ГЦА |
| 274. | При полном гидролизе нуклеозида образуются 1) углевод и ортофосфорная кислота 2) углевод и пуриновое основание 3) углевод и пиридин 4) углевод, ортофосфорная кислота и пуриновое основание |
| 275. | При полном гидролизе нуклеотида образуются 1) углевод и ортофосфорная кислота 2) углевод и пуриновое основание 3) углевод и пиридин 4) углевод, ортофосфорная кислота и пуриновое основание |
| 276. | Лактим-лактамная таутомерия характерна для 1) аденина 2) гуанина 3) пиридина 4) хинолина |
| 277. | Нуклеотиды – это 1) фосфаты нуклеозидов 2) нитраты нуклеозидов 3) хлориды нуклеозидов 4) нитраты нуклеозидов |
| 278. | Аденозин - 5’ – Монофосфорная кислота – это 1) АТФ 2) АМФ 3) АДФ 4) ЭДТА |
| 279. | АТФ – это 1) 5’- аденозилмонофосфат 2) 5’- аденозилдифосфат 3) 5’- аденозилтрифосфат |
| 280. | Аденин, гуанин, цитозин, тимин, дезоксирибоза, Н3РО4 входит в состав 1) ДНК 2) РНК 3) АТФ 4) ЭДТА |
| 281. | Аденин, гуанин, цитозин, урацил, рибоза, Н3РО4 входит в состав 1) ДНК 2) РНК 3) АТФ |
| 282. | ДНК находится 1) в ядрах клеток 2) в рибосомах клеток 3) в протоплазме клеток |
| 283. | Гидролиз РНК осуществляется в среде 1) щелочной 2) кислой 3) нейтральной |
| Омыляемые липиды |
| 284. | Масса непредельных жирных кислот, которая должна ежедневно поступать в органзим человека 1) 1 г 2) 3 г 3) 5 г 4) 10 г |
| 285. | Незаменымые для человека жирные кислоты 1) пальмитиновая, стеариновая 2) олеиновая, арахидоновая 3) олеиновая, линолевая 4) линолевая, линоленовая |
| 286. | Реагенты, позволяющие определить меру ненасыщенности триацилглицеринов 1) водный раствор NaOH, водный раствор KMnO4, H2 2) J2, водный раствор KMnO4, H2 3) J2, перекись водорода, H2 4) водный раствор NaOH, водный раствор KMnO4, J2 |
| 287. | Название соединения 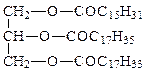 1) 1-пальмитоил-2-олеоил-3-стеароилглицерин 2) 1-олеоил-2-пальмитоил-3-стеароилглицерин 3) 1-пальмитоил-2-стеароил-3-олеоиноилглицерин 4) 1-пальмитоил-2-стеароил-3-олеоилглицерин 1) 1-пальмитоил-2-олеоил-3-стеароилглицерин 2) 1-олеоил-2-пальмитоил-3-стеароилглицерин 3) 1-пальмитоил-2-стеароил-3-олеоиноилглицерин 4) 1-пальмитоил-2-стеароил-3-олеоилглицерин |
| 288. | Структуре биологически важных жирных кислот соответствует утверждение 1) насыщенные участки углеводородного радикала находятся в зигзагообразной конформации 2) жирные кислоты могут быть только насыщенными 3) число атомов углерода колеблется от 1 до 20 4) содержат одну или две карбоксильные группы |
| 289. | Производными аминоспирта сфингозина являются 1) церамиды 2) коламинкефалины 3) воски 4) серинкефалины |
| 290. | Сложные липиды - это 1) жиры, масла 2) фосфолипиды 3) воски 4) церамиды |
| 291. | Простые липиды – это 1) жиры, масла 2) фосфолипиды 3) гликолипиды 4) сфингомиелины |
| 292. | Мыла образуются в результате реакции 1) щелочного гидролиза жиров 2) кислотного гидролиза жиров 3) окисления жиров 4) восстановления жиров |
| Неомыляемые липиды |
| 293. | Название соединения 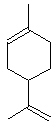 1) камфора 2) цитраль 3) α-пинен 4) лимонен 1) камфора 2) цитраль 3) α-пинен 4) лимонен |
| 294. | α-пинен 1) монотерпен 2) дитерпен 3) тритерпен 4) тетратерпен |
| 295. | Мирцен 1) монотерпен 2) дитерпен 3) тритерпен 4) тетратерпен |
| 296. | Структуре каротиноидов соответствет утверждение 1) в основе структуры каротиноидов лежит скелет гонана 2) большинство каротиноидов относится к монотерпенам 3) для каротиноидов характерна цис-конфигурация двойных связей 4) молекулы каротиноидов содержат значительное количество сопряженных двойных связей, поэтому имеют желто-красную окраску |
| 297. | Камфора 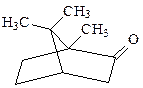 1) является тритерпеном 2) содержит 3 звена изопрена 3) проявляет свойства кетона 4) имеет 4 центра хиральности 1) является тритерпеном 2) содержит 3 звена изопрена 3) проявляет свойства кетона 4) имеет 4 центра хиральности |
| 298. | Название соединения 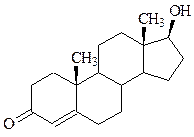 1) тестостерон 2) эстрон 3) прогестерон 4) холестерин 1) тестостерон 2) эстрон 3) прогестерон 4) холестерин |
| 299. | В молекуле эстрона отстутствует  1) боковая цепь у С17 2) альдегидная группа 3) ароматическое кольцо 4) фенольный гидроксил 1) боковая цепь у С17 2) альдегидная группа 3) ароматическое кольцо 4) фенольный гидроксил |
| 300. | К мужским половым гормонам относятся 1) эстрадиол, эстрон 2) тестостерон, андростерон 3) тестостерон, эстрадиол 4) прогестерон, холестан |
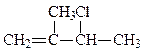 2)
2) 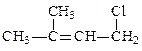 3)
3) 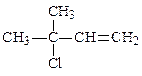 4)
4) 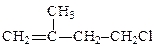
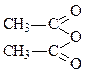 1) галогенанидридов 2) амидов 3) ангидирдов 4) сложных эфиров
1) галогенанидридов 2) амидов 3) ангидирдов 4) сложных эфиров 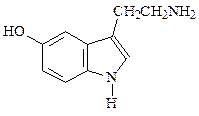 1) является производным пурина 2) является неароматическим гетероциклом 3) является производным пиримидина 4) является производным индола
1) является производным пурина 2) является неароматическим гетероциклом 3) является производным пиримидина 4) является производным индола 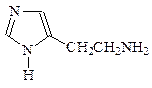 1) пиразол 2) имидазол 3) пурин 4) оксазол
1) пиразол 2) имидазол 3) пурин 4) оксазол 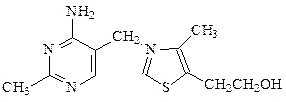 1) пиридин 2) пиримидин 3) пиррол 4) пиперидин
1) пиридин 2) пиримидин 3) пиррол 4) пиперидин 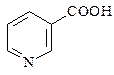 1) хинолин 2) пиперидин 3) пиримидин 4) пиридин
1) хинолин 2) пиперидин 3) пиримидин 4) пиридин 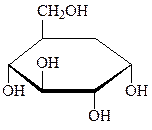 1) α-D-глюкопиранозе 2) β- D-глюкопиранозе 3) α-D-маннопиранозе 4) β- D-маннопиранозе
1) α-D-глюкопиранозе 2) β- D-глюкопиранозе 3) α-D-маннопиранозе 4) β- D-маннопиранозе 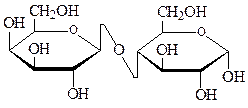 1) β-D-глюкопиранозил-(1→4)-α-D-глюкопираноза 2) α-D-глюкопиранозил-(1→4)-β-D-глюкопираноза 3) β-D-галактопиранозил-(1→4)-α-D-глюкопираноза 4) α-D-галактопиранозил-(1→4)-α-D-глюкопираноза
1) β-D-глюкопиранозил-(1→4)-α-D-глюкопираноза 2) α-D-глюкопиранозил-(1→4)-β-D-глюкопираноза 3) β-D-галактопиранозил-(1→4)-α-D-глюкопираноза 4) α-D-галактопиранозил-(1→4)-α-D-глюкопираноза 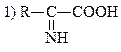
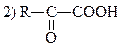
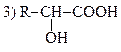
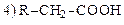
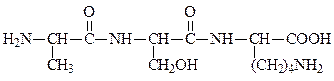 1) аланилтреониллизин 2) аланилсериллейцин 3) аланилтреониллейцин 4) аланилсериллизин
1) аланилтреониллизин 2) аланилсериллейцин 3) аланилтреониллейцин 4) аланилсериллизин 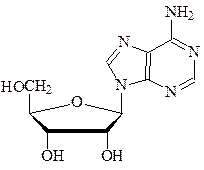 1) аденозин 2) 5'-адениловая кислота 3) аденозинмонофосфат 4) дезоксиаденозин
1) аденозин 2) 5'-адениловая кислота 3) аденозинмонофосфат 4) дезоксиаденозин 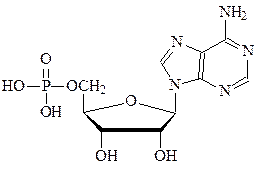 1) нуклеозид 2) кофермент НАДН 3) полисахарид 4) нуклеотид
1) нуклеозид 2) кофермент НАДН 3) полисахарид 4) нуклеотид 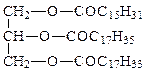 1) 1-пальмитоил-2-олеоил-3-стеароилглицерин 2) 1-олеоил-2-пальмитоил-3-стеароилглицерин 3) 1-пальмитоил-2-стеароил-3-олеоиноилглицерин 4) 1-пальмитоил-2-стеароил-3-олеоилглицерин
1) 1-пальмитоил-2-олеоил-3-стеароилглицерин 2) 1-олеоил-2-пальмитоил-3-стеароилглицерин 3) 1-пальмитоил-2-стеароил-3-олеоиноилглицерин 4) 1-пальмитоил-2-стеароил-3-олеоилглицерин  1) камфора 2) цитраль 3) α-пинен 4) лимонен
1) камфора 2) цитраль 3) α-пинен 4) лимонен 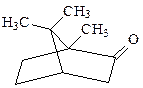 1) является тритерпеном 2) содержит 3 звена изопрена 3) проявляет свойства кетона 4) имеет 4 центра хиральности
1) является тритерпеном 2) содержит 3 звена изопрена 3) проявляет свойства кетона 4) имеет 4 центра хиральности 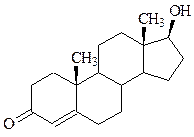 1) тестостерон 2) эстрон 3) прогестерон 4) холестерин
1) тестостерон 2) эстрон 3) прогестерон 4) холестерин  1) боковая цепь у С17 2) альдегидная группа 3) ароматическое кольцо 4) фенольный гидроксил
1) боковая цепь у С17 2) альдегидная группа 3) ароматическое кольцо 4) фенольный гидроксил 